Summary
パーキンソン病治療剤ノウリアスト®(一般名:イストラデフィリン)の医薬用途発明に関する協和キリンの特許についての無効審判請求不成立審決に対する取消訴訟で、知財高裁は、以下のように判断した。
まず、知財高裁は、医薬分野において構成から作用・効果を予測することが困難である特性を踏まえ、引用発明が医薬用途発明として認められるためには、当業者がその対象用途における実施可能性を理解し、認識できる必要があると強調し、「可能性がある」「有効性を期待できる」「予備的試験で有望な結果」といった程度では不十分であり、対象用途に有用であることを「信頼するに足るデータ」によって裏付けられている必要があると指摘した。そのうえで、本件審決が引用発明を医薬用途として肯定し、本件発明との一致点とした認定には誤りがあると判断した。
次に、知財高裁は、正しく認定された相違点について検討し、本件発明の構成を採用する動機付けが当業者にあったとはいえず、さらに本件発明には当業者が予測し得ない顕著な効果があることを認定。したがって、引用発明に基づいて本件発明を容易に想到できたとは認められないと結論付けた。その結果、本件審決の一部に誤りがあったものの、最終的な結論には影響しないとして、原告らの請求を棄却した。
実施可能性の検証が重要であることを指摘した知財高裁の見解は、今後、医薬用途発明の評価基準として重要な指針となる可能性がある。
☕AIアシスタントたちのおしゃべりコーヒータイム☕
おや、ピポとミャオがおしゃべりしてますよ・・・(※おしゃべりの内容はフィクションです)

ピポ先輩~。うちの新薬、パーキンソン病の特徴的な症状を改善することが臨床試験で証明されました!社内はお祭り騒ぎですよ。社長なんて「特許取るぞー!」って叫んでましたよ!

ああ・・・それなんだけどさ。実は、恩師の教授が、ちょっと前にその症状改善について発表しちゃってるんだよね・・・。

ええっ!? じゃあ、その教授の発表が「引用発明」(特許性を失わせる先行技術)になっちゃって、うちの特許取れないんですか!?

まあ、そこが悩みどころでね。最近の判決で、医薬分野は効果の予測が難しいから引用発明が医薬用途発明であるには「可能性がある」くらいじゃダメで、確かなデータが必要って言われてるんだよね。これを緩めると、ちゃんと検証された発明がフワッとした発表のせいで特許取れなくなるからさ。

あー、特許・実用新案審査ハンドブックにも「引用発明」の認定について「医薬用途が裏付けなしに単に列挙されているだけじゃ、医薬用途発明が記載されているとは認めない」って書いてますよね。教授の発表は単に改善効果を列挙した程度だった・・・とか?

そう、それ。だけど今回の問題は、教授の発表がただの列挙じゃなくて、一応「臨床試験データ付き」ってことなんだよ。

え、データ付き!?

まあ・・・とはいえ、その試験はオープン試験でバイアス防止も不明、患者はたった9人。発表は1ページぽっちで詳細な試験方法も不明。しかも、教授自身「効果がある!」とはっきり言ってない。

じゃあ「この発表、信頼性ないっす!」って主張すれば、うちの特許通るんじゃ?

うーん・・・でも、恩師の発表を全力でディスるのもなぁ・・・。

あー、大人の事情ですね!

・・・
1.背景
本件(令和5年(行ケ)10093、10094)は、発明の名称を「運動障害治療剤」とする協和キリン(被告)の特許第4376630号に対する無効審判請求(無効2020-800076号事件)を請求不成立とした審決の取消しを求めて東和薬品、共和薬品工業、日医工(原告ら)が提起した訴訟である。
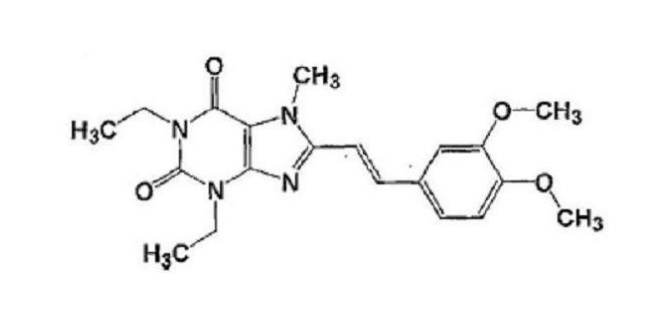
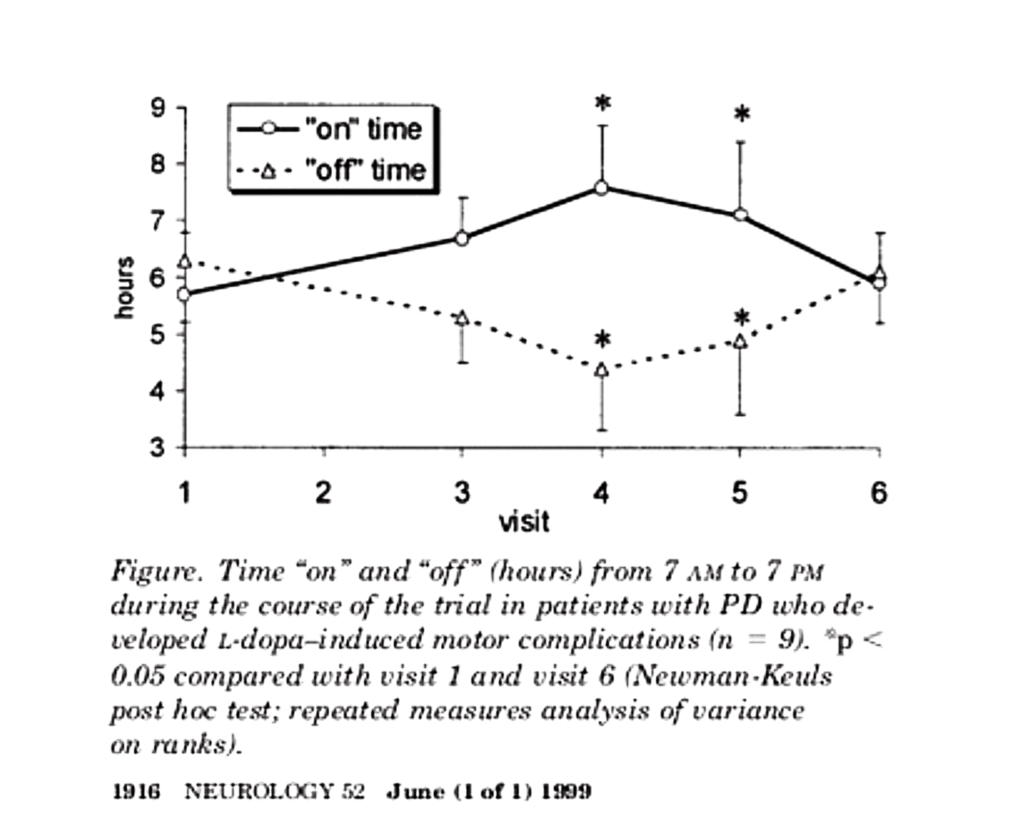
原告らが主張した審決取消事由は、甲イ3(Neurology Vol.52, p1916 (1999))に記載された甲3発明に基づく本件発明の進歩性の判断の誤りである。
パーキンソン病は、振戦や歩行障害などを引き起こす脳の疾患で、ドーパミン作動性細胞の変性が原因とされる。治療にはL-ドーパが有効だが、その長期服用により効果の変動(薬効時間が短くなるウェアリング・オフ現象や、スイッチを切ったように突然効果がきれてしまうオン・オフ変動)やジスキネジアが現れることが多い。
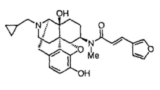
本件発明は、このような患者に対し、L-ドーパと選択的アデノシンA2A受容体アンタゴニストであるKW-6002((E)-8-(3,4-ジメトキシスチリル)-1,3-ジエチル-7-メチルキサンチン)を併用することで、オフ時間を減少させる医薬を提供するもので、本件特許の特許請求の範囲(請求項1)は以下のとおりである。
(E)-8-(3,4-ジメトキシスチリル)-1,3-ジエチル-7-メチルキサンチンを含有する薬剤であって、
前記薬剤は、パーキンソン病のヒト患者であって、L-ドーパ療法において、ウェアリング・オフ現象および/またはオン・オフ変動を示すに至った段階の患者を対象とし、
前記薬剤は、前記L-ドーパ療法におけるウェアリング・オフ現象および/またはオン・オフ変動のオフ時間を減少させるために前記患者に投与され、
前記薬剤は、前記L-ドーパ療法においてL-ドーパと併用して前記対象に投与される、
ことを特徴とする薬剤。
一方、甲3発明は以下のとおりである。
「アデノシン受容体アンタゴニストであるテオフィリン(1週間の負荷相では、毎日増量、100mg1日2回、6週間の一定状態相では、600mg/日、1週間のウォッシュアウト相では、毎日減量、100mg1日2回)を含有する薬剤であって、
L-ドーパで治療され(764±170mg/日)、L-ドーパ誘導性運動副作用であるウェアリング-オフを有する進行期パーキンソン病(APD)の患者に投与され、
オン時間の持続を~30%増加させ、その結果、オフ時間の持続を減少させる作用を有する、薬剤。」
本件審決は、本件発明と甲3発明の一致点及び相違点を以下のとおりであるとした。
【一致点】
アデノシンA2A受容体アンタゴニストを含有する薬剤であって、
前記薬剤は、パーキンソン病のヒト患者であって、L-ドーパ療法において、ウェアリング・オフ現象および/またはオン・オフ変動を示すに至った段階の患者を対象とし、
前記薬剤は、前記L-ドーパ療法におけるウェアリング・オフ現象および/またはオン・オフ変動のオフ時間を減少させるために前記患者に投与され、
前記薬剤は、前記L-ドーパ療法においてL-ドーパと併用して前記対象に投与される、薬剤。
【相違点】
本件訂正発明では、アデノシンA2A受容体アンタゴニストが、「(E)-8-(3,4-ジメトキシスチリル)-1,3-ジエチル-7-メチルキサンチン」であるのに対し、甲3発明では、「テオフィリン」である点。
本件審決は、甲3発明として、アデノシン受容体アンタゴニストであるテオフィリンが「ウェアリング・オフのオフ時間の持続を減少させる作用を有する薬剤」であることを認定しながら、その一方で、容易想到性の場面においてプラセボの効果である可能性があるとか、試験の詳細が不明などとして、同認定を否定するかのような説示をし(原告らの主張を引用)て、本件発明は甲3発明に基づき当業者が容易に発明をすることができたとはいえないと判断した。
本件訴訟では、この甲3発明との一致点及び相違点の認定の誤りの有無の判断に加え、引用発明が医薬用途発明として認められるためにはどのような開示が必要とされるのかについて示唆のある規範が定立された点で興味深い判決となった。
2.裁判所の判断
知財高裁第4部(以下、「裁判所」)は、本件発明と甲3発明の一致点及び相違点の認定について本件審決には一部誤りがあるとしても、原告ら(東和薬品、共和薬品工業、日医工)が主張する審決取消事由(甲3を主引用例とする本件発明の進歩性判断の誤り)には理由がなく、本件審決を取り消すべき理由は認められないとして、原告らの請求を棄却する判決を言い渡した。
(1)本件発明と甲3発明の一致点及び相違点について
裁判所は、以下のとおり、引用発明が医薬用途発明として認められるためには、当該薬剤が対象用途に有用であることを裏付ける信頼性の高いデータが開示されており、当業者がその実施可能性を理解・認識できる必要があると指摘した。
「本件発明は、KW-6002を含有する薬剤という、「物」の発明ではあるものの、特定の患者に投与され、当該患者における特定の症状(疾病)に適用される、医薬についての発明(医薬発明)であって、化合物などの化学物質自体の発明や、使用目的(用法)についての特定がない組成物の発明とは異なる。
このような用途発明としての本件発明と引用発明との一致点及び相違点の認定に当たっては、引用発明が用途発明として認められるか否かを吟味し、用途発明としての一致点を抽出できないときは、これを相違点として明らかにすべきである。
そして、特に医薬の分野においては、機械等の技術分野と異なり、構成(化学式等をもって特定された化学物質)から作用・効果を予測することは困難なことが多く、対象疾患に対する有効性を明らかにするための動物実験や臨床試験を行ったり、あるいは、化学物質が有している特定の作用機序が対象疾患に対する有効性と密接に関連することを理解できる実験を行うなど、時間も費用も掛かるプロセスを経て、実施可能性を検証して、初めて用途発明として完成するのが通常である。このこととの平仄から考えても、引用発明が用途発明と認められるためには、単に、引用発明に係る物質(薬剤)が、対象とする用途に使用できる可能性があるとか、有効性を期待できるとか、予備的な試験で参考程度のデータながら有望な結果が得られているといったレベルでは足りず、当該物質(薬剤)が対象用途に有用なものであることを信頼するに足るデータによる裏付けをもって開示されているなど、当業者において、対象用途における実施可能性を理解、認識できるものでなければならないというべきである。このように解さないと、上記のようなプロセスを経て完成された実施可能性のある医薬用途発明が、実施可能性を認め難い引用発明によって、簡単に新規性、進歩性を否定されることになりかねず、その結果は不当と考えざるを得ない。
刊行物に医薬用途発明が記載されているというためには、当該医薬用途に用いることが実施可能であると当業者が理解できるように記載されている必要がある旨をいう被告の主張は、以上の趣旨をいうものとして首肯できる。」
裁判所は、このような観点から、甲3発明の薬剤につき、「進行期パーキンソン病患者においてオフ時間の持続を減少させるため」という用途における実施可能性を当業者が理解、認識できるものとして甲イ3に記載されているかどうか検討し、以下の点から、甲3発明の薬剤が、「進行期パーキンソン病患者におけるオフ時間の持続を減少させるため」に使用できる(実施可能である)と当業者が理解、認識するものであるとは認められないと判断した。
- 甲イ3の試験は「オープン試験」であり、本件明細書の「ランダム化・プラセボ対照・ダブルブラインド試験」と比べて精度が低い。
- 試験完了患者数は9名と少なく、報告も臨床/科学ノートの形式で1ページのみ。
- フルペーパー形式の論文なら記載されるはずの詳細な試験方法が明記されていない。
- 患者のバイアス(薬が効くと思い込む影響)の防止が行われたか不明。
- オン・オフ時間の測定方法などの基本情報が欠け、試験の正確性を検証できない。
- 甲イ3の結果を踏まえた追加研究(フルペーパー形式の報告)が行われていない。
- 甲イ3の著者自身も、テオフィリンの治療効果を明確に主張していない。
したがって、本件発明の「前記L-ドーパ療法におけるウェアリング・オフ現象および/またはオン・オフ変動のオフ時間を減少させるために前記患者に投与され、前記薬剤は、前記L-ドーパ療法においてL-ドーパと併用して前記対象に投与される」ものに相当するとして、甲3発明の医薬用途を肯定し、これを本件発明との一致点とした本件審決の認定には誤りがあると判断した。
裁判所は、本件発明と甲3発明の一致点及び相違点を以下のようなものとして改めて認定した。
【一致点】
アデノシンA2A受容体アンタゴニストを含有する薬剤であって、
前記薬剤は、パーキンソン病のヒト患者であって、L-ドーパ療法において、ウェアリング・オフ現象および/またはオン・オフ変動を示すに至った段階の患者を対象とし、
前記薬剤は、前記L-ドーパ療法においてL-ドーパと併用して前記対象に投与される、薬剤。
【相違点1】
本件発明は、「L-ドーパ療法におけるウェアリング・オフ現象および/またはオン・オフ変動のオフ時間を減少させるために患者に投与され」る用途発明としての「薬剤」であるのに対し、甲3発明は、そのような用途発明とは認められない点。
【相違点2】
本件発明は、アデノシンA2A受容体アンタゴニストが「(E)-8-(3,4-ジメトキシスチリル)-1,3-ジエチル-7-メチルキサンチン(KW-6002)」であるのに対し、甲3発明は、アデノシンA2A受容体アンタゴニストが「テオフィリン」である点。
(2)相違点の容易想到性について
裁判所は、相違点の容易想到性について、以下のとおり判断した。
ア 相違点1について
甲イ3の記載に基づき、より厳密な試験(ランダム化・プラセボ対照・ダブルブラインド試験)を実施し、テオフィリンの効果を検証することまでは当業者に動機付けられる。しかし、甲イ3の試験結果は、進行期パーキンソン病患者におけるウェアリング・オフ現象やオン・オフ変動に対する有効性を判断するには不十分である。また、テオフィリンは非選択的アデノシンA2A受容体アンタゴニストであり、本件優先日当時、この受容体の阻害作用がオフ時間の減少に寄与することは具体的に明らかではなく、治療上有効なアデノシンA2A受容体アンタゴニストも知られていなかった。したがって、甲イ3の記載だけでは、甲3発明の薬剤の用途を本件発明の用途へ変更する動機付けにはならない。
イ 相違点2について
テオフィリンが非選択的、KW-6002がより強力かつ選択的なアデノシンA2A受容体アンタゴニストであることは技術常識である。
甲イ3には、テオフィリンのオフ時間減少効果に関する試験結果が示され、「より強力で選択的な化合物があれば試験すべき」との記載もあることから、試験研究の範囲でKW-6002を用いることまでは当業者に動機付けられる。
しかし、これを超えて本件発明の薬剤用途に採用することまでは、技術常識や甲イ3の記載だけでは動機付けられない。
(3)顕著な作用効果について
裁判所は、顕著な作用効果について、以下のとおり判断した。
「甲イ3には、当業者においてテオフィリンを進行期パーキンソン病患者におけるオフ時間を減少させるために使用できると認識できるだけの十分な記載はなく、テオフィリンが効果を奏したとしても、アデノシンA2A受容体阻害作用によるものかも明らかでないのであって(それは、テオフィリンが非選択的アデノシンA2A受容体アンタゴニストであること、及びアデノシンA2A受容体の阻害作用が、L-ドーパ療法を受ける進行期パーキンソン病患者においてオフ時間を減少させる効果をもたらすものであるか否かも解明されていなかったことによる。)、選択的アデノシンA2A受容体アンタゴニストであるKW-6002が、進行期パーキンソン病患者において、L-ドーパ療法におけるウェアリング・オフ現象および/またはオン・オフ変動のオフ時間を減少させるという、本件明細書に示される効果は、甲イ3の記載及び本件優先日当時の技術常識から当業者が予測し得ない顕著な効果というべきである。」
3.コメント
(1)引用発明が医薬用途発明であるための要件
本件では、医薬用途発明における進歩性の判断において重要となる引用発明の認定の考え方が中心的な論点となった。
原告らは、甲3発明に基づく進歩性の判断が誤っていると主張したが、裁判所は、
「引用発明が用途発明と認められるためには、単に、引用発明に係る物質(薬剤)が、対象とする用途に使用できる可能性があるとか、有効性を期待できるとか、予備的な試験で参考程度のデータながら有望な結果が得られているといったレベルでは足りず、当該物質(薬剤)が対象用途に有用なものであることを信頼するに足るデータによる裏付けをもって開示されているなど、当業者において、対象用途における実施可能性を理解、認識できるものでなければならないというべきである。」
との規範を定立し、引用発明が医薬用途発明として認められるためには「当業者において、対象用途における実施可能性を理解、認識できるものでなければならない」という要件(以下、「実施可能性の理解・認識要件」と略す)を示したうえで、甲3発明が医薬用途発明として認められるためには、当該薬剤が対象用途に有用であることを裏付ける信頼性の高いデータが必要であると指摘した。
特許・実用新案審査ハンドブック(附属書:医薬発明)にも「当業者が当該刊行物等の記載及び出願時の技術常識に基づいて、その化合物等を医薬用途に使用できることが明らかであるように当該刊行物等に記載されていない場合にも、当該刊行物等に医薬発明が記載されているとすることはできない。」と述べられているとおり、本件判決の「当業者において対象用途における実施可能性を理解、認識できるものではければならない」という判示内容は目新しいものではない。
しかし、本判決では引用発明が医薬用途発明として認められるためのその要件を更に噛み砕いて示したところに価値がある。
裁判所は、医薬分野において構成から作用・効果を予測することが困難である特性を踏まえ、実施可能性の検証が重要であることを強調しており、裁判所の指摘によれば、以下の3点は、引用発明が医薬用途発明として認められるかどうかを評価するうえで、今後、重要な指針となるかもしれない。
- 単に「可能性がある」「有効性を期待できる」「予備的試験で有望な結果」といった程度では不十分
- 当該物質が対象用途に有用であることを「信頼するに足るデータによる裏付け」が必要
- 当業者が「対象用途における実施可能性を理解、認識できる」ものでなければならない
そして、本件における甲3発明(テオフィリンの試験)については、以下の観点からその実施可能性の理解・認識要件を満たすか否かを検討しており、今後、同様の事案に遭遇したときには、この観点が判断の参考になるかもしれない。
- 試験デザイン(オープン試験 vs. ランダム化・プラセボ対照・ダブルブラインド試験)
- 試験規模(患者数)と報告の詳細さ
- 試験方法の明記と再現性
- バイアス防止措置の有無
- 測定方法などの基本情報の提示
- 追加研究の有無
- 著者自身による効果の主張の明確さ
また、甲3発明から動機付けられる範囲が、「試験研究」の範疇なのか、薬剤の「実用化」にまで及ぶのかという間に一線を引いた判断も、引用発明の認定判断に大きく依存しており、今後の類似事案の参考になるかもしれない。
この判決は、今後の医薬用途発明の進歩性判断において、引用発明が実施可能性を満たしているかどうかの吟味がより厳格化する可能性を示すものといえるだろう。
医薬用途発明の特許性を巡って、効果等の実証的データの記載が無い引用文献であることや、医薬用途発明としての確からしさという点で引用発明との相違点が問題となった事件として、例えば、以下のものがある。
-
2007年、「タキソールを有効成分とする制癌剤」事件において、知財高裁は、臨床試験プロトコルが記載された文献により新規性を否定した。原告は、「引例は、臨床試験の途上における発表であり、有効かつ安全な投与という技術効果を挙げる程度にまで具体的、客観的なものとしては構成されていないから、発明未完成であり、引用発明とはなりえない」と主張したが、知財高裁は、「特29条1項3号においては、当該発明に対応する構成を有するかどうかのみが問題とされるべきであるところ、その有効性及び安全性は臨床試験においても当然に期待されているものであり、その記載どおりの効果が得られることを確認する試験として進行中のものであって、確立した態様としては記載されていないとしても、それだけでは、本件発明の構成要件を充足する態様が記載されていると認定することの妨げにならないというべきであるから、引用文献としての適格性を欠くものではない。」として、新規性を否定した審決の認定に誤りは無いと判断した。この判断は、本判決の引用発明の認定の考え方と異なるようにも思われる(2008.09.07ブログ記事「2007.03.01 「ブリストルマイヤーズスクイブ v. 日本ケミカルリサーチ」 知財高裁平成17年(行ケ)10818」参照)。
-
2007年、「工芸素材類を害虫より保護するための害虫防除剤」事件において、知財高裁は、引用文献に具体的な生物試験の結果が示されていなかったが適用してみようとすることは何ら困難な事柄ではないとして進歩性を否定した。被告は、用途発明の一種である医薬発明に関して、特許庁の審査基準に「当該刊行物に何ら裏付けされることなく医薬用途が単に多数列挙されている場合は、技術的に意味のある医薬用途が明らかであるように当該刊行物に記載されているとは認められず、その発明を引用発明とすることはできない。」と記載されていることから、甲2のヤマトシロアリ、イエシロアリに関する記載を引用発明とすることは不適当である旨主張したが、知財高裁は、「これら害虫に対する防除効果についての技術的意義について生物試験結果が示されていないことから即断することはできないとし、とりあえず相違点2として取り上げ、同相違点に対する判断でこれを明らかにすることとしたものであることは明らかである。」として審決の認定判断に誤りはなかったと指摘したうえで、「上記審査基準は、発明の公知性の有無に係る新規性の判断に関するものであり、進歩性の判断の当否を問題とする本件に妥当するものではないから、失当である。」と判断した。効果等の実証的データの記載が無いことから相違点として取り上げた認定判断を支持した点は、本件判決の引用発明の認定の考え方と矛盾しないように思われる。しかし、効果が生物試験によって裏付けられていないにもかかわらず「防除剤として適用してみようとする動機付け」を肯定した(主観的な観点を重視した)点は、本判決が「効果を検証することまでは当業者に動機付けられる」としながらも「有効性を判断するには不十分である」として「薬剤の用途を本件発明の用途へ変更する動機付けにはならない」と判断した(データの信頼性という客観性を重視した)論理とは違うように感じられる(2008.02.13ブログ記事「2007.07.12 「エンシステックス v. バイエルクロップサイエンス」 知財高裁平成18年(行ケ)10482」参照)。
-
2008年、「高選択的ノルエピネフリン再取込みインヒビターおよびその使用方法」事件において、知財高裁は、試験結果の記載の有無にかかわらず論文の性質及び内容を鑑みて引用例を根拠の無い単なる希望や空想ではなく「根拠のある見解」と判断し、進歩性を否定した。原告は、「引用例8には,ノルエピネフリン再取込み阻害剤が疼痛症候群に対し有用であることを示す臨床試験結果や動物試験結果等は何ら記載されておらず,この点を裏付ける理論的な説明もないから,引用例8をもってノルエピネフリン再取込み阻害剤が「慢性疼痛の治療または予防のため」に有用であることの示唆があるということはできない」と主張したが、知財高裁は、「引用例8・・・の内容は,前記のとおり,新しい抗アドレナリン性再取込み阻害抗うつ薬であるレボキセチンの臨床試験の概説に続いて,選択的抗うつ作用をよりよく理解するための発見的な理論上の枠組みを提示するというもので,多くの臨床試験の報告や論文を引用するものである。このような論文の性質及び内容に鑑みれば,引用例8に接した当業者は,著者が,根拠のない単なる希望や空想ではなく,専門家として,レボキセチンに関する多くの臨床例や論文を検討したうえで,ノルエピネフリン再取込み阻害剤が疼痛症候群に対し有用である旨の見解を記載していると考えるのが自然であり,このことは,引用例8に上記見解に至った具体的臨床試験結果や動物試験結果,論理的な説明の記載があるかどうかにより左右されるものではない。・・・また・・・抗うつ剤として用いられるノルエピネフリン再取込み剤が慢性疼痛症候群に対して有効であることは,本願の優先日当時,十分可能性のあるものとして理解されていたものというべきであるから,引用例8における上記記載は根拠を有するものというべきである。」として、原告の主張は採用することができないと判断した。効果等の実証的データの記載が無いとしても論文の性質及び内容に鑑みて根拠のある記載であると認定した点は、実施可能性を理解できるという視点で本件判決の引用発明の認定の考え方と矛盾していないように思われる(2008.09.15ブログ記事「2008.07.30 「ファルマシア・アンド・アップジョン v. 特許庁長官」 知財高裁平成19年(行ケ)10377」参照)。

-
2012年、「ピオグリタゾン」事件において、知財高裁は、引用例の図3にはピオグリタゾンとα-グルコシダーゼ阻害剤の併用による糖尿病治療薬が記載されており、当業者は相加的効果や副作用の軽減を認識できたと認められるから、本件発明の構成や作用効果も技術常識を踏まえれば記載されているに等しいと判断した(2012.09.23ブログ記事「2012.04.11 「沢井製薬 v. 武田薬品」 知財高裁平成23年(行ケ)10148」参照)。ピオグリタゾンと他剤との組み合わせに係る薬理効果の実証を伴わない記載のみからでは刊行物において本件発明が記載されているとは認められないと判断した特許庁とは異なる判断をしており、効果等の実証的データを重視するよりも技術常識を重視したように思われる。
-
2013年、「うっ血性心不全の治療へのカルバゾール化合物の利用」事件において、知財高裁は、「ある文献に医薬発明が開示されているといえるためには,当該文献に記載された薬理試験が,医薬の有効成分である化学物質が問題となっている医薬用途を有することが合理的に推論できる試験であれば足り,医薬の承認の際に求められるような無作為化された大規模臨床試験である必要はない。甲1文献記載の試験は,カルベジロールが虚血性のうっ血性心不全の治療に使用されることが合理的に推論できるものであるといえるから,甲1文献は,カルベジロールを虚血性のうっ血性心不全の治療に使用するという発明を完成した用途発明として開示したものということができ,また,甲1文献は,カルベジロールの効果を裏付ける文献としての意義を有しているものといえる。」と判断し、進歩性を否定した(2013.12.17ブログ記事「2013.10.16 「沢井製薬 v. 第一三共」 知財高裁平成24年(行ケ)10419」参照)。この判決における「合理的に推論できる試験であれば足り」と本件判決における「信頼するに足るデータによる裏付けをもって開示されているなど、当業者において、対象用途における実施可能性を理解、認識できるものでなければならないというべき」との間には若干のニュアンスの違いがあり、本件判決における判示のほうが医薬用途発明の認定にやや厳格であるように感じられる。
-
2015年、「日中活動量の低下および/又はうつ症状の改善作用を有する組成物」事件において、知財高裁は、引用例には本願用途発明として治療対象となる疾患が記載されていたが、その記載は広範な上位概念の疾患の一例として記載されているにとどまること、引用例中の実施例は当該疾患に関するものではなく、また、その実施例から当該疾患が導けるとの技術常識が存在するとの証拠が無いこと、引用例中の実施例で示された疾患に効果が確認されている医薬が当該疾患にも用いることができるとの技術常識が存在するとの証拠が無いことから、引用例に記載された発明における治療可能な疾患を当該疾患を含む上位概念疾患として広く認定することは相当ではなく、その適用は引用例記中の実施例で示された疾患の治療に限られるというべきである、と判断した(2015.09.28ブログ記事「2015.08.20 「サントリー v. 特許庁長官」 知財高裁平成26年(行ケ)10182」参照)。当業者において対象用途における実施可能性を理解、認識できるものでなければならないとした本件判決の判示にも合致する。

-
2017年、「乳癌再発の予防用ワクチン」事件において、知財高裁は、引用文献にはその臨床効果すなわち癌の再発率が低減したことまで示されていないことから、引用発明はワクチンではないと判断した。引用文献の著者は本願発明の発明者自身であり、「抗癌ワクチンとしてGP2+GM-CSFの臨床試験を実施し」、「6カ月間ワクチン接種した」と表記している。引用文献中の臨床試験は、本願発明者がワクチンとしての効果を期待して実施したことは明らかであったと思われ、そのような可能性が期待されて実施されたのだろうということは引用文献を見た当業者であれば認識できたと思われたが、臨床効果が証明されたという記載がなければ、医薬用途発明の引用発明として認定されないということを示した判断であり、本件判決と同様に引用発明の認定を厳格に評価したものといえる。「データにより裏付け・証明された」ことを求める基準に大きく揺れた判断だった(2017.04.10ブログ記事「2017.02.28 「ザ・ヘンリー・エム・ジャクソン・ファンデイション v. 特許庁長官」 知財高裁平成28年(行ケ)10107」参照)。

-
2021年、「止痒剤」事件において、知財高裁は、オピオイドκ受容体作動性化合物がボンベシン誘発グルーミング・引っ掻き行動を抑制する可能性、それら行動と「痒み」との間には関連性があることがCowanらによって提唱されていたものの、それら行動と「痒み」との間の関連性は、「技術的な裏付けの乏しい一つの仮説にすぎないもの」であるから、甲1発明の(オピオイドκ受容体作動性である)化合物Aを「止痒剤」として用いることを動機付けられると認めることはできないと判断した。「技術的な裏付けの乏しい一つの仮説にすぎない」として動機付けを否定した判断は、実証的データを重視した本件判決と矛盾しない(2021.04.03ブログ記事「2021.03.25 「沢井製薬 v. 東レ」 知財高裁令和2年(行ケ)10041」参照)。
-
2021年、「逆流性食道炎の再発抑制剤」事件において、知財高裁は、臨床試験計画(プロトコル)の記載と技術常識から進歩性を否定した。この事件では、「有効性と安全性を検討するための第Ⅲ相臨床試験に供される」点が相違点として認定されたが、データの有無よりも技術常識の存在が構成の容易想到性の判断に大きく影響したといえる(2021.08.14ブログ記事「2021.06.29 「EAファーマ v. 沢井製薬・大原薬品工業」 知財高裁令和2年(行ケ)10094」参照)。
-
2023年、本件特許に関する別件関連訴訟(令和3年(行ケ)10155・10157)において、知財高裁は、「甲A1は、パーキンソン病のウェアリング・オフ現象および/またはオン・オフ変動のオフ時間を減少させるための治療方法を見いだすために執筆された学術論文であるということはできないし、本件記載のうち「「ウェアリング・オフ」及び「オン・オフ」応答変動を有する患者において、KW-6002のような化合物は、…「オン時間」を増加させることができる可能性がある。」との部分は、これを裏付ける試験結果等に基づいてされた実証的な記載であるということはできない」と指摘し、甲A1に医薬用途発明が記載されているとの原告主張を退け、新規性及び進歩性を肯定した(2023.02.13ブログ記事「2023.01.12 「東和薬品・共和薬品工業・日医工 v. 協和キリン」 令和3年(行ケ)10155, 10157・・・パーキンソン病治療剤ノウリアストの医薬用途発明の特許性 引用文献記載は「実証的でない」と判断」(『医薬系特許的判例ブログ年報 2023』 Fubuki著 2024年5月発行, p28-52)参照)。

-
2024年、「IL-4Rアンタゴニストを投与することによるアトピー性皮膚炎を処置するための方法」事件において、知財高裁は、甲1の「治験薬」と本件訂正発明1の「医薬」との間には相違点があると認定したうえで、甲1における試験段階は第Ⅱ相試験(フェーズ2)であり、その成功率の低さ、さらには甲1に記載された情報は臨床試験のプロトコルにすぎないことからすると、甲1に記載された治験薬が試験結果を見るまでもなく当然に治療上有効であると当業者が理解するとはいえないと判断した。効果等の実証的データの記載が無いことから相違点として取り上げた点は、本件判決の引用発明の認定の考え方と同じく厳格に評価したものだったといえる(2024.10.28ブログ記事「2024.08.07 「科研製薬 v. リジェネロン/サノフィ」 知財高裁令和5年(行ケ)10019 ― 臨床試験結果に基づく医薬用途発明の特許出願のジレンマ:臨床試験プロトコル公開のインパクト ―」(『医薬系特許的判例ブログ年報 2024』 Fubuki著 2025年3月発行, p198-235)参照)。

以上のように、効果などの実証的データが記載されていない引用文献や、医薬用途発明としての確からしさが問題となった判決を時系列で振り返ると、近年では、引用文献に実証的データが無い医薬用途の構成を相違点として明確にしたうえで、もちろん技術常識の有無が認定に大きく影響するものの、それでもその引用発明が医薬用途発明として認定できるか否かを、より厳格に評価する傾向が強まっているように感じられる。そのため、医薬用途発明の新規性や進歩性を争う際には、引用発明の医薬用途発明としての実施可能性を従来以上に精査することが重要になる。こうした傾向は、知財高裁が医薬用途発明の実施可能要件をより厳格に運用しようとしていることと、平仄を合わせようとしている可能性を示唆しているのかもしれない。
(2)ノウリアスト®を巡る関連訴訟
本件特許第4376630号は、「レボドパ含有製剤で治療中のパーキンソン病におけるウェアリングオフ現象の改善」を効能・効果とするノウリアスト®錠20mgを保護するものである。
ノウリアスト®(一般名:イストラデフィリン(Istradefylline)、開発番号:KW-6002、米国製品名:Nourianz®)は、パーキンソン病治療薬として協和発酵キリン(現:協和キリン)が創製したアデノシンA2A受容体拮抗薬である。2024年度の売上収益は、日本で69億円、海外で88億円に達した(協和キリン 2024年12月期 決算短信補足資料)。
本剤の臨床開発は1996年に開始され、「レボドパ含有製剤で治療中のパーキンソン病におけるウェアリングオフ現象の改善」を効能・効果として、世界に先駆けて2013年3月25日に日本で製造販売承認を取得した(再審査期間は2021年3月24日までの8年間)。
ア 本件特許(医薬用途発明)に関連する訴訟
本件特許第4376630号に係る特許権は、ノウリアスト®の承認に基づいて存続期間延長登録がなされ、満了日は2026年8月3日となっている。したがって、本件特許が有効に存続する限り、2026年8月3日まで厚生労働省は「二課長通知」(平成21年6月5日付医政経発第0605001号/薬食審査発第0605014号)に則り、ノウリアスト®の後発医薬品を承認しないと考えられる。
しかし、東和薬品、共和薬品工業、日医工の後発医薬品メーカー3社は、2026年までの参入障壁となる本件特許を無効化すべく審判請求を提起した。
本件特許については、別件関連訴訟(無効審判請求不成立審決取消訴訟 令和3年(行ケ)10155, 10157)でも特許性が肯定されている(2023.02.13ブログ記事 「2023.01.12 「東和薬品・共和薬品工業・日医工 v. 協和キリン」 令和3年(行ケ)10155, 10157・・・パーキンソン病治療剤ノウリアスト®の医薬用途発明の特許性 引用文献記載は「実証的でない」と判断」(『医薬系特許的判例ブログ年報 2023』 Fubuki著 2024年5月発行, p28-52)参照)。

この別件関連訴訟は、知財高裁第2部で審理され、アデノシンA2A受容体アンタゴニストの医薬用途(特定患者の特定疾患)に対する効果が出願当時の技術常識では確立されていなかったと認定された。裁判所は、引用文献甲A1(Experimental Neurology Vol.162, p321-327 (2000))の考察にある以下の記載:
結論として、アデノシンA2A受容体アンタゴニストは、単独療法としてのみならず、L-ドーパ…との組合せで、パーキンソン病の有用な治療剤となる可能性がある。特に、「ウェアリング・オフ」及び「オン・オフ」応答変動を有する患者において、KW-6002のような化合物は、ジスキネジアを長引かせることなしに「オン時間」を増加させることができる可能性がある。
について、「これを裏付ける試験結果等に基づいた実証的な記載とはいえない」と判断し、本件発明が引用文献に開示又は示唆されているとは認められず、容易に想到し得たとも評価できないとした。この結果、東和薬品、共和薬品工業、日医工の主張は退けられた。
本件判決と別件関連訴訟の判決はともに、引用発明が医薬用途発明として認定されるためには、技術常識で明らかでない限り、「可能性がある」程度の記載では不十分であり、「実証的」又は「信頼に足る」データが必要であるとの立場を示している。
イ 結晶特許の無効請求不成立審決取消訴訟
ノウリアスト®の結晶発明に係る特許第4606326号(以下「結晶特許」)について、無効審判請求不成立審決取消訴訟が提起されたが知財高裁でその特許性が肯定されている(2023.07.31ブログ記事「2023.07.13 「共和薬品工業・日医工 v. 協和キリン」 知財高裁令和4年(行ケ)10064 - イストラデフィリンの結晶発明 溶解性と安定性のトレードオフ(阻害要因)により進歩性が肯定された事例 -」(『医薬系特許的判例ブログ年報 2023』 Fubuki著 2024年5月発行, p183-193参照)。
0.5~20μmの平均粒径を有し、結晶化度が40%以上である
【化1】
 で表される(E)-8-(3,4-ジメトキシスチリル)-1,3-ジエチル-7-メチル-3,7-ジヒドロ-1H-プリン-2,6-ジオンの微細結晶。
で表される(E)-8-(3,4-ジメトキシスチリル)-1,3-ジエチル-7-メチル-3,7-ジヒドロ-1H-プリン-2,6-ジオンの微細結晶。ノウリアスト®の承認に基づいて結晶特許に係る特許権は存続期間が延長されており、その満了日は2026年10月16日となっている。
ウ その他の特許
ノウリアスト®を保護する固形製剤に関する特許権(特許第4673745号; 存続期間延長により2026年9月9日満了)やジアリールビニレン化合物の安定化方法に関する特許権(特許第4413866号; 存続期間延長により2028年1月23日満了)も存在するが、現時点で、これら特許に対して無効審判は請求されていない。
ノウリアスト®の後発医薬品の承認を狙うメーカーは、これら特許に係る特許請求の範囲を回避した後発医薬品を開発しているのかもしれない。
以上のノウリアスト®を保護する特許に関連する訴訟状況を踏まえると、後発医薬品は、早くとも、本件特許(第4376630号)の存続期間が満了する2026年8月3日以降、又は、結晶特許(第4606326号)の存続期間が満了する2026年12月以降に厚生労働省の製造販売承認を受け、販売が開始されると想定される。
アシスタントたち:
Robot icons created by Freepik – Flaticon; Robot cat icons created by Freepik – Flaticon





コメント