 2024年3月25日、エーザイは、経口チロシンキナーゼ阻害剤「レンビマ®」(Lenvima®)(一般名:レンバチニブメシル酸塩(Lenvatinib mesilate))に関する特許(米国特許第10,407,393号及び第11,186,547号、以下、本特許)の侵害を理由として、本剤に関する後発医薬品の簡略新薬承認申請(Abbreviated New Drug Application:ANDA)を行った後発医薬品メーカーであるSUN Pharma及びShilpaに対し、2019年11月以降、米国ニュージャージー州連邦地方裁判所に特許侵害訴訟を提起していましたが、2024年3月21日に、SUN Pharmaと和解契約(以下、本和解)を締結したと発表しました(2024.03.25 エーザイ press release: 米国におけるレンバチニブに関する特許侵害訴訟の和解について)。
2024年3月25日、エーザイは、経口チロシンキナーゼ阻害剤「レンビマ®」(Lenvima®)(一般名:レンバチニブメシル酸塩(Lenvatinib mesilate))に関する特許(米国特許第10,407,393号及び第11,186,547号、以下、本特許)の侵害を理由として、本剤に関する後発医薬品の簡略新薬承認申請(Abbreviated New Drug Application:ANDA)を行った後発医薬品メーカーであるSUN Pharma及びShilpaに対し、2019年11月以降、米国ニュージャージー州連邦地方裁判所に特許侵害訴訟を提起していましたが、2024年3月21日に、SUN Pharmaと和解契約(以下、本和解)を締結したと発表しました(2024.03.25 エーザイ press release: 米国におけるレンバチニブに関する特許侵害訴訟の和解について)。
Shilpaとの間では訴訟が係属中で、本和解における和解条件については現状非開示、本件による2024年3月期の連結業績予想への影響はないとのことです。
米国におけるLenvima®は、Differentiated Thyroid Cancer (DTC)、Renal Cell Carcinoma (RCC)、Hepatocellular Carcinoma (HCC)、Endometrial Carcinoma (EC)を適応としており、その売上収益は、2023年3月期の実績が1,605億円(1,185百万米ドル)、2024年3月期の予想は1,970億円(1,365百万米ドル)です。

それでは、Lenvima®を保護する米国特許の内容を見てみましょう。
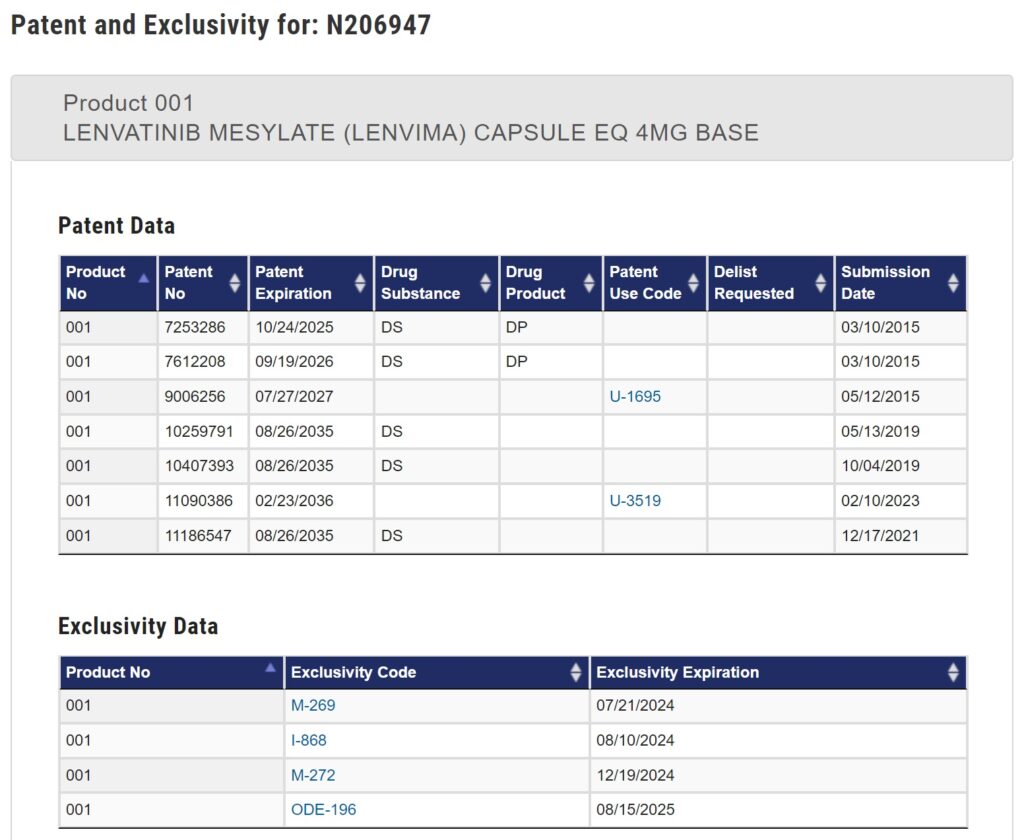
Lenvima®(4mg Capsule)のOrange Bookには、7件の特許が収載されています。
7件の特許の概要は以下のとおりです。
- ①7,253,286: 物質(特許延長)。
- ②7,612,208: 結晶
- ③9,006,256: 治療方法(U-1695 Method for treating thyroid carcinoma including differentiated thyroid cancer)
- ④10,259,791: 高純度のレンバチニブメシル酸塩
- ⑤10,407,393: 高純度のレンバチニブメシル酸塩
- ⑥11,090,386: 苦みを抑制するため塩基性物質との懸濁液にして投与する方法(U-3519 Treatment with Lenvima by administering Lenvima as a suspension)
- ⑦11,186,547: 高純度のレンバチニブメシル酸塩
これら特許が存在することにより、後発医薬品メーカーは、これら特許の侵害とならないよう又は特許は無効であることを主張してANDAを行う必要があります。
まず、物質特許①を無効にするか存続期間が満了する2025年10月24日までは、後発医薬品は承認されません。
後発医薬品メーカーが結晶特許②を回避することができず無効にすることもできないとなれば、同特許の存続期間が満了する2026年9月19日までは、後発医薬品は承認されないことになります。
同様に、後発医薬品メーカーが高純度のレンバチニブメシル酸塩に関する特許④⑤⑦を回避することができず無効にすることもできないとすれば、同特許の存続期間が満了する2035年8月26日までは、後発医薬品は承認されないことになります。
苦みを抑制するため塩基性物質との懸濁液にして投与する方法特許⑥については、確かにLenvima®のprescribing informationにはsuspensionを調製して投与する方法が記載されていますが、「苦みを抑制するため塩基性物質と」懸濁させる点は記載されていません。後発医薬品がこの特許の侵害を構成することになるのかどうかは議論がありそうです。
治療方法特許③が存在しますが、Differentiated Thyroid Cancer (DTC)を適応から外し、Renal Cell Carcinoma (RCC)、Hepatocellular Carcinoma (HCC)、Endometrial Carcinoma (EC)を適応とするのであれば、上述した特許の問題を解決できている限り、後発医薬品は承認されるかもしれません。
以上、各特許の内容を概観すると、後発医薬品メーカーとの特許攻防は、結晶特許②及び高純度のレンバチニブメシル酸塩に関する特許④⑤⑦を回避することができるかどうか、または無効にすることができるかどうか、が中心になると想像できます。
今回のプレスリリースで伝えられた訴訟対象であったとされる本件特許(米国特許第10,407,393号及び第11,186,547号)は、高純度のレンバチニブメシル酸塩に関する特許⑤⑦であり、物質特許①及び結晶特許②は含まれていなかったこと、そして和解に至ったことからすると、エーザイとSUN Pharmaは、結晶特許②の存続期間が満了する2026年9月19日以降であって、高純度のレンバチニブメシル酸塩に関する特許⑤⑦の存続期間が満了する2035年8月26日よりも前のどこかのタイミングで後発医薬品の販売を許す合意に至ったのではないかと想像されます。
しかし、そのタイミングに関する条件について開示してしまえば、訴訟が現在も係属中であるShilpaとの交渉に影響が生じるため、現状は非開示とせざるをえなかったという事情はあると思われます。

レンビマ®(Lenvima®)はエーザイの主力品。今後期待されるレケンビ®が成長するまでは後発医薬品の市場参入は阻止したいところです。



コメント