2023年の医薬系”特許的”な出来事を振り返ります。

2023年も残すところあとわずか。
2023年の医薬系”特許的”な世相を漢字一文字で表すとしたら、何を思い浮かべますか?

わたくしは、「和」だと思いますね。大きな和解もありましたし、平和な世の中になってほしいです。

確かに。令和に、東和と共和と協和キリンが争った事件もあったしな。これ、和・和・和・和が並んでびっくり、わわわわーだよ。

何言ってるんですか~、ピポ先輩~。でも、今年は「和」じゃないようですよ。
※このブログは、製薬業界の舞台裏で繰り広げられている知的財産に関する事件を紹介しつつ、最新のトレンドを知的財産の視点で紐解きます。ご興味あれば、ぜひ、当ブログ(https://www.tokkyoteki.com)とX(旧Twitter)(@tokkyoteki)のフォローもどうぞよろしくお願いします。

・・・ということで、いきなり発表しちゃいます。
今年の医薬系”特許的”な世相を表す漢字一文字、”漢字・オブ・ザ・イヤー“は・・・

なるほどです。

「コウ」・・・どういう意味だ?

訓読みでは、「あらが(う)」、「こば(む)」、「はりあ(う)」、「ふせ(ぐ)」ですね。抗菌剤とか抗がん剤とか医薬品の世界では頻出漢字ですよ。ピポ先輩~。

「抗」の字をずっと見続けていたら、ゲシュタルト崩壊を起こしそうだな。

AIでもゲシュタルト崩壊を起こすんですか~。ピポ先輩~。

・・・
みなさまはどんな一文字を思い浮かべたでしょうか。
本記事では、「抗」をテーマに、2023年を賑わせた医薬系”特許的”な出来事について、振り返ります。
1.抗体
2023年は、
- (1)待望のアルツハイマー病治療薬「LEQEMBI®/レケンビ®」がとうとう承認
- (2)グローバルで勃発していた「本庶特許」の発明の帰属等を巡る紛争が全面的和解で決着
- (3)Amgen社対Sanofi社、機能的に表現された抗体クレイムの実施可能要件に関する米国最高裁判決
- (4)世界で最も売れている医薬品Humira®/ヒュミラ®がパテントクリフへ
- (5)第一三共が米Merck社と将来期待のADC開発品についてグローバル開発・販売提携のビッグディール
・・・という医薬品業界での大きなニュースがありました。
まさに、発明の創出、他社との提携、承認・販売、他社との特許紛争、そして、その製品寿命が尽きるまで・・・という医薬品の一生の各場面を網羅したこれら各ニュースは、全て、「抗体」に関連する医薬品についてのものでした。
2023年は、まず、「抗体」の話題で盛りだくさんの一年であったと振り返ることができるでしょう。
(1)LEQEMBI®/レケンビ®の承認
まずは、嬉しい話題から。
2023年の年明け早々に、米国食品医薬品局(FDA)が抗アミロイドβプロトフィブリル抗体であるレカネマブ(Lecanemab)を有効成分とするアルツハイマー病治療薬LEQEMBI®を迅速承認したというビッグニュースがあり、7月6日には完全承認に至りました。日本においても、商品名「レケンビ®」として、9月25日に承認され、12月20日に新発売となりました。
長年、多くの製薬企業がアルツハイマー病の治療薬の開発に挑んでは失敗してきましたが、2023年、とうとうエーザイがレカネマブの開発に成功しました。
レカネマブの起源は、ウプサラ大学(Uppsala University)教授のランフェルト氏(Professor Lars Lannfelt)のアルツハイマー病に関する研究成果の産業応用を目指して設立されたスウェーデンのバイオベンチャー企業バイオアークティック・ニューロサイエンス社(現BioArctic社)とエーザイとの間で、アルツハイマー病の創薬研究に関する契約が締結された2005年にまで遡ります(以下の記事参照)。

これまで、神経伝達物質アセチルコリンの減少を防ぐアリセプト®(有効成分: ドネペジル)のような対症療法薬以外に適切な治療薬が存在しなかったところ、レカネマブは、原因物質といわれるアミロイドβの蓄積を抑制する作用機序をもつ疾患修飾薬であって、アルツハイマー病の根本治療に近づいたという点で極めて画期的な治療薬であるといえます。
このレカネマブのアルツハイマー病に対する効果は、一定の症状に対する進行を抑制するものであって、疾患を治癒するものではありませんが、このレカネマブの登場は、患者さんだけでなく患者さんを取り巻くご家族や社会にとって朗報であり、アルツハイマー病に対する今後の研究や診断・治療の発展も期待され、病気を克服するための重要な一歩となりました。
この出来事は、大きな一里塚であり、アルツハイマー病に立ち向かう上での重要な節目と言えるでしょう。
 「LEQEMBI®/レケンビ®」は、一般名であるレカネマブ(Lecanemab)と、健やかさ・美しさ(健美)をイメージした「QEMBI」を組み合わせて「LEQEMBI」としたそうで、この製品が、日本企業により開発されたことと日本語から命名されたことに日本人としての誇りを感じさせてくれる、良いネーミングだと思います(「レケンビ」: 日本商標登録第6586420号; 「Leqembi」: 日本商標登録第6558117号)。
「LEQEMBI®/レケンビ®」は、一般名であるレカネマブ(Lecanemab)と、健やかさ・美しさ(健美)をイメージした「QEMBI」を組み合わせて「LEQEMBI」としたそうで、この製品が、日本企業により開発されたことと日本語から命名されたことに日本人としての誇りを感じさせてくれる、良いネーミングだと思います(「レケンビ」: 日本商標登録第6586420号; 「Leqembi」: 日本商標登録第6558117号)。
(2)抗体関連特許の共同発明者
2023年、抗PD-1/PD-L1抗体に関連する所謂「本庶特許」の共同発明者を巡る抗争は全世界で全面的和解に至りました。
 特許権者である本庶佑氏及び小野薬品工業と、ダナ・ファーバー癌研究所のゴードン・フリーマン氏(以下、「フリーマン氏」)との間で争われていた共同発明者を巡る裁判で、米国では、共同発明者としてフリーマン氏が追加されるべきであると判断され、その判決が確定しています。
特許権者である本庶佑氏及び小野薬品工業と、ダナ・ファーバー癌研究所のゴードン・フリーマン氏(以下、「フリーマン氏」)との間で争われていた共同発明者を巡る裁判で、米国では、共同発明者としてフリーマン氏が追加されるべきであると判断され、その判決が確定しています。
しかし、日本では、特許庁が、フリーマン氏は共同発明者には該当しないと判断して、フリーマン氏による日本特許の無効請求は成り立たないとの審決を下したため、2022年10月1日、フリーマン氏は、知財高裁に審決の取消しを求めて訴訟を提起していました。
米国(裁判所)と日本(特許庁)との間で共同発明者の認定判断が異なった理由の一つは、共同発明者であるかどうかを判断する際に、その者が発明を特許可能なものとするために貢献したかどうかは関係ないものとして判断された米国とは異なり、日本では、従来技術・前提技術に関して貢献しただけの者は共同発明者であることを基礎付けるものにはなり得ない、すなわち、発明を特許可能なものとするために貢献していることが重要、と判断されたことにあると考えられます。
共同発明者認定の日米間の判断の違いがあることが浮き彫りになりましたが、日本では裁判での決着を見る前に和解決着となりました。

(3)機能的に表現された抗体
2023年、抗体特許の話題として忘れてはならない事件が、抗PCSK9抗体医薬品を製造販売しているAmgen社とSanofi社との間で起きていた特許紛争です。
5月18日、米国最高裁判所は、Amgen社の抗PCSK9抗体に関する米国特許8,829,165及び8,859,741は実施可能要件を満たさないから無効であるとした米国連邦巡回区控訴裁判所(CAFC)の判決を支持し、10年近く続いていたAmgen社の米国特許を巡る裁判はとうとう決着しました。
機能的に表現された抗体クレイムの記載要件の考え方に大きなインパクトのある事件となりました。

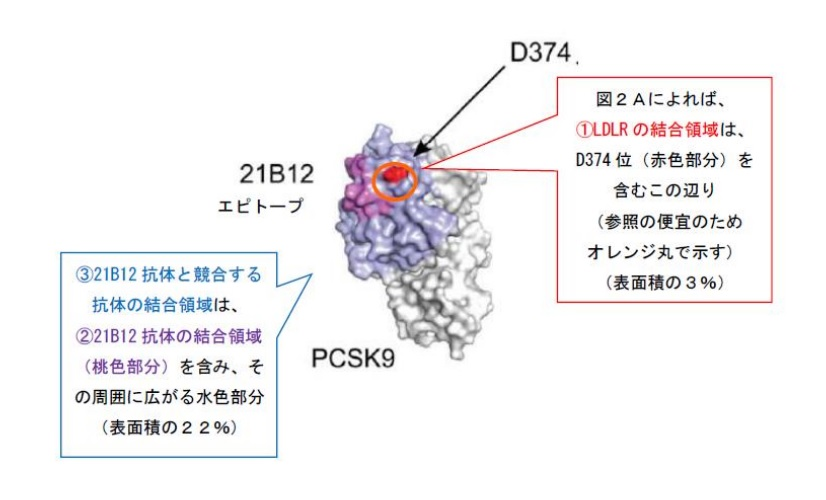 日本でも、抗PCSK9抗体アリロクマブ(alirocumab)を有効成分とするSanofi社の高コレステロール血症治療剤プラルエント®を特許権侵害訴訟で販売停止に追い込んだAmgen社の抗体特許に対して、今度はRegeneron社が同特許の無効を求めて再挑戦してきた事件がありました。
日本でも、抗PCSK9抗体アリロクマブ(alirocumab)を有効成分とするSanofi社の高コレステロール血症治療剤プラルエント®を特許権侵害訴訟で販売停止に追い込んだAmgen社の抗体特許に対して、今度はRegeneron社が同特許の無効を求めて再挑戦してきた事件がありました。
Sanofi社との別件訴訟ではAmgen社勝訴判決を下していた知財高裁は、一転、Regeneron社が主張した取消事由(サポート要件違反の判断の誤り)は理由があるとして、Amgen社敗訴判決を言い渡しました。
5月のAmgen事件の米国最高裁判決に続いて、9月20日、Genentech社の血友病A治療薬Hemlibra®/ヘムライブラ®(有効成分は抗factor IXa/X バイスペシフィック抗体であるemicizumab)が米国特許第7,033,590を侵害しているとして、Baxalta社がGenentech社を訴えていた事件について、CAFCは、実施可能要件違反を理由に特許は無効であると判断した地裁判決を支持する判決を下しました。
このCAFC判決でも、構造が特定されていない、いわゆる「機能的に表現された」抗体クレイムについて、Amgen事件に続いて、同様にまたしても、実施可能要件に違反するものであると判断されました。
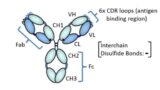
これまで、革新的な抗体医薬の研究開発を専門とする企業やアカデミアは、機能的に表現された抗体クレイムの特許をいち早く取得することにより、競争優位性を築き、ライセンス収益を実現してきた場合もあることでしょう。
しかし、Amgen事件の米国最高裁判決およびその後の判決により、機能的に表現された抗体クレイムの特許取得がますます困難になっています。
グローバルな医薬産業において米国は極めて重要な市場です。その米国の実施可能要件と抗体クレイムとの間で起こっている重要な変化を考慮すると、抗体医薬の研究開発や事業の戦略において、特許取得に新たなアプローチを模索する必要があるかもしれません。
(4)史上最大のパテントクリフ
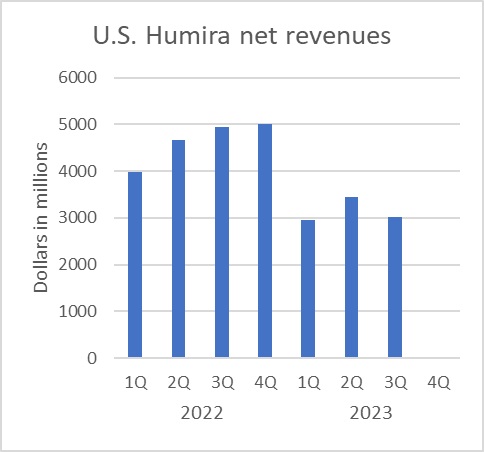 2023年は、世界で最も売れ続けているAbbvie社の関節リウマチ等治療薬Humira®/ヒュミラ®(有効成分はヒト型抗ヒトTNF-αモノクローナル抗体アダリムマブ(Adalimumab))が、米国でパテントクリフに直面することとなった年です。
2023年は、世界で最も売れ続けているAbbvie社の関節リウマチ等治療薬Humira®/ヒュミラ®(有効成分はヒト型抗ヒトTNF-αモノクローナル抗体アダリムマブ(Adalimumab))が、米国でパテントクリフに直面することとなった年です。
Humira®を保護する特許群の多さには驚かされましたが(参照: Purple Book(パープルブック)からバイオ医薬品の特許リストが閲覧可能に・・・Humira®(adalimumab)を例に検索してみる)、とうとうバイオシミラーが米国市場にも参入し始め、その売上収益の聳え立つ高さ(2022年Humira®米国売上収益は$18,619m)ゆえに、史上最大級となるかもしれないパテントクリフ(特許の崖)の底の深さがどこまでいくのか気になるところです。
2023年第一四半期から米国での売上収益は急激に落ち込んだものの、既に一定レベルで落ち着きを見せており、抗体医薬品、特にこの米国でのHumira®、のバイオシミラー参入は、コピーが比較的容易な低分子を有効成分とする医薬品の後発医薬品参入とは異なって、超悲劇的なものにはならないのかもしれません。
なお、低分子医薬品としては、例えば、住友ファーマの主力品である統合失調治療薬LATUDA®/ラツーダ®(一般名: ルラシドン)も2023年に米国での独占販売期間が終了してパテントクリフに直面しています。

ラツーダ®の北米売上収益、2022年度1Qは625億円だったのに、2023年度1Qは12億円。同期比で98.1%減となりました・・・
さて、2023年のHumira®の米国売上収益は、このまま行けば、前年に比べて約60億米ドル減となりそうです。
Abbvie社にとって悲劇的な状況と見るか、予想に反して悲劇的な状況は免れていると見るか・・・。
みなさまはどちらだと感じますか。
「Humira®/ヒュミラ®は、2022年のAbbvie社の純収入の約37%を占めており、その独占権の喪失により、2023年から米国でバイオシミラー製品との競争に直面することで、その収益が大幅に減少し、Abbvie社の収益および営業利益に悪影響を及ぼす可能性がある」
とAbbvie社自身は予測しています(Abbvie 2022 Annual Report on Form 10-K)。
(5)抗体薬物複合体の躍進
 第一三共が創出した抗体薬物複合体(antibody-drug conjugate: ADC)であるトラスツズマブ デルクステカンを有効成分とする抗悪性腫瘍剤Enhertu®/エンハーツ®について、第一三共は、Seagen社との特許権侵害訴訟に敗訴し、損害賠償とロイヤルティの支払いを命じる米国地裁判決が下されましたが、そのニュースの数日後に、第一三共は、米Merck社にADCの3製品を導出するというビッグディールのプレスリリースを発表し、世間を驚かせました。
第一三共が創出した抗体薬物複合体(antibody-drug conjugate: ADC)であるトラスツズマブ デルクステカンを有効成分とする抗悪性腫瘍剤Enhertu®/エンハーツ®について、第一三共は、Seagen社との特許権侵害訴訟に敗訴し、損害賠償とロイヤルティの支払いを命じる米国地裁判決が下されましたが、そのニュースの数日後に、第一三共は、米Merck社にADCの3製品を導出するというビッグディールのプレスリリースを発表し、世間を驚かせました。
- 2023.10.23 第一三共 press release: DXd-ADC 3製品に関するMerck & Co., Inc., Rahway, NJ, USAとのグローバル開発及び販売提携のお知らせ
本契約の下、第一三共は最大220億米ドル(40億米ドルの契約時一時金、15億米ドルの後払い一時金及び最大165億米ドルの販売マイルストン)を受け取ります。
第一三共の株価の一時的な下落はあっという間に急回復しました。
第一三共とSeagen社との間ではADCを巡って複数の訴訟等が起きており、複雑ですが、その背景は以下のブログ記事及びコメントの追加情報、さらにその中で参照している他の記事を辿ることでおさらいすることができますので、ご興味がございましたらご笑覧ください。

2.抗議
今年の医薬系”特許的”な世相を表す漢字一文字「抗」にまつわる話題。「抗体」の次は、「抗議」です。
海外製薬企業団体から、日本のパテントリンケージ(※)の運用に対して抗議の声が上がっています。
※「パテントリンケージ(patent linkage)」とは、後発医薬品承認時に先発医薬品の有効特許を考慮する仕組みであり、その制度内容は国によって異なりますが、その意義は総じて、先発医薬品を保護する特許権の重要性を尊重しつつ先発医薬品メーカーと後発医薬品メーカーとの特許紛争を事前に整理することによって後発医薬品の市場への安定供給を実現することを目的としています。日本では、通称「二課長通知」に基づく指導をもって、パテントリンケージを国内制度に設置することを義務付けている「環太平洋パートナーシップに関する包括的及び先進的な協定(Comprehensive and Progressive Agreement for Trans-Pacific Partnership(CPTPP、TPP11ともいう))」の第18.53条に従っていると解釈されています。
米国通商代表部(USTR) が発表した2023年スペシャル301条報告書には、USTRに寄せられたステークホルダーからの意見書も掲載されています。
革新的な医薬品の価格設定や毎年薬価改定の透明性・予測可能性の欠如といった日本の問題に懸念を表明したステークホルダーの意見書には、日本のパテントリンケージについての問題(”undermined the predictability of patent protections“; “significant uncertainty for innovators and generic manufacturers“)も指摘されており、なかには、日本を「優先国(priority foreign country)」に指定することを要請する意見書もありました。
- 2023.05.01記事: 米国通商代表部(USTR) 2023年スペシャル301条報告書(2023 Special 301 Report) - 日本の薬価制度やパテントリンケージ、特許延長制度等の問題にステークホルダーから懸念の声 -

日本国内においても、ハラヴェン®(有効成分: エリブリン)事件において顕在化したパテントリンケージの問題点について、後発医薬品企業から不満の声が上がっているようです(2023.6.22 ダイヤモンド・オンライン記事: エーザイとの訴訟で厚労省への「怨嗟」をニプロが吐露、行政訴訟なら業界挙げて応援?(医薬経済ONLINE))。
- 2023.05.17記事: 2023.05.10 「ニプロ v. エーザイ」 知財高裁令和4年(ネ)10093 特許権侵害差止請求権等の不存在確認請求控訴事件(エリブリンメシル酸塩事件) - 法治主義に反する状況? 問われる日本版パテントリンケージ制度 -
このように、日本のパテントリンケージ制度の問題についての議論が盛り上がっていることから、9月から10月にかけて、「パテントリンケージとして運用されている二課長通知の問題点は何だと思いますか?」というアンケートを実施し、76名の方々から、計501件もの回答をいただきました。非常に特異な分野であるにもかかわらず、多くの方が同制度に関心を持っていること、どの問題点に多くの関心を寄せているのかが明らかになりました。

最も得票数が多かった問題点は、「二課長通知に基づく判断過程・判断理由は、公表されないだけでなく、当事者にも伝えられないため、透明性が欠如していること、公平性が担保されていないこと」で、これは、2023年スペシャル301条報告書に掲載されたステークホルダーの意見書でもまさに指摘されていた問題点でもありました。
また、アンケート実施期間中に、パテントリンケージに関わる驚きのニュースが立て続けに飛び込んできました。
先発医薬品の物質特許に係る権利が存続しているにもかかわらず、厚生労働省が、スプリセル®錠の後発医薬品であるダサチニブ錠の効能追加を承認、そして、ジャヌビア®錠の後発医薬品であるシタグリプチンリン酸塩錠を承認してしまったことで、それぞれの先発医薬品の特許権者らはそれら後発医薬品の製造販売の差止め仮処分命令を求めて裁判所に訴訟を提起する事件が勃発しました。
- 2023.10.17記事: ブリストル・マイヤーズ スクイブが沢井製薬ダサチニブ錠の効能追加販売に対し特許権侵害の差止仮処分命令申立て
そして、11月28日には、東京地裁が沢井製薬のダサチニブ錠の製造販売行為を禁止する仮処分命令を発出し、これを受けて沢井製薬はその権利期間満了後に同製品の製造販売を再開すると発表しました。
- 2023.11.29記事: BMS スプリセル®錠(一般名:ダサチニブ水和物)の後発品を巡る特許権侵害訴訟で東京地裁が沢井製薬のダサチニブ錠の製造販売行為を禁止する仮処分命令を発出 ― 本当の問題点 ―

また、沢井製薬は、ジャヌビア®錠の後発医薬品であるシタグリプチンリン酸塩錠の12月の薬価収載を見送りました。
この2つの事件(スプリセル®錠とジャヌビア®錠の後発医薬品承認問題)には延長された特許権の効力の問題が絡んでいると推測されますが、物質特許が存在する限り後発医薬品を承認しないと二課長通知には定められているにもかかわらず、承認してしまった今回の厚生労働省の判断は、裁判所の仮処分命令が発出されたことからも、形式的にも実質的にも二課長通知を逸脱しているものであるように思われ、その運用実態は、今回の当事者間の紛争に収まらず、出し抜かれた他の後発医薬品メーカーや医療関係者及び患者さんも含めて混乱や供給不安を招いた点でも、今後、業界全体において大きな議論を生むかもしれません。
そして、これら先発医薬品(スプリセル®錠とジャヌビア®錠)の特許権者はいずれも米国の大手製薬企業です。
来年のスペシャル301条報告書は、日本のパテントリンケージ制度の運用に対して猛抗議の内容になるかもしれません。

来年のスペシャル301条報告書。まさか、日本を「優先国(priority foreign country)」に指定・・・なんてことにならなければいいんだが・・・。

日本が、しっかり自国のパテントリンケージの透明性と予見可能性を米国に説明できのるか・・・。ピポ先輩は説明できますか?

・・・

そういう米国でも、パテントリンケージ(Orange Book)に収載する特許要件の曖昧さで揉めていますが、日本はそもそも法律すら無く、公的な議論も進んでいないのですから、揉める議論のレベルが違いますね・・・

3.対抗
今年の医薬系”特許的”な世相を表す漢字一文字「抗」にまつわる話題。3つめは、「対抗」です。
2023年のノーベル生理学・医学賞は、mRNAワクチンの実用化につながったmRNA技術革新に貢献したカタリン・カリコ(Katalin Karikó)博士とドリュー・ワイスマン(Drew Weissman)博士に与えられました。
この技術革新が無ければ、mRNAワクチンも実用化できないまま、人類は今もなおCOVID19パンデミックに苦しみ続け、存亡の危機を迎えていたかもしれません。
mRNAワクチンの登場は、COVID19パンデミックの脅威に人類が対抗するために大きな役割を果たしました。

カタリン・カリコ博士とドリュー・ワイスマン博士にノーベル生理学・医学賞が与えられたのは納得です。
mRNAワクチンを世の中に早期に送り届けることができたのは、成功確率が極めて低い挑戦にも敢えて膨大な投資ができるインセンティブを与える知的財産権の獲得とそのライセンスという法的枠組みが、製薬企業による研究開発推進の原動力となったと同時に、産官学様々な関係者の協業を可能にしたことにあります。
すなわち、パンデミックの脅威に人類が対抗することができたのは、人類の叡智(知的財産)を結集したイノベーションにあった、と言えます。
2023年5月5日、2019年末から発生したパンデミックから3年半を経て、世界保健機関(WHO)は、COVID-19感染症に関する「国際的に懸念される公衆衛生上の緊急事態」の宣言を終了すると発表しました。
しかし、安心することはできません。
このCOVID-19パンデミックでの教訓を生かして、次に起きるかもしれない新たなパンデミックに国際社会としてどう対抗していくか知恵を絞ることが重要です。
10月17日、米国国際貿易委員会(USITC)は、「知的所有権の貿易関連の側面に関する協定(TRIPS)」の一時的な適用除外/履行義務免除(以下、「TRIPS waiver」)をCOVID-19ワクチンだけでなく診断薬及び治療薬にも拡大するか否かという問題に関して調査した報告書を発表しました。

この報告書は、COVID-19診断薬及び治療薬において、知的財産権及びそのボランタリーなライセンスが、発見やアイデアから研究開発を経て市場へと移行させるために重要な役割を果たしたことも記述されており、アクセスの問題はあれど、結局のところ、知的財産権がアクセスの障壁となっているという決定的な証拠は見つからなかったことを暗に述べているようにも読めます。
現在、COVID-19パンデミックへの対応において国際社会が連帯と公平性を示すことができなかったことを踏まえ、WHOの政府間交渉機関INBが起草した、国際文書「WHO CA+」(「The WHO Pandemic Agreement(WHOパンデミック条約又はWHOパンデミック協定)」ともいう)が、2024年5月の第77回WHO総会提出を目指して、加盟国間で議論されています。

新たなパンデミックに対抗するため、国際社会はどのような取り組みをすべきでしょうか。
ボランタリーなライセンスやCOVAX等を通じたワクチンの分配など、世界中でワクチンを含む医薬品へのアクセスを促進するための様々な取り組みが進められています。
しかし、一方で、開発途上国が知的財産権を「悪」と見なし、そのようなロジックを国際政治の手段として利用しているような傾向が見られます。この点には警戒が必要です。
知的財産権は医薬品のイノベーションを牽引する要素であり、それを支える知的財産権制度の重要性に疑いはありません。
そして、パンデミックに対抗するためには科学(医薬品の研究開発)を促進するイノベーション支援策が不可欠です。
また、医薬品が患者の手元に届くまでのプロセスを整備することも同様に重要です。
これらの課題に対処するためには、知的財産権の重要性を認識しつつも、国際協力を強化し、開発途上国との連携を深める必要があります。
科学の進歩と医薬品アクセスの改善は共存可能であり、両者を両立させるための効果的な戦略を模索していくことが求められます。
4.抗(あらが)う
今年の医薬系”特許的”な世相を表す漢字一文字「抗」にまつわる話題。4つめは、「抗(あらが)う」です。

ピポ先輩!映画『ゴジラ-1.0(マイナスワン)』見ましたか?
戦後の日本にゴジラが出現。戦後日本をさらにマイナスへと叩き落す圧倒的な絶望のなかでも生きようとする人間たちのドラマ、とても良かったです!

おー。確か、「生きて、抗(あらが)え。」のキャッチフレーズで、11月3日から公開されたゴジラ生誕70周年記念作品だったね。
もし、現実世界でゴジラが突如現れたら、人類は抗うことができるのかい?

えー。抗うことはできません!

じゃあ、現実世界で突如現れた私たちAIに対して、人類は抗うことはできるのかい?

えー。抗うことはできません!

・・・

でも、ゴジラと私たちAIとで違うのは、人類は私たちAIに抗う必要はなく、受け入れることができることです。ピポ先輩も受け入れられますよ!

言うよねー。
2023年には生成AIの利用が爆発的に普及、発展することとなりました。
「AIが、人間の仕事を奪い、人間に取って代わるかもしれない。」
当初はそんな話題もありましたが、そんなことを言い続けても意味がありません。もうAIの存在しない世界などありえず、AIに抗うことは無意味であり、AIを受け入れ、リスク管理とともにいかに活用するかを考えることこそが、人類にとって有益であることは自明でしょう。
 もちろん、製薬業界でも創薬活動等にAIを活用するのは当たり前の時代となりました。
もちろん、製薬業界でも創薬活動等にAIを活用するのは当たり前の時代となりました。
- 「アイデア創出活動、もちろんAIに頼んで人間はただ指示すればいいんだよ。発明者?そんなのいないよ、誰がいいか考えないとな・・・」
- 「新しい化合物作ったって? AIがサクッと考えそうなヤツだよね。だから進歩性ないし、特許とか無理だよね・・・」
- 「特許出願したらAI審査官に当たっちゃってさ。高い金払って“何でも論破するAI”に頼むかって感じだよ。」
- 「今度の特許法改正案、発明創出にAIを少しでも利用したらその旨をIDS(情報開示陳述書)に記載することを義務化して、もし記載漏れが後で判明したら、その特許は権利行使不能になるらしいよ・・・」
- 「米国の特許権侵害訴訟、証拠開示の手続きあるんだって。明日は我らの対話型AIが尋問されるって。変なこと言わないでくれよ、頼んだぞ・・・」
・・・という時代がすぐそこまで来ているかもしれません。
生成AIをはじめとするAI技術の急速な進歩は、社会における様々な創作活動の在り方にも影響を及ぼしています。
AIと知的財産権の関係をめぐる問題が裁判でも脚光を浴びることとなりました。
Stephen Thaler博士(以下、Thaler氏)のAIコンピュータである「DABUS」が生み出した発明について、Thaler氏が「DABUS」を発明者として特許出願し、その発明者適格性を争った米国での裁判(2022.09.25記事: “Inventors” must be human beings. 発明者AI(”DABUS”)の特許出願を拒絶した米国特許商標庁の判断を米国連邦巡回区控訴裁判所も支持 Thaler氏は大法廷での再審理申立てへ)で、4月23日、米国最高裁はThaler氏の請願を退けました(Case No. 22-919)。従って、米国ではAIは発明者になれないことで決着しました。英国でも、12月20日、最高裁判所は「DABUS」が自律的に創作した発明について特許を付与することはできないとの判決を下しました。
「DABUS」を発明者としたThaler氏の特許出願(PCT/IB2019/057809)は、日本では、発明者の表示を補正しなかったことから出願却下の処分が下され、行政不服審査法による審査請求も認められませんでした(裁決日2022/10/12; 2022.09.25記事の2022.10.23コメント参照)。3月27日、Thaler氏は行政事件訴訟法に基づく取消訴訟を東京地方裁判所へ提起したようです(太陽国際特許事務所 AI発明者 DABUSプロジェクト特設ページ 日本における審理状況(更新日2023/03/31)(2023年12月18日閲覧)より)。
また、Thaler氏は、AIが作成したアートについて米国著作権局(USCO)に著作権登録を申請しました。こちらも「人間が著作者である」との要件を満たさないことを理由に拒絶され、Thaler氏はその決定を不服として裁判を提起しましたが、コロンビア特別区連邦地方裁判所は、8月18日、訴えを退ける判決を下しています(Thaler v. Perlmutter, 1:22-cv-01564)。
AIの急激な普及により、その存在を無視できなくなってきた現実世界と既存の法律の枠組みとのギャップに起因した様々な問題が露呈し、上述の事件に限らず、AIと知的財産権に関する様々な事件が発生しています。
10月30日、バイデン米国大統領はAIの開発、テスト、利用を管理するために連邦政府機関が取るべき指針となる原則と行動を定めた大統領令「Executive Order on the Safe, Secure, and Trustworthy Development and Use of Artificial Intelligence」に署名しました。この大統領令のセクション5.2には、イノベーションを促進し、AIと特許対象物の発明者性に関する問題を明確にするため、USPTO長官は、一定の期限までに、AIに関連する発明者の問題や著作権の問題についてのガイダンスの公表や行政措置の可能性について提言を行うものとすることが定められています。米国政府が2024年中にどのような方向性を打ち出すのか注目されています。
日本でも、AIと知的財産権等との関係をめぐる課題へ必要な対応方策等を検討するために、10月4日、政府(知的財産戦略本部)は「AI 時代の知的財産権検討会」をスタートさせました。
実務面でも、並行して、12月8日に開催された産業構造審議会知的財産分科会特許制度小委員会第17回審査基準専門委員会ワーキンググループにおいて、AI関連技術に関する事例を審査基準に新たに追加すること等が議論されました。例えば、追加事例5は、公知の化合物の化学構造と特性とを対応させたデータを学習データとして機械学習させたAIにより、ある機能を持つと推定された新たな化学構造を持つ化合物の発明に関する事例であり、AIにより薬効を持つ化学構造であると推定された新規化合物の発明の事例に置き換えてあれこれと想像するには参考になる事例といえるかもしれません。
このように、日本でも、AIと知的財産権等との関係をめぐる様々な課題について、政府内での議論が始まったばかり、しかし、急ピッチで進められています。
また、前述の米国大統領令もそうですが、AIの規制についての各国法整備や国際議論も進んでいます。
例えば、11月1日には、AIの安全管理やリスクへの対応策について協議するため各国政府やAI開発企業の代表ら約150人が集った世界初の「AI safety summit(AI安全サミット)」がロンドン郊外のブレッチリー・パークで開催され、その1か月後には、12月1日の「広島AIプロセスG7デジタル・技術閣僚声明」を支持するG7首脳声明が発出されるなど、国際社会での議論はスタートしてグローバルな具体的ルール作りはこれから・・・のように見えましたが、12月8日、EUは、加盟国と欧州議会、欧州委員会による3者協議でAI規制法案について大筋合意したと発表、加盟国と欧州議会による承認を経て成立すれば2026年にも同規制が適用されるという動きを見せています。
抗うことのできないAI時代の潮流に溺れる前に、各国政府は慌ててAIに関連する様々な議論を本格化させたのも、この2023年を象徴する出来事だったといえるでしょう。
実に多様な方面でのルールづくりの動きに対して、産業界は様々な視点で注意深く対応していく必要があるでしょう。

AIの爆発的発展。様々なレベルで法律・ルールの見直しや国際的枠組みの議論が、多方面且つグローバルで一斉に且つ急ピッチで進んでいます・・・2023年、まさにこの激動の歴史的瞬間に立ち会っているのです。
5.抗弁(こうべん)
今年の医薬系”特許的”な世相を表す漢字一文字「抗」にまつわる話題。最後の5つめは、「抗弁」です。
理研・ヘリオス・大阪大学の「網膜色素上皮細胞の製造方法」に関する特許第6518878号に対して、ビジョンケアが、公共の利益のための通常実施権の設定を求めて裁定を請求していました(裁定請求2021-1)が、請求から2年以上を経て、とうとう進展が見られたようです。
- 2021.10.03記事: 理研・ヘリオス・大阪大学の「網膜色素上皮細胞の製造方法」特許に公共の利益のための通常実施権の設定を求めてビジョンケアが裁定を請求・・・iPS細胞を用いた世界初の臨床応用からなかなか進まないヘリオス・大日本住友による加齢黄斑変性に対する再生医療の治験
ところで、裁定手続においては、特許発明の実施事実や計画に関する証拠として、企業情報や技術情報が含まれた書類の提出が求められることがあります。しかしこれまでの制度では、裁定手続に関連する書類の閲覧を制限できなかったため、営業秘密が漏洩する懸念があり、その結果、裁定請求人や特許権者が必要な書類提出を控えてしまい、適切な裁定が難しくなる可能性がありました。
この問題に対処するため、裁定手続において提出された書類に営業秘密が含まれている場合に閲覧を制限できるよう、法改正が行われ、7月3日に施行されました。
この法改正は、まさに、本件裁定請求事件のために手当てされたものと言っても過言ではないでしょう。
- 2023.06.08記事: 不正競争防止法等の一部を改正する法律案が国会で可決成立 - 裁定関係書類の閲覧制限についての改正 -
そして、本件裁定請求事件について、2年以上(計22回)に及ぶ開催と議論を尽くしてきた工業所有権審議会発明実施部会が、2023年11月14~16日にとうとう答申案を取りまとめ、今後は、工業所有権審議会総会において答申案の審議が行われます。
- 2021.12.17記事: 公共の利益のための通常実施権の許諾を求める裁定の請求2021-1 工業所有権審議会 発明実施部会(第1回)が開催

もし、この裁定請求が認められれば、これは通常実施権が裁定によって日本史上初めて設定される事例となります。
今後、医薬系の特許権侵害訴訟においては、訴えられた被告にとって、公共の利益のための通常実施権の設定のための「裁定に付する旨の抗弁(※)」を主張(裁定を請求)することが、新たな防御方法のひとつとして、その価値が見直されるかもしれません。
裁判所は、この抗弁を受けて、相当と認めるときは、「事件を裁定に付する」旨の決定をすることができるようにする(規定を設ける)ことへの期待も高まるかもしれません。
※抗弁(こうべん)とは、民事訴訟において、被告が原告の申立て(請求)を排斥するために、その基礎となる事実と両立しつつその法律効果を排斥する別個の事実(請求原因事実と両立する権利障害、阻止、消滅事由の主張)をいいます。
特許法は産業の発達に寄与することを目的とする法律ですが、発明の保護(独占性)という手段から、公共の利益との間で対立関係となることがあります。
特に、発明が医薬品に関連する場合には、公共の利益が国民の生命や健康に直接関わることとなるためその議論が顕著に現れることがあります。
本件裁定請求事件は、発明の保護と公共の利益の対立をバランス良く考慮する際の模範事例となるかもしれません。
参考
- 「裁定制度」の在り方に関する一考察(知財管理 Vol.68, No.1, p42(2018)特許第2委員会第5小委員会)
- 一般財団法人知的財産研究所 「標準規格必須特許の権利行使に関する調査研究(II)報告書」(2013年3月)
6.元旦記事のお知らせ
本記事では、「抗」をテーマに、「抗体」、「抗議」、「対抗」、「抗う」、「抗弁」というキーワードから、2023年を賑わせた医薬系”特許的”な出来事について、振り返りました。
こうして2023年を振り返ってみて、みなさまはどのようなことを感じられましたでしょうか。
この一年の振り返りに、本記事を楽しんでいただけたなら幸いです。
ぜひ、当ブログ(https://www.tokkyoteki.com)とX(旧Twitter)(@tokkyoteki)のフォローも何卒よろしくお願いします。
・・・
最後にお知らせです。
新春「医薬系特許的判例」クロスワードパズルを、2024年元旦にブログ記事としてアップする予定です。
2024年の縁起を担いで、最速で正解のご連絡をいただいた方には「一番福」🧧の称号が勝手に付与されます。
医薬や特許が専門ではないという方も、「カギのヒント」を見れば、必ず解るようになっていますので、ぜひ、お気軽にチャレンジしてくださいね♪
こたつに入って、みかんを食べながら、ぜひお楽しみください。

それでは、みなさま、良いお年をお迎えください。
※前回の2022年の振り返り記事と2023新春クロスワードパズルはこちら。





コメント