- コスメディ製薬の溶解型マイクロニードル製剤は、生体親和性の高いヒアルロン酸を基材とした微細なニードル(針)が整列したシート状に成形されたもの。皮膚に貼付することで、ニードルが直接皮膚の内部に入り、溶解・浸透する。
- バイオセレンタックも、溶解型マイクロニードル等のDDS技術をもとに経皮吸収製剤等の開発を行っており、溶解型マイクロニードル製剤を巡って、同社が保有する特許第4913030号に係る特許権侵害訴訟や無効審決取消訴訟等、バイオセレンタックとコスメディ製薬との間で10年以上にわたる特許紛争が続いていた。
- バイオセレンタックの特許第4913030号についてコスメディ製薬が請求した無効審判において、特許庁は、独立特許要件違反があると判断してバイオセレンタックの訂正請求を認めず、特許を無効とする審決をしたため、バイオセレンタックは、独立特許要件違反と判断した本件審決には誤りがあると主張して審決の取消しを求める訴訟を提起した。
- 知財高裁(第4部)は、本件審決を取り消すべき違法が認められないことは明らかであるから、バイオセレンタックの請求を棄却する判決をした。10年以上にわたる特許紛争はやっと収束しそうである。
1.コスメディ製薬の溶解型マイクロニードル製剤
コスメディ製薬株式会社は、2001年5月に有限会社コスメディとして設立され(京都薬科大学内で活動)、医薬品・化粧品・医療機器の研究開発および製造・販売をしている。2008年11月に世界初のマイクロニードル化粧品を上市した。
マイクロニードル技術とは、微細針の先端部に薬剤を含有させ、皮膚に貼付することで薬剤を体内に投与するパッチ形態の新規経皮吸収製剤。
- 参照: 2021.10.04 コスメディ製薬株式会社 https://prtimes.jp/main/html/rd/p/000000005.000069471.html
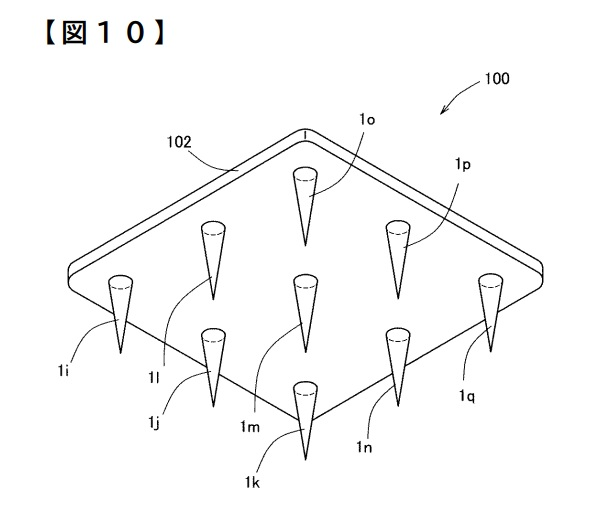
コスメディ製薬の独自技術で開発された溶解型マイクロニードルは、生体親和性の高い高分子ヒアルロン酸を基材として、薬剤や有効成分を混合したものを、用途や目的に合わせて数十から数百μmの長さの微細な針が整列したシート状に成形したものです。 皮膚に貼付することで、ニードルが直接皮膚の内部に入り、内部で溶解・浸透します。このため、薬剤を皮膚に塗布するよりも、はるかに効率的かつ多量の有効成分を伝達することが可能となります。 溶解型ニードルは、その効果はもとより、安全性や簡便性からも、注射に代わる剤型として、医薬分野だけでなく美容分野でも大変注目されています。
コスメディ製薬株式会社 website(https://cosmed-pharm.co.jp/innovation/)より
本記事で紹介する特許紛争において訴訟の対象となった商品ではないが、現在、コスメディ製薬が製造販売している保湿・肌ハリ・シート状美容液「Quanis Dermafiller(クオニス ダーマフィラー)」を購入し、ヒアルロン酸マイクロニードル技術がどんなものか試してみた(https://cosmedy.jp/shop/product_categories/quanis)。
粘着性のある肌色シートの中央に載っている透明シートがマイクロニードルが備わっている部分で、整列している「微細な針」をはっきりと肉眼で確認するのは難しかったが(誤ってこちらの中央の透明シートも剝がして捨ててしまうところであった・・・)、シートを気になる目尻に貼って全体を指で肌に押し当て密着させると、程良いチクチクを感じることができる。
シートを貼ったまま寝るわけだが、そのチクチク感が、皮膚に貼付したシート上の無数の微細な針である固体ヒアルロン酸が直接皮膚の内部に入って徐々に溶解・浸透していくのだと想像させてくれる。

翌日、シートを貼っていた部分の肌には少しハリがでてきたような・・・若返ったかな。
2.マイクロニードルを巡るバイオセレンタックとコスメディ製薬との特許紛争
(1)バイオセレンタックとコスメディ製薬との特許権侵害訴訟
株式会社バイオセレンタックは、元京都薬科大学薬物動態学教室教授の高田寛治氏が薬物動態、製剤技術、DDSに関する研究成果として取得した数々の特許の実用化を図ることを目的として2001年8月1日に設立された。自己溶解型マイクロニードル等のDDS技術をもとにして経皮吸収製剤等の共同開発を行っている(株式会社バイオセレンタックwebsiteより)。
バイオセレンタックの高田寛治氏は、2009年7月に、コスメディ製薬がヒアルロン酸マイクロニードルを発売するということを新聞記事で知ったようである(後述の大阪地裁平成27年(ワ)11759 別紙1)。
バイオセレンタックが既に2005年1月31日にしていた「経皮吸収製剤,経皮吸収製剤保持シート,及び経皮吸収製剤保持用具」に関する出願(優先日)は特許第4913030号として2012年1月27日に登録された。
特許第4913030号の【請求項1】(登録時)
水溶性かつ生体内溶解性の高分子物質からなる基剤と、該基剤に保持された目的物質とを有し、皮膚に挿入されることにより目的物質を皮膚から吸収させる経皮吸収製剤であって、
前記高分子物質は、コンドロイチン硫酸ナトリウム、ヒアルロン酸、グリコーゲン、デキストラン、キトサン、プルラン、血清アルブミン、血清α酸性糖タンパク質、及びカルボキシビニルポリマーからなる群より選ばれた少なくとも1つの物質であり、
尖った先端部を備えた針状又は糸状の形状を有すると共に前記先端部が皮膚に接触した状態で押圧されることにより皮膚に挿入される、経皮吸収製剤。
2012年5月2日、コスメディ製薬は、同特許に対して無効審判を請求している(無効2012-800073号事件)。無効審判事件については後述する。
バイオセレンタックは、2013年2月20日、コスメディ製薬らによる体内で溶解する微小針であるマイクロニードル技術を用いた化粧品の製造・販売が、特許第4913030号に係る特許権の侵害に当たる旨主張して、コスメディ製薬らに対し同製品の製造・販売の差止めを求めるとともに特許権侵害に基づく損害賠償金等の支払を求めた。
しかし、東京地裁は、本件特許には進歩性欠如の無効理由があり、特許無効審判により無効にすべきものと認められるから、バイオセレンタックは本件特許権に基づく権利を行使することができない、と判断した(東京地裁平成25年(ワ)4303)。
知財高裁もバイオセレンタックの控訴を棄却し(知財高裁平成26年(ネ)10109)、コスメディ製薬らに対する特許権侵害訴訟は特許権者であるバイオセレンタックの敗訴で確定した。
そして、今度は、コスメディ製薬と同社の代表取締役であるP1が、上記訴訟の原告であったバイオセレンタック、同訴訟でバイオセレンタックを代表した代表取締役のP2、バイオセレンタックの代表取締役であり本件特許の発明者であるP3並びに同訴訟で訴訟代理人を務めたP4に対し、バイオセレンタックが「コスメディによる本件特許権侵害及び研究成果盗用」という虚偽の事実をコスメディ製薬の取引先である岩城製薬及び資生堂に告知した行為は不競法2条1項14号(現行法では21号「競争関係にある他人の営業上の信用を害する虚偽の事実を告知し、又は流布する行為」)の不正競争に該当する或いは上記告知がP1の名誉を棄損したと主張して、損害賠償の支払を求め訴訟を提起した。
しかし、大阪地裁は、コスメディ製薬の請求を棄却(参考: 2016.05.10 「コスメディ製薬 v. バイオセレンタック」 大阪地裁平成27年(ワ)11759)、知財高裁も控訴を棄却した(参考: 2017.03.22 「コスメディ製薬 v. バイオセレンタック」 知財高裁平成28年(ネ)10094)。

(2)繰り返されたバイオセレンタックの特許請求の範囲の訂正
2012年5月2日、コスメディ製薬は、同特許に対して無効審判を請求した(無効2012-800073号事件)。
特許庁は、バイオセレンタックの訂正請求(「皮膚に挿入される,経皮吸収製剤」とあるのを,「皮膚に挿入される,経皮吸収製剤(但し,・・・及び経皮吸収製剤を収納可能な貫通孔を有する経皮吸収製剤保持用具の貫通孔の中に収納され,該貫通孔に沿って移動可能に保持された状態から押し出されることにより皮膚に挿入される経皮吸収製剤を除く)」に訂正)を認め無効審判請求は成り立たないと審決した。
コスメディ製薬は同審決の取消しを求めて審決取消訴訟を提起した。
裁判所は、訂正が特許請求の範囲の減縮を目的とするものということができるための前提として、訂正前後の特許請求の範囲の記載がそれぞれ技術的に明確であることが必要であるとして、本件訂正事項による訂正後の請求項1の記載は、技術的に明確であるとはいえないから、本件訂正事項は特許請求の範囲の減縮を目的とするものとは認められないと判断し、審決を取消した(参照: 2015.03.11 「コスメディ製薬 v. バイオセレンタック」 知財高裁平成26年(行ケ)10204)。

審決は取消され、特許庁で再審理となったが、訂正請求を認めて審判請求を不成立とした審決に対する2回目の取消訴訟(2013.11.27 平成25年(行ケ)10134)を経て、特許庁は、バイオセレンタックの新たな訂正請求(「針状又は糸状の形状を有すると共に」とあるのを「針状又は糸状の形状を有し,シート状支持体の片面に保持されると共に」に訂正)を認め、無効審判請求は成り立たないと審決した。
コスメディ製薬はこれを不服として3回目となる審決取消訴訟を提起し、裁判所は、訂正後の請求項1の記載は、技術的に明確であるとはいえないから、本件訂正事項は、特許請求の範囲の減縮を目的とするものとは認められないと判断し、またもや審決を取消した(参照: 2017.07.12 「コスメディ製薬 v. バイオセレンタック」 知財高裁平成28年(行ケ)10160)。

これまで、バイオセレンタックの訂正請求を認めた特許庁審決は裁判所で取消される、ということが何度も繰り返されたわけである。
審決は取消され、特許庁で再審理となったが、特許庁は、バイオセレンタックの新たな訂正請求(特許請求の範囲の請求項1に「皮膚に挿入される,経皮吸収製剤」とあるのを「皮膚に挿入される,経皮吸収製剤(但し,目的物質が医療用針内に設けられたチャンバに封止されるか,あるいは縦孔に収容されることによって基剤に保持されている経皮吸収製剤を除く)」に訂正)を認め、無効審判請求は成り立たないと審決した。
コスメディ製薬はこれを不服として4回目となる審決取消訴訟を提起した。
しかし、裁判所は、本件訂正事項を認め、コスメディ製薬の請求を棄却した(参照: 2019.02.06 「コスメディ製薬 v. バイオセレンタック」 知財高裁平成30年(行ケ)10100)。

コスメディ製薬はこの判決を不服として最高裁へ上訴したが、上告受理申立却下となり、同審決(無効2012-800073号事件)は2019年12月17日に確定した。
コスメディ製薬が特許第4913030号に対して請求していたもうひとつの無効審判(無効2013-800146号事件)は上記審決が確定したことで、2020年1月17日に特許庁での審理が再開した。
本記事で紹介するのがこの無効2013-800146号事件に係る審決取消請求事件(知財高裁令和3年(行ケ)10089)である。
コスメディ製薬が特許第4913030号に対して最初に無効審判を請求し、紛争が勃発してから少なくとも10年以上が経過した。
3.本件(知財高裁令和3年(行ケ)10089)の背景
(1)本件訴訟提起に至った経緯
本件(知財高裁令和3年(行ケ)10089)は、バイオセレンタック(原告)の「経皮吸収製剤、経皮吸収製剤保持シート、及び経皮吸収製剤保持用具」に関する特許第4913030号についてコスメディ製薬(被告)が請求した無効審判(無効2013-800146号事件)において、バイオセレンタックが請求項1及びこれに従属する一群の請求項について訂正請求をしたが、特許庁は、本件訂正発明13には独立特許要件違反がある(引用発明2との相違点1C及び3Cが当業者にとって容易に想到できる)と判断して本件訂正を認めず、本件発明(請求項1、19)についての特許を無効とする審決をしたため、バイオセレンタックが独立特許要件違反と判断した本件審決には誤りがあると主張して審決の取消しを求めた訴訟である。
(2)本件訂正発明1、13、19
本件訂正発明1、13、19(下線部が訂正により加えられた部分)
【請求項1】
水溶性かつ生体内溶解性の高分子物質からなる基剤と、該基剤に保持された目的物質とを有し、皮膚(但し、皮膚は表皮及び真皮から成る。以下同様)に挿入されることにより目的物質を皮膚から吸収させる経皮吸収製剤であって、
前記基剤は自己溶解するものであり、
前記高分子物質は、コンドロイチン硫酸ナトリウム、ヒアルロン酸、グリコーゲン、デキストラン、プルラン、血清アルブミン、血清α酸性糖タンパク質、及びカルボキシビニルポリマーからなる群より選ばれた少なくとも1つの物質(但し、デキストランのみからなる物質は除く)であり、
基剤、目的物質及び水を含む曳糸性を示す糊状物が乾燥した物であり、
尖った先端部を備えた針状又は糸状の形状を有すると共に前記先端部が皮膚に接触した状態で押圧されることにより皮膚に挿入される、経皮吸収製剤
(但し、目的物質が医療用針内に設けられたチャンバに封止されるか、あるいは縦孔に収容されることによって基剤に保持されている経皮吸収製剤を除く)。
【請求項13】
前記目的物質は、薬物、生理活性物質、化粧品、又は栄養素に属するものである請求項1~12のいずれかに記載の経皮吸収製剤。
【請求項19】
シート状の支持体の片面に請求項1~17のいずれかに記載の経皮吸収製剤が1又は2個以上保持され、皮膚に押し当てられることにより前記経皮吸収製剤が皮膚に挿入される経皮吸収製剤保持シート。
(3)本件訂正発明13と引用発明2の相違点1C及び3C
相違点1C
本件訂正発明13は、「高分子物質」が、「水溶性かつ生体内溶解性」で、「コンドロイチン硫酸ナトリウム、ヒアルロン酸、グリコーゲン、デキストラン、プルラン、血清アルブミン、血清α酸性糖タンパク質、及びカルボキシビニルポリマーからなる群より選ばれた少なくとも1つの物質(但し、デキストランのみからなる物質は除く)であり」、「基剤」が、「自己溶解するもの」であるのに対し、引用発明2は、「ポリマー」が、「可溶性(溶融性および生分解性を含む)」とされており、「固体マトリクス」が、自己溶解するものとの特定がない点。
相違点3C
本件訂正発明13は、経皮吸収製剤が、「基剤、目的物質及び水を含む曳糸性を示す糊状物が乾燥した物であ」るのに対し、引用発明2には、そのような特定がされていない点。
4.裁判所の判断
主 文
1 原告の請求を棄却する。
2 訴訟費用は原告の負担とする。
裁判所(知財高裁・第4部)は、「本件訂正発明13は、特許出願の際独立して特許を受けることができるものではなく、請求項13についての訂正が認められないから、請求項1~17及び19からなる一群の請求項についての訂正及びこの訂正に関連した明細書の記載についての訂正は、一体的に認められないとした本件審決の判断に誤りはない。」として、原告主張の取消事由は理由がなく、本件審決を取り消すべき違法が認められないことは明らかであるから、原告の請求を棄却することとし、主文のとおり判決した。
以下に、裁判所の判断を一部抜粋する。
(1)相違点1Cの容易想到性について
「引用発明2と甲1-1文献に記載の装置は、薬剤の経皮投与に関するもので技術的分野を共通にし、針を使用する場合の恐怖感、不快感という共通の課題の解決を図るものである。また、引用発明2と、甲1-1文献に記載の装置及び薬とは、生体内溶解性の基剤(マトリクス又はキャリア)に目的物質である薬物を保持させることにより、尖った先端部を有する穿孔器ないし固体薬物を成形し、これを患者の皮膚を通して直接投与し、薬効を発現させる剤という点で、課題解決原理を同じくする。
引用発明2においては、微小穿孔器がかなり迅速に溶解し、角質層を貫通するように十分強い限り、任意の生体適合性材料が、微小穿孔器として役立ち得るとされている(【0024】)。
ヒアルロン酸は、活性成分の即時送達用の水溶性キャリアとして甲1-1文献の9頁18ないし30行目に列挙された中の冒頭に記載されている。ヒアルロン酸が、生体内において、タンパク質と共に粘稠な溶液やゲルを作って、細胞間質として組織構造の維持や、関節では潤滑作用を営む物質であり、水溶性かつ生体内溶解性であること(岩波理化学辞典第4版(甲8)の「ヒアルロン酸」の項)、皮膚は水を含み、表皮と真皮を合わせた水分量は57.7%であるが(甲33)、真皮の水分量は70%程度で(甲12)、これは、生体内の他の組織とほぼ同程度であること(甲13)はいずれも技術常識に属するから、ヒアルロン酸は真皮で溶解するといえる。
また、強度の観点からいうと、甲1-1文献の請求項1には「該薬が患者の皮膚を貫通するのに十分な構造強度のものであるときに患者の皮膚を通して押し出すことができることを特徴とする装置」との記載があるから、同文献において水溶性キャリアとして例示されているヒアルロン酸は、皮膚を貫通する十分な構造的強度を有するものといえる。
甲2-1文献においてマトリクス材料として列挙される材料と、甲1-1文献においてキャリアとして列挙される材料とは、共通するものが複数あり(セルロース、ヒドロキシプロピルメチルセルロース、ヒドロキシエチルセルロース、ゼラチン等)、当業者は、この点からも、甲1-1文献記載のキャリアを甲2-1文献のマトリクス材料として使用してみようと試みるものといえる。
そうすると、当業者は、引用発明2のポリマーとして、甲1-1文献記載の水溶性かつ生体内溶解性を有するヒアルロン酸を採用し、皮膚に挿入された際に自己溶解して薬物が送達されるものとすることは容易に想到し得たものといえる。」
(2)相違点3Cの容易想到性について
「本件優先日において、ヒアルロン酸が曳糸性を有することは技術常識であったものということができる。「糊状物」が何を意味するかについて、訂正明細書には記載するところはないが、・・・本件訂正発明13において、「糊状」とは、引離法において引き離された形態が保持される程度の、また、鋳型法において、鋳型に押し付けて充填できる程度の賦形性を有するものであると理解でき、さらに、「曳糸性を示す糊状物」とは、そのような性質を有し、かつ、糸を引く性質を有するものであると理解できる。
・・・また、甲57実験成績証明書によれば、ヒアルロン酸の水溶解物は、0.5重量%及び5重量%のものは、水溶液であり、10重量%のものは、粘稠な水溶液であり、30重量%及び40重量%のものは糊状物であったとされ、被告による実験報告書2(乙19。以下「乙19実験報告書」という。)には、ヒアルロン酸の、0.5%、5%、10%、30%及び40%水溶液に関しての記載があり、40%水溶液は、液体ではなく流動性を失ったゲル状半固形物であったことが記載されており、いずれの結果も、ヒアルロン酸濃度が低いと液体状で、濃度が高くなると糊状(ゲル状)になることが示されている。
・・・そして、そのような液体溶液は粘度によって糊状にも粘稠な液体にもなり得るのであって、その差は相対的であり、いずれの状態になるように調整するにしても、それは、当業者が適宜設定し得た事項にすぎない。
ヒアルロン酸は曳糸性を有することは・・・技術常識である以上、当業者においてこのように適宜調整された液体溶液は、曳糸性を示すものになるといえる。なお、甲57実験成績証明書及び乙19実験報告書からみれば、希薄なヒアルロン酸水溶液は曳糸性を示さないが、鋳型で乾燥させてマイクロニードルを作るに当たって、乾燥させるという目的からみて、そのような希薄な溶液を使用することは想定されない。
以上によれば、引用発明2において、甲1-1文献に記載のヒアルロン酸を採用する際に、ヒアルロン酸と薬剤を含む液体溶液を、「曳糸性を示す糊状物」とすることは、当業者が容易になし得たことというべきである。」
(3)顕著な作用効果について
「原告は、・・・本件訂正発明は、基剤、目的物質及び水を含む曳糸性を示す糊状物を乾燥させるという構成を採用することにより物理的強度と優れた水溶性という2つの効果を両立するものであり、これらの効果は、訂正明細書(実施例1ないし23)から把握できる旨主張する。
訂正明細書の【0106】ないし【0163】には、実施例1ないし24として、基剤、目的物質及び水を含む曳糸性を示す糊状物を乾燥させたこと(実施例1ないし9、11ないし21、24は引離法、実施例10、22及び23は鋳型法)、実施例3ないし6、11、12、17、18、20、21においては、上記目的物質(薬剤)をマウスに皮膚から投与し、効果があったことが記載されている。
しかし、訂正明細書等を全体としてみても、これらの効果が奏されたことが曳糸性を示す糊状物を乾燥させるという構成を採用したことによるものであることを示唆する記載はない。・・・訂正明細書における上記構成に係る記載は、いずれも製造上の便宜に関するものというべきであり、上記構成の技術的意義については何らの記載もない。
他方で、甲2-1文献には、微小穿孔器が、皮膚の穿孔のために、図2Aないし2Gに示されるような尖らせてあるか鋭利にされた形状を有すること(【0018】、【0021】)、鋳型を用いる方法等により微小穿孔器を製造することができること(【0025】)が記載されているのであるから、実際に微小穿孔器を製造したことや使用したことの記載がなくても、物理的強度の課題を解決することについての具体的手段が示されているといえる。甲1-1文献に記載の薬も患者の皮膚を貫通するのに十分な構造強度のものであることは前記・・・のとおりである。
そうすると、原告主張の効果は、相違点3Cに係る本件訂正発明の構成を採用することにより、当業者が予想し得る範囲のものであるというべきであるから、原告の上記主張は採用できない。」
5.コメント
裁判所は、引用発明と副引用例とは、薬剤の経皮投与に関するもので技術的分野を共通にし、生体内溶解性の基剤に目的物質である薬物を保持させることにより、尖った先端部を有する穿孔器ないし固体薬物を成形し、これを患者の皮膚を通して直接投与し、薬効を発現させる剤という点で、針を使用する場合の恐怖感、不快感という課題を解決する原理を同じくすることから、当業者は、引用発明に副引用例のヒアルロン酸を適用し、本件訂正発明との相違点に容易に想到し得ると判断した。
敗訴したバイオセレンタックが最高裁へ上訴する可能性はあるが、知財高裁がコスメディ製薬によるバイオセレンタック特許の無効請求を認める審決を維持したこと、同特許に係る別件特許権侵害訴訟事件でもコスメディ製薬が勝訴判決を得ていることから、溶解型マイクロニードル製剤を巡るバイオセレンタックとコスメディ製薬との間で繰り広げられていた10年以上にわたる特許紛争はやっと収束しそうである。




コメント