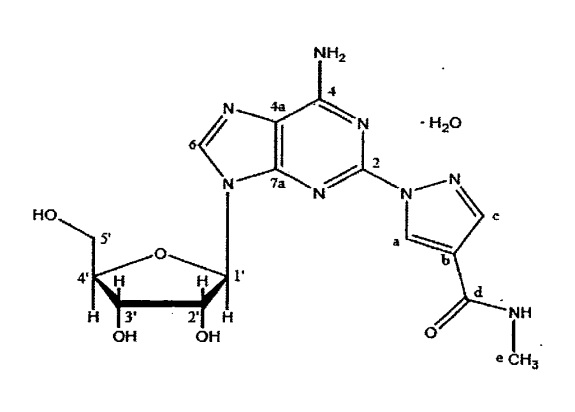
 アステラス製薬が米国で販売している心機能検査補助剤Lexiscan®(レキスキャン、活性成分: regadenoson)について、Hospira社がその後発品承認を求める簡略新薬申請(Abbreviated New Drug Applications: ANDA)を米国食品医薬品局(FDA)に提出したことから、アステラス製薬及び特許権者であるGilead社がHospira社に対して提起していた特許権侵害訴訟において、2022年5月19日、米国デラウェア州連邦地方裁判所は、Hospira社による特許無効の抗弁を取り上げるまでもなく、Hospira社はいずれの特許権(米国特許8,106,183、8,524,883、RE47301)も侵害していないとの判決を下しました。
アステラス製薬が米国で販売している心機能検査補助剤Lexiscan®(レキスキャン、活性成分: regadenoson)について、Hospira社がその後発品承認を求める簡略新薬申請(Abbreviated New Drug Applications: ANDA)を米国食品医薬品局(FDA)に提出したことから、アステラス製薬及び特許権者であるGilead社がHospira社に対して提起していた特許権侵害訴訟において、2022年5月19日、米国デラウェア州連邦地方裁判所は、Hospira社による特許無効の抗弁を取り上げるまでもなく、Hospira社はいずれの特許権(米国特許8,106,183、8,524,883、RE47301)も侵害していないとの判決を下しました。
Regadenosonの一水和物に関する発明を保護する特許で、元々はCV Therapeutics社が特許権者であったところ、買収によりGilead社が現在の特許権者となっています。
- 2022.05.19 Astellas US LLC et al v. Hospira, Inc. Case Number: 1:18-cv-01675; Opinion
今後、アステラス製薬は、この判決に対して上訴し、訴訟が決着するまでの間、Hospira社によるLexiscan®の後発品発売を停止するための措置を取る予定とのことです。
- 2022.05.20 アステラス製薬 press release: 心機能検査補助剤「Lexiscan®(レキスキャン)」特許侵害訴訟の判決について
「Lexiscan®」は、アステラス製薬が2000年7月にCV Therapeutics社から導入(北米における共同開発ならびに独占的販売権を取得)した核医学検査等の心機能検査時の薬理学的負荷としての使用を目的とした注射剤です。
冠血管平滑筋、血管内皮等に多く存在するアデノシンA2A受容体を選択的に刺激するメカニズムをもつ薬剤で、急速静注により迅速に冠血管を拡張させるとともに、体重による用量調節が不要な心機能検査補助剤です。
2008年4月10日、CV Therapeutics社がFDAから承認を取得しました(現在のNDA holderは、Astellas Pharma US, Inc.)。
- 2008.04.11 アステラス製薬 press release: 心機能検査補助剤「LexiscanTM(レキスキャン)」米国での承認取得のお知らせ
- 2008.06.25 アステラス製薬 press release: 心機能検査補助剤「LexiscanTM(レキスキャン)」米国での新発売のお知らせ
その後、CV Therapeutics社を巡って「すったもんだ」の買収劇がありましたが・・・。
- 2009.02.27 アステラス製薬 press release: 米国医薬品会社CV Therapeutics社に対する株式公開買付けに関するお知らせ
- 2009.03.12 Gilead press release: Gilead Sciences Agrees to Acquire CV Therapeutics for $20.00 Per Share
- 2009.03.16 アステラス製薬 press release: 米国医薬品会社CV Therapeutics社に対する買収提案終結に関するお知らせ
Lexiscan®(レキスキャン)の2022年3月期での年間売上収益(米国)は、$725Mと小さくありません。
- 2022.04.27発表 アステラス製薬 2021年度決算 2022年3月期 決算補足資料
2022年4月11日、FDAは、
- DR REDDYS LABORATORIES LTD
- ACCORD HEALTHCARE INC、
- APOTEX INC
- HONG KONG KING FRIEND INDUSTRIAL CO LTD
の4社のANDAを承認しています。
後発品の市場参入となれば、アステラス製薬の今後の業績への影響は少なからずあるかもしれません。


コメント