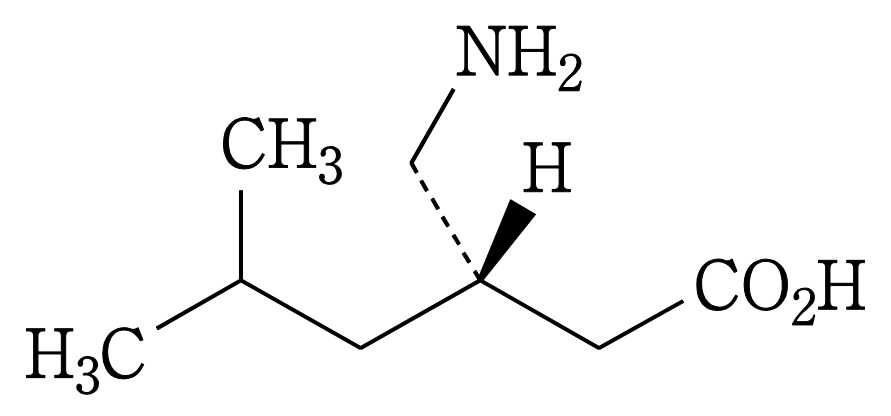
 本件(東京地裁令和2年(ワ)19927)は、発明の名称を「イソブチルGABAまたはその誘導体を含有する鎮痛剤」とする特許第3693258号に係る特許権の特許権者である原告(ワーナー-ランバート)が、被告(小林化工)に対し、プレガバリンを有効成分とし「効能又は効果」を「神経障害性疼痛・線維筋痛症に伴う疼痛」として承認を受けた後発医薬品プレガバリンOD錠「KN」(被告医薬品)が本件特許の特許請求の範囲の請求項1ないし4記載の各発明の技術的範囲に属し、被告による被告医薬品の製造等が上記各発明の実施に当たると主張して、特許法100条1項に基づく被告医薬品の製造等の差止め並びに同条2項に基づく被告医薬品の廃棄を求めた事案である。
本件(東京地裁令和2年(ワ)19927)は、発明の名称を「イソブチルGABAまたはその誘導体を含有する鎮痛剤」とする特許第3693258号に係る特許権の特許権者である原告(ワーナー-ランバート)が、被告(小林化工)に対し、プレガバリンを有効成分とし「効能又は効果」を「神経障害性疼痛・線維筋痛症に伴う疼痛」として承認を受けた後発医薬品プレガバリンOD錠「KN」(被告医薬品)が本件特許の特許請求の範囲の請求項1ないし4記載の各発明の技術的範囲に属し、被告による被告医薬品の製造等が上記各発明の実施に当たると主張して、特許法100条1項に基づく被告医薬品の製造等の差止め並びに同条2項に基づく被告医薬品の廃棄を求めた事案である。
1.はじめに(リリカ®用途特許を巡る本件事件の背景)
本件特許権に係る専用実施権者であるファイザーは、プレガバリンを有効成分とし「効能又は効果」を「神経障害性疼痛・線維筋痛症に伴う疼痛」とする先発医薬品リリカ®(カプセル・OD錠)を販売しており、リリカ®は、2019年度には国内売上が1000億円を超える大型製品となっていた(2021年9月にファイザーからヴィアトリス製薬へ製造販売移管)。
ジェネリックメーカーは、リリカ®の再審査期間終了(2018年4月15日)後にリリカ®のジェネリックの薬事承認を申請できるが、リリカ®を保護する本件特許(効能・効果を保護する医薬用途特許)の問題を回避できなければ、そのジェネリックの承認を取得し販売することはできない。
本件特許は、実は20年の存続期間満了日が2017年7月16日であったところ、効能・効果追加承認ごとに特許存続期間の延長が登録され、最長満了日は2022年7月16日となっており、リリカ®のジェネリック参入に対抗する最後の砦となっていた。
このようにジェネリックの参入障壁となっていた本件特許に対して、2017年1月16日、ジェネリックメーカーである沢井製薬は、とうとう特許無効審判を請求した(無効2017-800003号事件)。審判には、他のジェネリックメーカーも次々と沢井製薬側への参加を表明(15社)。本件被告(小林化工)もその参加人として審判に加わった一社であった。
参考記事:
審判請求から3年半が経過した2020年7月14日、その特許無効審判事件において、特許庁の審決が下された。その内容は、特許権者(原告)による請求項1及び2に係る本件訂正を認めず、請求項1及び2に係る発明についての本件特許を無効とし、他方、請求項3及び4に係る本件訂正を認め、請求項3及び4に係る発明についての審判の請求は成り立たないというものであった(以下「本件審決」という。)。
参考記事:
この審決に対して、原告は、本件審決のうち請求項1及び2に係る部分の取消しを求める審決取消訴訟(知財高裁令和2年(行ケ)第10135号)を提起している。なお、本件審決のうち請求項3及び4に係る部分は確定したので、本件特許の請求項3及び4は以下の表1のとおりに訂正された。
以下の表1を見てほしい。本事件のポイントは、リリカ®のジェネリック(被告医薬品)の「効能又は効果」である「神経障害性疼痛・線維筋痛症に伴う疼痛」が、各請求項の「炎症性疼痛」及び「術後疼痛」という構成要件を充足するかどうかである。
| 請求項 | 訂正前 | 訂正後 | 審決での訂正可否判断 |
|---|---|---|---|
| 1 | (本件発明1) 式I(省略)(式中,R1は炭素原子1〜6個の直鎖状または分枝状アルキルであり,R2は水素またはメチルであり,R3は水素,メチルまたはカルボキシルである)の化合物またはその医薬的に許容される塩,ジアステレオマー,もしくはエナンチオマーを含有する痛みの処置における鎮痛剤。 | (本件訂正後発明1) 式I(省略)(式中,R1は炭素原子1〜6個の直鎖状または分枝状アルキルであり,R2は水素またはメチルであり,R3は水素,メチルまたはカルボキシルである)の化合物またはその医薬的に許容される塩,ジアステレオマー,もしくはエナンチオマーを含有する,痛覚過敏又は接触異痛の痛みの処置における鎮痛剤。 | 否 |
| 2 | (本件発明2) 化合物が,式IにおいてR3およびR2はいずれも水素であり,R1は-(CH2)0-2-iC4H9である化合物の(R),(S),または(R,S)異性体である請求項1記載の鎮痛剤。 | (本件訂正後発明2) 式I (省略)(式中,R3およびR2はいずれも水素であり,R1は-(CH2)0-2-iC4H9である)の化合物の(R),(S),または(R,S)異性体を含有する,神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛みの処置における鎮痛剤。 | 否 |
| 3 | (本件訂正前発明3) 化合物が,(S)-3-(アミノメチル)-5-メチルヘキサン酸または3-アミノメチル-5-メチルヘキサン酸である請求項1記載の鎮痛剤。 | (本件発明3) (S)-3-(アミノメチル)-5-メチルヘキサン酸または3-アミノメチル-5-メチルヘキサン酸を含有する,炎症を原因とする痛み,又は手術を原因とする痛みの処置における鎮痛剤。 | 可 |
| 4 | (本件訂正前発明4) 痛みが炎症性疼痛,神経障害による痛み,癌による痛み,術後疼痛,幻想肢痛,火傷痛,痛風の痛み,骨関節炎の痛み,三叉神経痛の痛み,急性ヘルペスおよびヘルペス後の痛み,カウザルギーの痛み,特発性の痛み,または線維筋痛症である請求項1記載の鎮痛剤。 | (本件発明4) 式I(省略)(式中,R1は炭素原子1〜6個の直鎖状または分枝状アルキルであり,R2は水素またはメチルであり,R3は水素,メチルまたはカルボキシルである)の化合物またはその医薬的に許容される塩,ジアステレオマー,もしくはエナンチオマーを含有する,炎症性疼痛による痛覚過敏の痛み,又は術後疼痛による痛覚過敏若しくは接触異痛の痛みの処置における鎮痛剤。 | 可 |
上記のとおり本件特許の無効審決は取消訴訟係属中であり、請求項の無効が確定したわけではなく、訂正により有効と判断された請求項の属否判断がされたわけでもないが、厚生労働省は、特許庁での一部無効審決を以って、パテントリンケージを働かせることなく、2020年8月17日、リリカ®のジェネリック(被告医薬品含む22社80品目!)を初承認し、同年12月11日には各ジェネリックメーカーが一斉にジェネリックを薬価基準収載・販売するに至った。
厚生労働省がジェネリックを承認した同日、ファイザーは、「特許庁が2020年7月14日に審決したリリカ用途特許の特許無効審判にて訂正を認めた特許請求項が、リリカが製造販売承認を取得している神経障害性疼痛および線維筋痛症に伴う疼痛の適応症を対象としているため、特許満了前のジェネリック医薬品の承認とそれに続く販売は特許権の侵害にあたると考えています。」との声明とともに、複数のジェネリックメーカーを相手取り、東京地裁に特許権侵害訴訟を提起するとともに仮処分命令の申し立てを行ったと発表した(2020.08.17 ファイザー press release: 「リリカ®」に関する特許権侵害訴訟および仮処分命令の申し立てについて)。この記事で紹介するのがその特許権侵害訴訟の東京地裁判決(東京地裁令和2年(ワ)19927)である。
仮に、ファイザーの主張するとおり、リリカ®のジェネリックの販売行為が本件特許権の侵害に当たるとの判決に至れば、リリカ®の全てのジェネリックの供給は違法となり停止せざるを得なくなる可能性、結果、医薬品の安定供給に支障をきたし、公衆衛生に問題が生じる可能性、別の見方で言えば、特許権侵害に該当するジェネリックを特許が存在するにもかかわらず承認した厚生労働省のパテントリンケージの運用が抱える問題によって医薬品供給に混乱を招くおそれ・・・がまさに顕在化する可能性もあった。
参考記事:

当初、ファイザーは、「複数の」ジェネリックメーカー(どのメーカーかは不明)を相手取り、東京地裁に特許権侵害訴訟を提起したと発表したが、本件判決言渡し時点で被告は小林化工のみであった。
本件訴訟の被告が小林化工のみであったことから、当初被告として提訴された他のジェネリックメーカーへの提訴は取下げたのか、それとも別訴訟で被告として提訴されているのかは現在点で不明である。もし、他のジェネリックメーカーを訴えていないまたは訴えを取り下げたのだとすると、他のメーカーとファイザーとの間で何かしらの和解で合意したのか、2021年9月にファイザーからリリカ®の製造販売移管受けたヴィアトリス製薬(MylanとPfizerの事業部門pjohnとの統合により誕生。ジェネリックメーカーとしてリリカ®OD錠のオーソライズドジェネリック(AG)も販売)の戦略上の判断なのか、本件訴訟で勝訴判決を得てから一斉にジェネリックを訴える作戦だったのか・・・は明らかでない。
しかし、被告小林化工は、2020年12月4日(この1週間後に被告医薬品は薬価基準収載された)に発覚した抗真菌剤イトラコナゾール錠に睡眠剤成分が混入した問題で、全ての医薬品の一時出荷停止(2021年12月に医薬品の製造工場などをサワイグループホールディングスに譲り渡すことで合意と発表)、特に被告医薬品は現在も販売していないようであることもあり、本件判決の結論はさておき、小林化工を相手にして本件訴訟で差止め及び廃棄を求めつづけたことにどれだけ意味があったのだろうか、と思うところはある。
- 2022.01.31 小林化工お知らせ: 疼痛治療剤(神経障害性疼痛・線維筋痛症)プレガバリン OD錠 25mg・50mg・75mg・150mg「KN」自主回収(クラスⅡ)のお知らせ
2.争点と裁判所の判断(結論)
裁判所は、本件発明1及び2については、無効の抗弁は理由があり、訂正の再抗弁は理由がないこと、本件発明3及び4については、被告医薬品は各技術範囲に属するとは認められないから、延長登録された本件特許権の効力が被告医薬品の製造等に及ぶかについて判断するまでもなく、原告の請求はいずれも理由がないとしてこれを棄却する判決をした。
各争点の裁判所の結論は赤字のとおり。
(1) 本件発明1及び2について
ア 無効の抗弁
(ア) 実施可能要件違反の成否(争点1-1)・・・「実施可能要件に違反する」
(イ) サポート要件違反の成否(争点1-2)・・・「サポート要件に違反する」
イ 訂正の再抗弁
(ア) 本件訂正が訂正要件を満たすか(争点1-3)・・・「本件訂正は訂正要件違反であるから訂正の再抗弁は理由がない」
(イ) 本件訂正により無効理由が解消されるか(争点1-4)
ウ 延長登録された本件発明1及び2に係る本件特許権の効力が被告医薬品の製造等に及ぶか(争点1-5)
(2) 本件発明3及び4について
ア 被告医薬品が本件発明3及び4の技術的範囲に属するか
(ア) 文言侵害の成否(争点2-1)・・・「被告医薬品は、効能・効果を神経障害性疼痛及び線維筋痛症に伴う疼痛とする疼痛治療剤であり、「炎症性疼痛」及び「術後疼痛」の鎮痛剤であるとは認められないから、構成要件を充足するとは認められない」
(イ) 均等侵害の成否(争点2-2)・・・「被告医薬品は、均等の第1及び5要件を満たさず、本件発明3及び4の構成と均等なものとは認められない」
イ 延長登録された本件発明3及び4に係る本件特許権の効力が被告医薬品の製造等に及ぶか(争点2-3)
3.裁判所の判断
裁判所は、本件発明1及び2については、無効の抗弁は理由があり、訂正の再抗弁は理由がないこと、本件発明3及び4については、被告医薬品は各技術範囲に属するとは認められないから、延長登録された本件特許権の効力が被告医薬品の製造等に及ぶかについて判断するまでもなく、原告の請求はいずれも理由がないとしてこれを棄却する判決をした。
以下に、主な争点についての裁判所の判断を紹介する。
(1)本件発明1及び2の実施可能要件違反の成否
ア 医薬用途発明の実施可能要件違反の判断基準について
裁判所は、医薬用途発明の実施可能要件を満たすための基準を以下のとおり判示した。
「いわゆる医薬用途発明においては,一般に,当業者にとって,物質名,化学構造等が示されることのみによっては,当該用途の有用性及びそのための当該医薬の有効量を予測することは困難であり,当該発明に係る医薬を当該用途に使用することができないから,そのような発明において実施可能要件を満たすためには,明細書の発明の詳細な説明に,薬理データの記載又はこれと同視し得る程度の記載をすることなどにより,当該用途の有用性及びそのための当該医薬の有効量を裏付ける記載を要するものと解するのが相当である。
本件発明1及び2の特許請求の範囲においては,本件化合物が「痛みの処置における」(構成要件1B)「鎮痛剤」(構成要件1C)及び「鎮痛剤」(構成要件2C)として作用することが記載されているところ,いずれも本件化合物の鎮痛効果が認められる痛みは特定されていない。
しかし,本件明細書には,本件化合物について,「痛みの処置とくに慢性の疼痛性障害の処置における使用方法である。このような障害にはそれらに限定されるものではないが炎症性疼痛,術後疼痛,転移癌に伴う骨関節炎の痛み,三叉神経痛,急性疱疹性および治療後神経痛,糖尿病性神経障害,カウザルギー,上腕神経叢捻除,後頭部神経痛,反射交感神経ジストロフィー,線維筋痛症,痛風,幻想肢痛,火傷痛ならびに他の形態の神経痛,神経障害および特発性疼痛症候群が包含される。」・・・と記載されていることに照らすと,本件発明1及び2は,本件化合物が少なくとも上記各痛みに対して鎮痛効果を有することを内容とするものと解される。
したがって,本件発明1及び2について実施可能要件を満たすというためには,本件明細書の発明の詳細な説明に,薬理データの記載又はこれと同視し得る程度の記載をすることなどにより,上記各痛みに対して鎮痛効果があること及びそのための当該医薬の有効量を裏付ける記載が必要であるというべきである。」
イ 本件発明1及び2は実施可能要件に違反する
そして、裁判所は、痛みの分類及び機序についての本件出願当時の技術常識及びホルマリン試験・カラゲニン試験・術後疼痛試験についての本件明細書の記載等によれば、以下のとおり本件発明1及び2は実施可能要件に違反すると判断した。
「本件明細書の発明の詳細な説明においては,ホルマリン試験,カラゲニン試験及び術後疼痛試験の各薬理データの記載により,本件化合物が侵害受容性疼痛に分類される痛みに対して鎮痛効果があること及びそのための当該医薬の有効量が裏付けられているものの,本件発明1及び2がその内容とする「痛み」,すなわち,少なくとも「炎症性疼痛,術後疼痛,転移癌に伴う骨関節炎の痛み,三叉神経痛,急性疱疹性および治療後神経痛,糖尿病性神経障害,カウザルギー,上腕神経叢捻除,後頭部神経痛,反射交感神経ジストロフィー,線維筋痛症,痛風,幻想肢痛,火傷痛ならびに他の形態の神経痛,神経障害および特発性疼痛症候群」・・・の各痛みに対して鎮痛効果があること及びそのための当該医薬の有効量を裏付ける記載がないから,本件発明1及び2は,実施可能要件に違反する。」
(2)本件発明1及び2のサポート要件違反の成否
ア サポート要件違反の判断基準について
裁判所は、サポート要件を満たすための基準を以下のとおり判示した。
「特許請求の範囲の記載が明細書のサポート要件(法36条6項1号)に適合するか否かは,特許請求の範囲の記載と発明の詳細な説明の記載とを対比し,特許請求の範囲に記載された発明が,発明の詳細な説明に記載された発明で,発明の詳細な説明の記載により当業者が当該発明の課題を解決できると認識できる範囲のものであるか否か,また,その記載や示唆がなくとも当業者が出願時の技術常識に照らし当該発明の課題を解決できると認識できる範囲のものであるか否かを検討して判断すべきものである。」
イ 本件発明1及び2はサポート要件に違反する
「前記・・・のとおり,本件明細書の発明の詳細な説明には,本件化合物について,上記各痛みのうち,侵害受容性疼痛に分類される痛みに対して鎮痛効果があることの記載はあるものの,その余の痛みに対して鎮痛効果があることについての記載があるとは認められない。
したがって,本件明細書の発明の詳細な説明の記載は,当業者が,本件発明1及び2の上記課題の解決,すなわち少なくとも上記各痛みの全てに対して鎮痛効果を有することを認識できる範囲のものとはいえず,また,当業者が本件出願当時の技術常識に照らして上記各痛みに対して鎮痛効果を有することを認識できる範囲のものともいえないから,本件発明1及び2は,サポート要件に違反する。」
ウ 原告の反論
原告は、「サポート要件を充足するといえるためには,明細書に接した当業者が技術常識も踏まえて課題が解決できるであろうとの合理的期待が得られれば足り,明細書に基づき追試や分析をすることによって更なる技術の発展に資することができれば足りる」と主張した。
しかし、裁判所は、以下のとおり原告の主張は採用することができないと判断した。
「明細書は,発明の技術内容を一般に開示するとともに,特許権として成立した後にその効力の及ぶ範囲(特許発明の技術的範囲)を明らかにするという役割を有するものであるから,サポート要件に適合するというためには,前記アのとおり,特許請求の範囲に記載された発明が,発明の詳細な説明に記載された発明で,発明の詳細な説明の記載により当業者が当該発明の課題を解決できると認識できる範囲のものであるか,その記載や示唆がなくとも当業者が出願時の技術常識に照らし当該発明の課題を解決できると認識できる範囲のものである必要があるというべきである。
そして,前記イのとおり,本件明細書に接した当業者は,本件出願当時の技術常識を踏まえても,本件発明1及び2で鎮痛効果を有するとされる各痛みに対して鎮痛効果を生じると認識することができたとはいえない。」
(3)本件発明1及び2の訂正の再抗弁
ア 請求項2に係る本件訂正について
裁判所は、請求項2に係る本件訂正のうち、「鎮痛剤」を「神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛みの処置における鎮痛剤」と訂正する点については、形式上は、特許請求の範囲を減縮するものといえるとしながらも、以下のとおり新規事項を追加するものであるとして、訂正要件を満たすとは認められないと判断した。
「前記・・・のとおり,本件明細書の発明の詳細な説明には,本件化合物について,侵害受容性疼痛に対して鎮痛効果があること及びそのための当該医薬の有効量を裏付ける記載があるものの,その他の痛みに対して鎮痛効果があることなどを裏付ける記載があるとはいえない。そして,前記・・・によれば,「神経障害又は線維筋痛症による,痛覚過敏又は接触異痛の痛み」とは,侵害受容性疼痛ではなく,神経障害性疼痛又は心因性疼痛に分類されるものである。
したがって,上記訂正は,神経障害性疼痛又は心因性疼痛の処置における鎮痛剤という新規事項を追加するものであって,本件明細書に記載した事項の範囲内においてされたものではないので,訂正要件を満たすとは認められない(法134条の2第9項,126条5項)。」
イ 請求項1に係る本件訂正について
「本件訂正前の請求項2は請求項1を引用しており,これらは一群の請求項を構成する。そして,請求項2に係る本件訂正は,当該請求項についての訂正が認められるときは請求項1とは別の訂正単位として扱われることを求めるものである。しかし,前記アのとおり,請求項2に係る本件訂正は認められないから,請求項1と請求項2は依然として一群の請求項を構成していることになり,請求項1に係る本件訂正も認められない(法134条の2第3項)。」
(4)本件発明1及び2について(小括)
裁判所は、以上によれば、その余の点を判断するまでもなく、本件発明1及び2については、実施可能要件違反及びサポート要件違反が認められるから、無効の抗弁は理由があり、請求項1及び請求項2に係る本件訂正は訂正要件に違反するものであるから、訂正の再抗弁は理由がない、と判断し、したがって、延長登録により存続期間が延長された本件特許権の効力が被告医薬品に及ぶか否かにかかわらず、原告の被告に対する本件発明1及び2に基づく被告医薬品の製造、販売及び販売の申出の差止請求並びに被告医薬品の廃棄請求は、いずれも理由がない、と判断した。
(5)被告医薬品が本件発明3及び4の技術的範囲に属するか
裁判所は、効能又は効果を「神経障害性疼痛・線維筋痛症に伴う疼痛」として承認を受けた被告医薬品は、本件発明3及び4の各技術的範囲に属するとは認められないから、その余の点について判断するまでもなく、被告医薬品が本件特許権を侵害するとは認められないと判断した。
ア 文言侵害の成否
裁判所は、前記前提事実のとおり、被告医薬品は、効能・効果を「神経障害性疼痛及び線維筋痛症に伴う疼痛」とする疼痛治療剤であり、「炎症を原因とする痛み」及び「手術を原因とする痛み」の鎮痛剤であるとは認められないから、「炎症を原因とする痛み」及び「手術を原因とする痛み」(本件発明3の構成要件3B)又は「炎症性疼痛による痛覚過敏の痛み,又は術後疼痛による痛覚過敏若しくは接触異痛の痛みの処置における」(本件発明4の構成要件4B)を充足するとは認められない、と判断した。
「本件発明3に係る特許請求の範囲及び本件明細書の記載を総合すると,構成要件3Bの「炎症を原因とする痛み」及び「手術を原因とする痛み」とは,それぞれ本件明細書における「炎症性疼痛」及び「術後疼痛」を意味するものと理解できる。
そして・・・ホルマリン試験,カラゲニン試験及び術後疼痛試験は侵害受容性疼痛としての痛覚過敏,接触異痛等に対する鎮痛効果を検証するための試験であることが本件出願当時の技術常識であったから,本件明細書において動物モデル試験により本件化合物の鎮痛効果が検証されたのは,侵害受容性疼痛のみであったと理解できる。
さらに,・・・本件審決予告において,痛みには本件訂正前発明4記載の各痛みを含む種々のものがあり,鎮痛剤であればあらゆる種類の痛みに有効であるというわけではないところ,本件明細書からは,「炎症性疼痛」及び「術後疼痛」以外の本件訂正前発明4記載の各痛みに対して鎮痛効果を有することを認識することはできないと指摘されたことを受けて,原告は,本件訂正を行い,鎮痛剤の処置対象となる痛みを,本件審決予告において実施可能要件及びサポート要件を満たすと判断された「炎症を原因とする痛み(炎症性疼痛)」及び「手術を原因とする痛み(術後疼痛)」に限定したと説明したものである。
以上の本件発明3に係る特許請求の範囲及び本件明細書の記載の解釈並びに本件訂正の経緯等によれば,構成要件3Bの「炎症を原因とする痛み」及び「手術を原因とする痛み」とは,侵害受容性疼痛である炎症性疼痛及び術後疼痛を意味し,これら以外の痛みを含むものではないと解するのが相当である。
・・・構成要件4Bの「炎症性疼痛」及び「術後疼痛」とは,構成要件3Bの「炎症を原因とする痛み」及び「手術を原因とする痛み」と同様に,侵害受容性疼痛である炎症性疼痛及び術後疼痛を意味し,本件訂正前発明4記載の「神経障害による痛み」及び「線維筋痛症」は含まないと解するのが相当である。」
イ 均等侵害の成否
裁判所は、以下のとおり、被告医薬品は、均等の第1及び5要件を満たさず、本件発明3及び4の構成と均等なものとは認められないと判断した。
「いかなる痛みに対して鎮痛効果を有するかは,本件発明3において本質的部分というべきであり,その鎮痛効果の対象を異にする被告医薬品は,本件発明3の本質的部分を備えているものと認めることはできない。したがって,本件発明3に係る特許請求の範囲に記載された構成中の被告医薬品と異なる部分が本件発明3の本質的部分でないということはできないから,被告医薬品は均等の第1要件を満たさない。
また,・・・原告は,本件訂正前発明3においては鎮痛の対象となる痛みを限定していなかったところ,本件訂正により「炎症を原因とする痛み」及び「手術を原因とする痛み」に限定していることからすると,本件発明3との関係においては,被告医薬品の効能・効果である神経障害性疼痛及び線維筋痛症に伴う疼痛を意図的に除外したと認めるのが相当である。
したがって,被告医薬品は均等の第5要件も満たさない。
以上によれば,被告医薬品は,本件発明3の特許請求の範囲に記載された構成と均等なものとは認められない。
・・・同様に,・・・被告医薬品は,本件発明4の特許請求の範囲に記載された構成と均等なものとは認められない。」
4.コメント
(1)医薬用途発明について記載要件を満たすために必要とされる明細書への記載の程度とは
本件において、裁判所は、医薬用途発明に係る出願において、明細書に医薬用途(例えば、疾患名)を記載しただけで、薬理試験結果又はこれと同視し得る程度の記載や出願当時の技術常識といった当該疾患に有用であるとの裏付けが無い場合には、実施可能要件違反となり、さらには、その記載だけでは当業者が当該発明の課題を解決できると認識できるものとは認められないことになりサポート要件違反ともなる、と判断した。
薬剤の開発疾患でその薬剤候補が有用性を示すのかどうかを評価するための動物モデルは、その疾患を完璧に再現できているということは少なく、ある程度のサイエンスの合理性と推測を頼りに疾患モデルを選択・評価し、適応症の広がりの可能性も検討していくことになることが多いのが実情だろう。
そして、サイエンスを厳格に突き詰めれば、特定の疾患ひとつひとつにおいてもさらに病態・病因・患者背景などいくらでも細分化できるのであり、そのような際限もない分類をつまみ上げて、明細書にそのデータの裏付けが足りないからデータが必要だ、記載が必要だ、と極論することは妥当ではなく、一定の技術常識と一定の合理的な期待に基づいて試験結果から一定の適用範囲の広がりを解釈・判断することが妥当であろう。
その意味で技術常識の把握は非常に重要となる。
薬理試験結果を得た場合に、その結果から医薬用途発明をどの疾患の範囲まで・どの深さまで明細書に記載し、権利化に向けて追求するかという問題は悩めば悩むほど技術常識という沼に落ちるかもしれない。
医薬用途発明について実施可能要件を満たすために必要とされる明細書の記載の程度とは?との問いに対して、「薬理データの記載又はこれと同視し得る程度の記載」ときれいに答えをまとめることはできても、実際の個々の疾患分野でその境界線をはっきりと引くことは難しく、争いとなったら、結局は技術常識の裏付けをどれだけ主張できるるかが勝敗の分かれ目となるとしか答えようがないだろう。
これまで、医薬用途発明について明細書の記載の程度が問題となり、実施可能要件が争われた事件は種々あるが(記事「記載要件/引例適格/データは必要か」1.(2)参照)、特に、本件のように、技術常識を踏まえても明細書に記載された薬理試験結果がその医薬用途発明(疾患への有用性)への範囲までは裏付けられていないとされた典型的な事件を以下に例示する。


一方、医薬用途発明についてのサポート要件を検討するうえでは、いわゆる「フリバンセリン事件」判決も念頭において、実施可能要件とは区別して考えなければならないだろう。
本判決では、形式的には明細書にその痛みに有用である旨の記述はあるものの効果の裏付けがなかったことから、「効果を有するとされる各痛みに対して鎮痛効果を生じると認識することができたとはいえない」、「当該発明の課題を解決できると認識できる範囲のもの」とはいえないと判断された。
本判決は「フリバンセリン事件」判決の考え方よりもサポート要件について厳しい方向に振れているように感じる。
また、当然のことながら、疾患の理解とサイエンスが進歩し、実施可能な疾患の裏付けが広がる又は深まる可能性はあるだろうし、実は有効ではないことが後になって判明して実施可能性の範囲は狭まる場合もあるかもしれないが、判断基準は、「出願当時」の当業者・技術常識目線である。
本件で、原告は、明細書に記載された各薬理試験についての専門家からの意見書を提出したが、裁判所は、いずれも本件出願後に作成されたものであり、それら主張された医薬用途を裏付ける得る出願当時の技術常識に関する文献が存在するとは認められないことに変わりはないから、それら意見書に基づく原告の主要を採用することはなかった。
(2)特許権侵害訴訟の行方
本件において、裁判所は、特許請求の範囲の記載の意義を明細書の記載(特許法第70条2項)及び技術常識に基づいたその解釈並びに本件訂正の経緯等を参酌することによって、効能・効果を「神経障害性疼痛及び線維筋痛症に伴う疼痛」とする被告医薬品は、本件発明の構成要件を充足せず、また、均等の第1及び5要件を満たさず本件発明の構成と均等なものとも認められないとして、本件発明の技術的範囲には属しないと判断した。
すなわち、この判断は本件特許権がファイザーのリリカ®自体も保護しないことを意味する。
本事件について、原告は、本件判決を不服として知財高裁に控訴したのかどうかは定かでないが、本件特許の無効審決の取消しを求める審決取消訴訟(知財高裁令和2年(行ケ)第10135号)を提起しており、その判決言渡期日が2022年2月9日3月7日に控えている。
2022年2月9日3月7日の知財高裁の判決により、この事件がさらに混沌へと向かうのか、それとも決着へ向かうのか・・・見守りたい。
5.おわりに
仮に、ファイザーの主張するとおり、リリカ®のジェネリックの販売行為が本件特許権の侵害に当たるとの判決に至っていれば、リリカ®の全てのジェネリックの供給は違法となり停止せざるを得なくなる可能性もあったわけで、医薬品の安定供給に混乱を生じかねなかった。
ひとまずそうならなかったことは喜ばしいことであるが、特許権侵害に該当(医薬品の安定供給が混乱)するおそれがあったにもかかわらずジェネリックを承認した厚生労働省のパテントリンケージの運用がこのまま改善されずに放置されたままで良いのかという問題は依然として残り続ける。

コメント
【追記】
「リリカ」®の後発医薬品差止請求に対する判決が多数出されているとのことで、裁判所ホームページに今後掲載されると思われるとのことです。小林化工だけではありませんでした。ジェネリックが販売されている状況で先発側が妥協できる和解や取下げはやはりそもそもあり得なかったということか・・・。
2022.02.08 窪田法律事務所 note: 東京地裁が疼痛治療剤「リリカ」®の後発医薬品の差止請求を棄却
https://note.com/kubota_law/n/n324609fbbbf5