エビリファイ®はアリピプラゾール(aripiprazole)を有効成分とする抗精神病薬であり、日本では「統合失調症」の効能・効果で2006年1月に製造販売承認を取得した。世界での売上は 2014年度には6,542億円(そのうち米国は5,225億円)に達し、大塚ホールディングス株式会社の連結売上高の約4割を占めた。現在は、ジェネリックの参入により売り上げは落ち込んでいるが(米国では、2015年4月にジェネリックが承認、2015年度売上は前年比で約60%減少)、エビリファイ®(錠・OD錠・散・内用液)の新剤形として月1回投与によりコンプライアンスを向上させたアリピプラゾール持続性注射剤(月1回製剤)「エビリファイメンテナ」が好調に売り上げを伸ばしている。
エビリファイ®について、日本でも2017年2月にジェネリックが初承認され、エビリファイ®の売上は落ち込んでいるが、再審査期間及び用途特許が存在していることから、エビリファイ®とジェネリックとの間で、さらにジェネリックの中でも沢井製薬と他のジェネリックメーカーとの間で、効能・効果が異なる状況にある。沢井製薬が「統合失調症」に加え、「双極性障害における躁症状」及び「うつ病・うつ状態(既存治療で十分な効果が認められていない場合に限る)」の効能・効果追加承認を得て、他のジェネリックメーカー(「統合失調症」のみ)を出し抜いている状況である。以下に、現在の日本におけるエビリファイⓇの用途特許を巡るジェネリックメーカーの動きをまとめた。
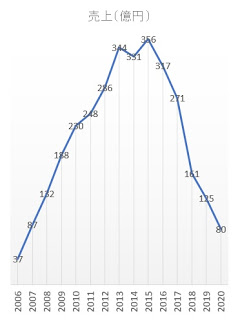
1.エビリファイ®の日本での売上推移(億円)(大塚ホールディングス決算補足資料
ファクトブックより)
2006年度: 37(エビリファイⓇ承認)
2007年度: 87
2008年度: 132
2009年度: 188
2010年度: 230
2011年度: 248
2012年度: 286
2013年度: 344
2014年度: 331(昨年度末の消費税増税前需要増加による一時的売上増の反動の影響で前期比で減少)
2015年度: 356
2016年度: 317(薬価改定において市場拡大再算定の適用を受けた影響で前期比で減少)
2017年度: 271(ジェネリック初承認「統合失調症」)
2018年度: 161(沢井が「双極性障害における躁症状」追加承認)
2019年度: 125(沢井が「うつ病・うつ状態」追加承認)
2020年度: 80(計画)
2.大塚製薬が保有する用途特許(日本特許第4178032号)の現状
エビリファイ®の特定の効能・効果(「双極性障害における躁症状」、「うつ病・うつ状態(既存治療で十分な効果が認められていない場合に限る)」)を保護している、大塚製薬が保有する用途特許(日本特許第4178032号、2022年1月29日満了(さらに存続期間延長登録あり))が、複数のジェネリックメーカーからそれぞれ特許無効審判を請求されている(無効2018-800113; 無効2018-800123; 無効2018-800127; 無効2018-800130)。特許無効審判を請求しているのは、共和薬品工業、ニプロ、東和、Meiji Seikaファルマ。これらメーカーのジェネリックは「統合失調症」のみを効能・効果とするいわゆる「虫食い」であり、上記特許の無効審決を得て、効能・効果の追加承認を得ようと試みていると思われる。
上記特許無効審判の審理は昨年11月28日に審決の予告に至った。しかし、その内容は、「双極性障害」に関する用途発明に係る請求項1、4、5は無効とするが、「鬱病」に関する用途発明に係る請求項2については請求不成立とするものだったため、ジェネリックメーカー側にとっては喜ばしい結果といえるものではなかった。しかも、2020年2月7日には特許権者が訂正請求書を提出したようであり、審理はしばらく続くと思われ、特許は有効に存続しつづけている。
3.本件用途特許で保護されるアリピプラゾール製剤の効能・効果
下記表1に、本件用途特許(第4178032号)の請求項1と、エビリファイ®及びジェネリックの現在の効能・効果を対比した。赤字が本件特許で保護されている効能・効果である。現在、大塚製薬の本件用途特許が有効に存在しているにもかかわらず、なぜ、沢井製薬が本件特許でカバーされている効能・効果でジェネリックを販売できているのかについては後述する。
表1 本件用途特許(第4178032号)請求項1、エビリファイ®、ジェネリックの対比
|
構成
|
請求項1
|
エビリファイⓇ
|
沢井のジェネリック
|
共和、ニプロ、東和、MeijiSeikaファルマのジェネリック
|
|
1
|
鬱病、・・・
躁、・・・
特定できない症状の発現を有する双極性I型障害・・・
及び
循環型を有する双極性II型障害
からなる群から選ばれた
5-HT1A受容体サブタイプに関連した中枢神経系の障害
|
・統合失調症
・双極性障害における躁症状
・うつ病・うつ状態(既存治療で十分な効果が認められない場合に限る)
・小児期の自閉スペクトラム症に伴う易刺激性
|
・統合失調症
・双極性障害における躁症状
・うつ病・うつ状態(既存治療で十分な効果が認められない場合に限る)
|
・統合失調症
|
|
2
|
を治療するための医薬組成物であって、式(1)・・・のカルボスチリル化合物、及び医薬として許容される塩又は溶媒和物の治療有効量を含む医薬組成物。
|
を治療するための医薬組成物であって、アリピプラゾールの治療有効量を含む医薬組成物。
|
を治療するための医薬組成物であって、アリピプラゾールの治療有効量を含む医薬組成物。
|
を治療するための医薬組成物であって、アリピプラゾールの治療有効量を含む医薬組成物。
|
4.各ジェネリックメーカーの動き(無効審判請求と効能・効果追加承認のタイミング)
エビリファイ®の再審査期間のうち、「統合失調症」及び「双極性障害における躁症状」については2006年1月23日~2016年1月22日、「うつ病・うつ状態(既存治療で十分な効果が認められていない場合に限る)」については2013年6月14日~2017年6月13日である。前者の再審査期間終了を待って2017年2月15日に初承認されたジェネリックは、いずれも効能・効果が「統合失調症」のみの「虫食い」であった。「うつ病・うつ状態」は再審査期間中であり、「双極性障害における躁症状の改善」は同効能・効果を保護する上記用途特許が有効に存続していたため承認されなかったと考えられる(いわゆる「パテントリンケージ」(註1))。
註1: 厚生労働省は「医療用後発医薬品の薬事法上の承認審査及び薬価収載に係る医薬品特許の取扱いについて(平成21年6月5日付け医政経発第0605001号/薬食審査発第0605014号)」及び「承認審査に係る医薬品特許情報の取扱いについて(平成6年10月4日付け薬審第762号審査課長通知)」において、後発医薬品の薬事法上の承認審査にあたっては、先発医薬品の一部の効能・効果等に特許が存在する効能・効果等については承認しない方針であり、特許の存否は承認予定日で判断するものであることとしている。
このジェネリックの初承認時(2017年2月15日)の効能・効果は、沢井製薬も他のジェネリックメーカーと同じく「統合失調症」のみであった(下記表2を参照。ピンク色部分はジェネリックが実質申請できない再審査期間。)。
表2 特許無効審判請求とジェネリックの効能・効果追加承認のタイミング
|
大塚の動き
|
沢井の動き
|
共和、ニプロ、東和、MeijiSeikaファルマの動き
|
|||||
|
エビリファイⓇ承認・再審査期間
|
特許第4178032の経過
|
||||||
|
統合失調症
|
双極性障害における躁症状
|
うつ病・うつ状態
|
小児期の自閉スペクトラム症に伴う易刺激性
|
||||
|
2006
|
1/23承認
|
||||||
|
2008
|
8/29登録
|
||||||
|
2012
|
1/18承認
|
||||||
|
2013
|
6/14承認
|
||||||
|
2016
|
~1/22再審査期間
|
~1/22再審査期間
|
|||||
|
9/28承認
|
|||||||
|
2017
|
2/15「統合失調症」承認
|
2/15「統合失調症」承認
|
|||||
|
3/6特許無効審判請求
|
|||||||
|
~6/13再審査期間
|
|||||||
|
2018
|
3/29審決予告
|
||||||
|
7/9無効審判請求取下
|
|||||||
|
8/21訂正審判請求
|
|||||||
|
9/5「双極性障害における躁症状」承認
|
|||||||
|
9/7共和が特許無効審判請求
|
|||||||
|
10/18ニプロが特許無効審判請求
|
|||||||
|
10/19東和が特許無効審判請求
|
|||||||
|
11/12MeijiSeikaファルマが特許無効審判請求
|
|||||||
|
11/14訂正審決
|
|||||||
|
2019
|
3/6「うつ病・うつ状態」承認
|
||||||
|
11/28審決予告
|
|||||||
|
2020
|
~9/27再審査期間
|
||||||
|
2022
|
1/29特許期間満了(20年)
|
||||||
2017年3月6日、沢井製薬は、共和薬品工業、ニプロ、東和、Meiji Seikaファルマよりも先んじて、上記用途特許の無効審判を請求し(無効2017-800030)、2018年7月9日に請求を取下げている。沢井製薬は、その後タイミングよく、2018年9月5日に「双極性障害における躁症状」の追加承認(「うつ病・うつ状態(既存治療で十分な効果が認められていない場合に限る)」も2019年3月6日に追加承認)を得ていることから、大塚製薬から上記効能・効果に関する実施許諾を得たのではないかと推測される。沢井製薬が有利な審決の予告(この時は、「双極性障害」に関する用途発明に係る請求項だけでなく、「鬱病」に関する用途発明に係る請求項も無効とするものであった!)を得ていたのにもかかわらず無効審判請求を取下げたのは、沢井製薬にとっては先発品と同じ効能効果を他のジェネリックメーカーに先駆けて追加したいことと、大塚製薬にとっては特許無効審決となった結果多くのジェネリックメーカーにより先発品と同じ効能効果が追加されてしまうよりも沢井製薬だけにまずは留めておきたいという思惑、とが一致したのかもしれない。ジェネリックの中で、現在、上記効能・効果の追加承認を得ているのは沢井製薬だけであり、共和薬品工業、ニプロ、東和、Meiji Seikaファルマ等の他のジェネリックメーカーは、効能・効果の点で沢井製薬に先を越された状況となっている。
5.沢井製薬の無効審判請求のタイミングについての考察
効能・効果「うつ病・うつ状態」についてのジェネリックの承認申請が可能となるのは、その再審査期間終了日である2017年6月13日経過後であり、そこから承認審査に約1年を要すると見積もると、その間にいわゆる「パテントリンケージ」を解決できていれば、遅くとも2018年半ばには同効能・効果の追加承認を得られると想定される。無効審判請求から無効審決まで約1年半と見積もると、2017年初めには無効審判を請求しておきたいところである。実際に、沢井製薬は2017年3月に特許無効審判を請求していることから、上記見立てのタイミングとの辻褄は合う。
効能・効果「双極性障害における躁症状」についてジェネリックの承認申請が可能となるのは、「統合失調症」と同じく、その再審査期間終了日である2016年1月22日経過後であり、本件用途特許が存在しなければ(無効審決を得ていたとしたら)2017年2月15日のタイミングで「統合失調症」と共に「双極性障害における躁症状」も承認を得られたはずである。しかし、沢井製薬はそのタイミング前には本件用途特許に対して無効審判を請求していなかった。
沢井製薬が「双極性障害における躁症状」についての承認取得に重点を置いていたのであれば、2017年2月15日のタイミングで「統合失調症」とともに「双極性障害における躁症状」の承認も目指して、2015年中には無効審判を請求していただろう。しかし実際は、2017年3月に無効審判請求しており、そのタイミングは「うつ病・うつ状態」についての承認を目指したタイミングと辻褄が合っている。そして、無効審判請求をしたのは沢井製薬だけであり、他のジェネリックメーカーの参加も無かったことから、無効審判の審理と共に特許権者との和解交渉をコントロールし易かったと想像される。「双極性障害における躁症状」の効能効果追加承認から6カ月遅れて「うつ病・うつ状態」の効能効果追加承認に至ったのは、沢井製薬自身の事情か、PMDAの審査上の事情か、大塚製薬と交わしたかもしれない和解契約の条件なのかは定かではない。
6.今後の見通し
前述の通り、本件用途特許の無効審判の審理は昨年11月28日に審決の予告に至った。しかし、その内容は、「双極性障害」に関する用途発明は無効、「鬱病」に関する用途発明は請求不成立とするものであり、2020年2月7日には特許権者が訂正請求書を提出したようであることから、審理はしばらく続く。訂正請求の審理を経て審決予告通り「双極性障害」に関する用途発明を無効とする審決に至るのであれば、各ジェネリックメーカーは「双極性障害における躁症状」の効能効果追加承認を得ることができるだろう(早ければ2020年内か)。審決予告通りの審決となれば、一方の「鬱病」に関する用途発明は有効に存続することになり、審決取消訴訟に発展したとしても「鬱病」に関する用途発明の無効をジェネリックメーカーが勝ち取れるかどうかは不透明であり、仮に審決取消判決を勝ち取って「無効」審決に至るとしてもさらに年月を要するだろう。従って、沢井製薬以外の各ジェネリックメーカーは「うつ病・うつ状態」の効能効果追加承認を、その特許存続期間満了(特許期間延長分を含めて2026年8月)まで待たざるを得ないという可能性はあり得る。ジェネリックの中でいち早く「双極性障害における躁症状」及び「うつ病・うつ状態」の効能効果追加承認の取得に成功した沢井製薬の競争優位な状況はしばらく続きそうである。
本件用途特許(第4178032号。20年の特許満了日は2022年1月29日)における存続期間延長登録による延長期間:
- 「双極性障害における躁症状の改善」の特許期間延長: +3年4月19日
- 「うつ病・うつ状態(既存治療で十分な効果が認められない場合に限る)」の特許期間延長: +4年6月3日
7.参考:
- 2013.06.14 大塚製薬 press release: うつ病治療の新たな選択肢「エビリファイ®」が抗精神病薬としてうつ病・うつ状態の効能追加の承認取得
- 2019.08.03 記事 エビリファイ®用途特許を巡るジェネリックメーカーの動き



コメント
【追記】
特許第4178032号の訂正後の請求項2に係る発明(鬱病用途)についての審判請求は成り立たないとの審決(無効2018-800113, -800123, -800127, -800130)。審決日2020.05.12。
【追記】
「双極性障害における躁症状の改善に対する効能・効果」は特許第4178032号の無効審決受けて承認へ。「鬱」は請求不成立審決のため未だ効能効果追加されずか・・・
・2020.07.22 Meiji Seikaファルマ press release: 抗精神病薬「アリピプラゾール『明治』」「効能・効果」および「用法・用量」の追加承認取得に関するお知らせ
https://www.meiji-seika-pharma.co.jp/pressrelease/2020/detail/200722_02.html
・2020.07.22 日医工 press release: アリピプラゾール錠3mg/6mg/12mg「日医工」アリピプラゾールOD錠3mg/6mg/12mg/24mg「日医工」アリピプラゾール散1%「日医工」双極性障害における躁症状の改善に対する効能・効果および用法・用量追加のお知らせ
https://www.nichiiko.co.jp/company/press/detail/4901/1117/4541_20200722_01.pdf
・2020年7月改訂(第6版)ニプロ アリピプラゾール錠3mg「ニプロ」医薬品インタビュ-フォーム」より: 「2020年7月には、「双極性障害における躁症状の改善」に対する「効能・効果」、「用法・用量」が追加承認された。」
審決(無効2018-800113, -800123, -800127, -800130)に対して取消訴訟提起(6/24又は6/25)⇒令和2年(行ケ)10077, 10078, 10079, 10080, 10081, 10082, 10083