2020年2月17日、非ステロイド性消炎・鎮痛剤(COX-2選択的阻害剤)セレコックス(Celecox)®錠のジェネリックが初承認となりました(20社40品目)。20社のジェネリックの中には、ファイザーのセレコキシブ「ファイザー」があり、これはオーソライズド・ジェネリック(AG)のようです。
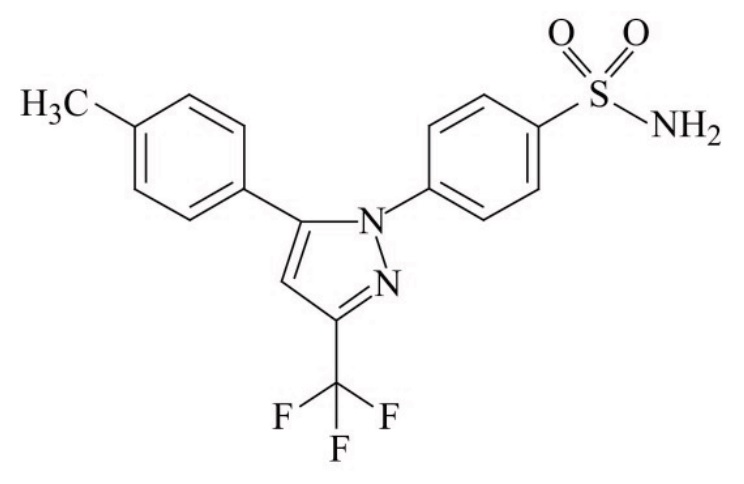
有効成分であるセレコキシブは、1992 年に米国サール社(現 米国ファイザー社)で合成されました。日本では、1996 年4月から山之内製薬(現 アステラス製薬)と日本モンサント(現 ファイザー)が共同開発を実施し、2007年1月26日に「関節リウマチ、変形性関節症」を効能・効果としてアステラス製薬がセレコックス®錠の製造販売承認を取得しました(販売提携 ファイザー)。2009年6月17日には「腰痛症、肩関節周囲炎、頸肩腕症候群、腱・腱鞘炎」、さらに2011年12月22日には、「手術後、外傷後並びに抜歯後の消炎・鎮痛」の効能・効果が追加承認されました。
再審査期間は、「関節リウマチ、変形性関節症」については、2007年1月26日~2015年1月25日(8年間)、「腰痛症、肩関節周囲炎、頸肩腕症候群、腱・腱鞘」及び「手術後、外傷後並びに抜歯後の消炎・鎮痛」についても、「関節リウマチ、変形性関節症」の残余期間(2015年1月25日)までということで、再審査期間が終了した2015年以降、セレコックス®錠の市場独占性は特許によって守られていました。
しかし、2019年11月14日に、セレコックス®錠を保護する物質特許は満了したことから(偶然にも、組成物特許の無効理由を認める判決も同日付で出された)、2020年2月にはジェネリックの承認がされると推測されていました(2019.11.14 「東和薬品・日本ケミファ・ヘキサル v. ジー.ディー.サール」 知財高裁平成30年(行ケ)10110; 10112; 10155)。
- 物質特許(第3025017号)・・・2019年11月14日に延長存続期間(5年間)満了。
- 組成物特許(第3563036号)・・・20年の存続期間満了日は2019年11月30日、期間延長登録により、「関節リウマチ、変形性関節症」については2022年6月26日、「腰痛症、肩関節周囲炎、頸肩腕症候群、腱・腱鞘炎」及び「手術後、外傷後並びに抜歯後の消炎・鎮痛」については2024年11月30日が満了日だった。しかし、本件特許に対する無効審判(無効2016-800112号)の請求不成立審決とされた部分は取り消されるべき(サポート要件に適合しない)とした2019年11月14日付の知財高裁判決(2019.11.14 「東和薬品・日本ケミファ・ヘキサル v. ジー.ディー.サール」 知財高裁平成30年(行ケ)10110; 10112; 10155)がだされていた。

コメント
2020.03.16 ファイザー株式会社 press release: 「ファイザー、セレコキシブ錠でAG市場に参入
先発医薬品と同一の品質を有する医薬品で治療する選択肢を提供し、増大するNCDの負担軽減に貢献」
https://www.pfizer.co.jp/pfizer/company/press/2020/2020_03_16.html
【追記】
2020.06.19 ファイザー press release: セレコキシブ錠100mg「ファイザー」、同200mg「ファイザー」発売
~ファイザー初のAGで社会と患者さんが負うNCDの負担軽減に貢献~
https://www.pfizer.co.jp/pfizer/company/press/2020/2020_06_19.html