マーデュオックス®軟膏の差止請求訴訟: 東京地裁平成28年(ワ)14131
【背景】
原告(レオ ファーマ)が保有する「医薬組成物」に関する特許権(第5886999号)を侵害すると主張して、被告ら(製造販売元である中外製薬及び販売会社であるマルホ)に対して被告物件(尋常性乾癬治療剤「マーデュオックス®軟膏」)の生産等の差止め及び廃棄を求めた事案。
請求項1:
ヒトまたは他の哺乳動物において乾癬を処置するための皮膚用の非水性医薬組成物であって,マキサカルシトールからなる第1の薬理学的活性成分A,およびベタメタゾンまたは薬学的に受容可能なそのエステルからなる第2の薬理学的活性成分B,ならびに少なくとも1つの薬学的に受容可能なキャリア,溶媒または希釈剤を含む,医薬組成物。
請求項11:
ヒトの乾癬を処置するための,請求項1~10のいずれか1項に記載の組成物
請求項12:
医学的有効量で1日1回局所適用される,請求項11に記載の組成物
【要旨】
本件発明12は本件優先日における公知文献に記載された発明に基づいて当業者が容易に発明をすることができたものであり、そして、本件発明12に従属している他のいずれの発明も同様に当業者が容易に発明をすることができたものである。
したがって、本件発明1ないし4、11及び12に係る本件特許には、特許法29条2項違反の無効理由があるから、原告は上記各発明に係る本件特許権を行使することができない。
よってその余の点について検討するまでもなく、原告の請求はいずれも理由がない。
請求棄却。
相違点に係る容易想到性についての判決抜粋:
「乙15発明は,「ヒトにおいて乾癬を処置するために皮膚に塗布するための混合物であって,1α,24-dihydroxycholecalciferol(タカルシトール),およびBMV(ベタメタゾン吉草酸エステル),ならびにワセリンとを含有する非水性混合物であり,皮膚に1日2回塗布するもの」というものである。そして,乙16及び17に開示されているように,本件優先日において,乾癬治療剤としてのマキサカルシトールの軟膏が既に知られていたのであるから,当業者であれば,乾癬を処置するための混合物である乙15発明において,ビタミンD3の類似体からなるタカルシトールに代えて,同じくビタミンD3の類似体からなるマキサカルシトールを使用する程度のことは,容易に想到できることというべきである。
・・・乙24及び25に開示されているように,本件優先日において,タカルシトール軟膏が1日1回の用法で乾癬処置に使用されることも既に知られていたのであるし,そもそも塗布方式(1日1回か,2回か)の検討は,治療効果の向上や,副作用の低減等の観点から,当業者が適宜行うことにすぎないことであるから,当業者であれば,乙15発明において,塗布の回数を1日1回とする程度のことは,容易に想到できることというべきである。」
相違点に係る顕著な作用効果についての判決抜粋:
「・・・乙15に開示されている治療効果は,本件明細書に開示された本件発明12における有効な斑治癒の効果と実質的に変わらないというべきである。
なお,原告は,本件発明12の治療効果に関して,甲10及び甲11を提出するが,これらが頒布されたのは本件優先日以降であるから,本件明細書に開示された範囲を超えてこれらに基づく効果を本件発明12の進歩性の判断において参酌することは許されない。・・・少なくとも,原告が主張するような効果,すなわち,混合物を適用する場合,1日の適用回数を減らしても優れた効果が得られることを,本件明細書の記載から読み取ることはできないから,そのような効果を本件発明12の進歩性の判断において考慮することはできない(まして,原告が指摘する甲11に示されるようなサイトカイン分泌の相乗的抑制効果については,かかるメカニズムは本件明細書には一切記載されていないから,そのような効果を本件発明12の進歩性の判断において参酌することは許されない。)。」
【コメント】
明細書に開示された範囲を超える効果や記載から読み取ることはできない効果を、進歩性の判断において参酌することは許されない。
本事件では、控訴人が提出した論文(甲10)は参酌されなかった。
発明の効果が顕著かどうかについての結論はよいとしても、効果に関する主張として提出された論文が参酌されなかった点については、理由が明らかでない。
優先日?(出願日の間違いでは?)以降に頒布されたものだから参酌されなかったのか、明細書に開示された範囲を超えていたから参酌されなかったのか(判決文を見る限り、控訴人は新たな効果を主張しているようには感じられないが・・・)。
顕著でないとの結論に変わりはないから説明を省略したということはないと思うが、進歩性における効果の顕著性を主張する際に後出しデータが参酌されるかどうかは両当事者にとって極めて重要なポイントとなることから、判決には丁寧な理由付けを示していただきたい。
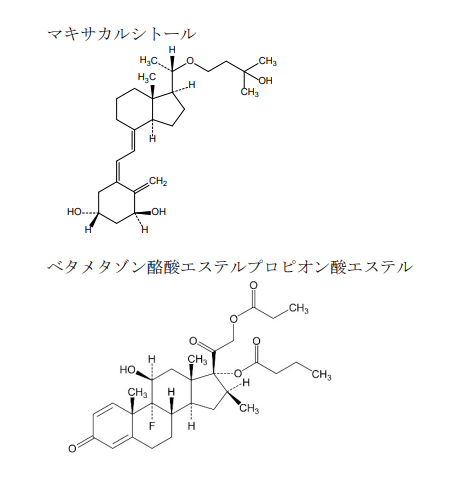 マーデュオックス®軟膏(Marduox® Ointment)は活性型ビタミンD3外用剤であるマキサカルシトール(Maxacalcitol)軟膏の有効成分Maxacalcitolとvery strongクラスのステロイド外用剤であるベタメタゾン酪酸エステルプロピオン酸エステル(BBP)軟膏の有効成分BBPをそれぞれ承認製剤濃度で配合した尋常性乾癬治療外用剤である。
マーデュオックス®軟膏(Marduox® Ointment)は活性型ビタミンD3外用剤であるマキサカルシトール(Maxacalcitol)軟膏の有効成分Maxacalcitolとvery strongクラスのステロイド外用剤であるベタメタゾン酪酸エステルプロピオン酸エステル(BBP)軟膏の有効成分BBPをそれぞれ承認製剤濃度で配合した尋常性乾癬治療外用剤である。
参考:
- 中外製薬 press release: 2016.03.28 「尋常性乾癬治療剤(配合外用剤)「マーデュオックス®軟膏」製造販売承認取得のお知らせ」
ところで、本件特許の実施例として記載されているカルシポトリオール(Calcipotriol)とベタメタゾンジプロピオネート(Betamethasone Dipropionate)を含む軟膏に直接関連すると思われる製品は、レオファーマが製造販売元・協和発酵キリンが販売元となっている尋常性乾癬治療剤ドボベット®軟膏(Dovobet® Ointment)。
ドボベット®軟膏(Dovobet® Ointment)は、活性型ビタミンD3誘導体であるカルシポトリオール水和物52.2μg/g(カルシポトリオールとして50.0μg/g)と副腎皮質ホルモンであるベタメタゾンジプロピオン酸エステル0.643mg/gを含有する配合剤であり、レオ ファーマで開発され、日本では2014年7月に承認された。
ドボベット®軟膏の配合成分であるカルシポトリオール(無水物)は「ドボネックス®軟膏 50μg/g」として、ベタメタゾンジプロピオン酸エステルは「リンデロン®‐DP 軟膏」として市販されている。
参考:
- 協和発酵キリン press release: 2014.07.04 「尋常性乾癬治療の配合外用剤「ドボベット®軟膏」承認取得のお知らせ」
国内において、尋常性乾癬の適応を有する活性型ビタミンD3誘導体とステロイドの配合剤という点で、マーデュオックス®軟膏(Marduox® Ointment)(中外・マルホ)とドボベット®軟膏(Dovobet® Ointment)(レオ ファーマ・協和発酵キリン)は競合関係にある。
本件特許は第1の薬理学的活性成分Aがマキサカルシトールに限定されたものとして登録されたが、もともと本件出願は特願2013-014098(特開2013-075923)の分割出願であり、さらにその原出願は特願2008-191182(特開2008-297309、特許5721926)の分割出願であり、さらにその原出願は特願2000-613441(WO2000/064450、特表2002-542293、特許4426729)の分割出願であった。特許4426729は、第1の薬理学的活性成分Aとしてカルシポトリオール、第2の薬理学的活性成分Bとしてベタメタゾンに限定されたものとして登録され、ドボベット®軟膏で存続期間延長登録もされている(延長登録出願番号2014-700172、存続期間満了日2023.12.04)。
特許5721926は、溶媒成分C等の限定下ではあるが第1の薬理学的活性成分Aも第2の薬理学的活性成分Bも一定の範囲で登録されている(存続期間満了日2020.01.27。存続期間延長登録出願情報なし)。

コメント