併用医薬発明の実施可能要件: 知財高裁平成27年(行ケ)10021
【背景】
「ウイルス感染症およびその他の内科疾患を治療するための化合物,組成物および方法」に関する特許出願(特願2008-505632号。特表2008-538354号、WO2006/110656)の拒絶査定不服審判請求に対する不成立審決(不服2012-1280号)の取消訴訟。争点は、本願併用医薬発明の実施可能要件(特許法36条4項1号)の充足の有無。
本願発明(請求項1):
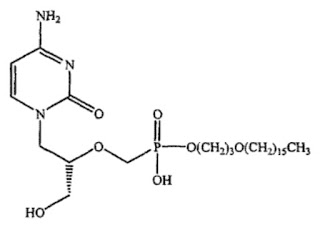
薬理学的に有効な量の下記の構造を有する化合物または医薬上許容可能されるその塩(以下,下線部分を「HDP-CDV又はその塩」ともいう。)と,少なくとも1つの免疫抑制剤とを含む,ウイルス感染を治療するための医薬組成物であって,前記ウイルス感染は,アデノウイルス,オルソポックスウイルス,HIV,B型肝炎ウイルス,C型肝炎ウイルス,サイトメガロウイルス,単純ヘルペスウイルス1型,単純ヘルペスウイルス2型又はパピローマウイルス感染である,医薬組成物。
【要旨】
主 文
1 原告の請求を棄却する。
裁判所の判断
裁判所は、取消事由1(実施可能要件の判断の誤り)について、まず下記のとおり医薬用途発明の実施可能要件の一般原則について言及した。
「(1) 特許法36条4項1号は,明細書の発明の詳細な説明の記載は,「その発明の属する技術の分野における通常の知識を有する者がその実施をすることができる程度に明確かつ十分に記載したもの」でなければならないと定めるところ,この規定にいう「実施」とは,物の発明においては,当該発明にかかる物の生産,使用等をいうものであるから,実施可能要件を満たすためには,明細書の発明の詳細な説明の記載は,当業者が当該発明に係る物を生産し,使用することができる程度のものでなければならない。
そして,医薬の用途発明においては,一般に,物質名,化学構造等が示されることのみによっては,当該用途の有用性及びそのための当該医薬の有効量を予測することは困難であり,当該医薬を当該用途に使用することができないから,医薬用途発明において実施可能要件を満たすためには,本願明細書の発明の詳細な説明は,その医薬を製造することができるだけでなく,出願時の技術常識に照らして,医薬としての有用性を当業者が理解できるように記載される必要がある。」
上記原則に照らし、本願の併用医薬としての有用性を当業者が理解できるように記載されているかについて、下記のとおり判断した。
「本願発明は,前記1において述べたように,抗ウイルス化合物であるシドフォビルの脂質含有プロドラッグとして公知のHDP-CDVに対し,免疫抑制剤をエンハンサーとして併用することにより,HDP-CDVの生物学的利用能を増強させ,より良い治療効果を奏する組成物とすることを技術的特徴とすることに照らせば,本願発明について医薬としての有用性があるというためには,HDP-CDVと免疫抑制剤を併用すると,HDP-CDVの生物学的利用能が増強されるだけでなく,HDP-CDVを単独で用いた場合に比べて,ウイルス感染の治療効果が向上することが必要であると解するのが相当である。
(中略)
そこで,本願明細書の発明の詳細な説明におけるHDP-CDV並びにエンハンサー及び免疫抑制剤に関する記載について検討すると・・・本願発明のようにHDP-CDVと免疫抑制剤との組合せを選択した場合にも,免疫抑制剤は,HDP-CDVの生物学的利用能を向上させる役割を果たすことについて一応の示唆がある。しかし,・・・
HDP-CDVあるいはその上位概念である抗ウイルス化合物と,特定の「免疫抑制剤」を併用した事例についての記載は,生体内(インビボ)における実験だけでなく,生体外(インビトロ)における実験についても一切記載されていない。前記のとおり,表1において,エンハンサーとして使用できる薬物として,抗不整脈や抗鬱薬などの種々の薬物と並んで免疫抑制剤が記載されているのみであって,免疫抑制剤によりHDP-CDVの生物学的利用能がどの程度向上するのかは具体的に確認されておらず,また,免疫抑制剤にはウイルス感染症を悪化させるという技術常識があることを念頭においた説明(例えば,免疫抑制作用によるウイルス感染症の悪化が生じない程度のエンハンサーとしての免疫抑制剤の用量など。)もないから,HDP-CDVと免疫抑制剤を投与すると,免疫抑制作用によるウイルス感染症の悪化が生じてエンハンサーとしての作用を減殺してしまい,HDP-CDV自体が有するウイルス感染治療作用を損なうという疑念が生じるものといわざるを得ない。
そうすると,本願明細書の発明の詳細な説明の記載から,ウイルス感染症を発症している患者に対してHDP-CDVと共に免疫抑制剤を投与すると,HDP-CDVの生物学的利用能が増強されることを当業者が理解することが可能であったとしても,上記の技術常識に照らすと,それと同時に,免疫抑制剤の利用により免疫が抑制されて感染症が悪化することが懸念されることから,HDP-CDVと免疫抑制剤を併用した場合には,HDP-CDVを単独で用いる場合に比べてウイルス感染の治療効果が向上するか否かは不明であるというほかなく,当業者が本願発明に医薬としての有用性があることを合理的に理解することは困難である。
したがって,本願明細書の発明の詳細な説明の記載は,本願出願日当時の技術常識に照らして,当業者が,本願発明の医薬としての有用性があることを理解できるように記載されていないから,実施可能要件を充足するということはできない。」
以上、裁判所は、本願発明が実施可能要件を欠くとした審決の判断には誤りがないからその余の審決の当否を判断するまでもなく原告の請求には理由がないと判断した。
【コメント】
併用医薬の実施可能要件が争われた事例である。本願併用医薬の有用性を示せるような具体的な実験例の記載は明細書中に一切なく、また出願日当時の技術常識を照らしても有用性があることを合理的に理解することは困難だった。併用医薬の実施可能要件が争われた最近の事件としては下記判決がある。
HDP-CDVとはcidofovir hexadecyloxypropyl esterの略称であり、出願人であるキメリクス社(Chimerix)が開発中であるbrincidofovir (CMX001)に相当する抗ウイルス剤のことのようである(参考publication)。
欧米での本願の審査状況は下記のとおり。
- EP1865967: The application has been withdrawn
- EP2842559: Request for examination was made
- US2007003608 (A1): Abandoned — Failure to Respond to an Office Action
- US2011015149 (A1): Non Final Action Mailed


コメント