アリピプラゾール(Aripiprazole)の中間体: 知財高裁平成22年(行ケ)10352
【背景】
「ベンゼンスルフォナート化合物」に関する特許出願(特願2000-399828; 特開2002-193915)の拒絶審決(不服2007-31090)取消訴訟。審決では、本願発明は刊行物1(特開平7-179457号公報)に記載された発明(引用発明)及び刊行物2に記載された発明に基づいて当業者が容易に発明することができたものであるから特許法29条2項の規定により特許を受けることができないと判断した。
請求項:
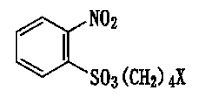
一般式(1)【化1】(右図参照)
[式中,Xはハロゲン原子を示す。]で表されるベンゼンスルフォナート化合物。
引用発明の内容:
4-クロロブチルp-トルエンスルフォナート化合物
一致点:
「4-クロロブチル 置換ベンゼンスルフォナート化合物」である点
相違点A:
置換ベンゼンスルフォナート化合物のベンゼン環上の置換基が,本願発明においては,「o-ニトロ」であるのに対し,引用発明においては,「p-メチル」である点
【要旨】
1. 取消事由1(本願発明の容易想到性の判断の誤り-周知技術の認定の誤り)について
原告は、
「審決が,刊行物2のみに基づいて,技術常識ないし周知技術として,「アルキル化剤として,p-メチルベンゼンスルフォナートより,o-ニトロベンゼンスルフォナートの方が優れていることが周知といえる。」と認定したことは誤りである」
と主張したが、裁判所は、そのように認定した審決に誤りは認められず、原告の主張は失当であると判断した。
また、原告は、実施した実験結果を提出(甲7)することによって、
「脱離基として優れたスルフォナートを有する化合物が優れたアルキル化剤であることが技術常識とはいえない」
と主張した。
しかし、裁判所は、
「原告が依拠する上記実験は,種々,反応条件を変えて目的化合物の収率や純度を比較したものであり,収率において相違が生じた原因が,単にアルキル化剤として使用した化合物の相違によるものであるか否かは不明であるから,実験条件によって結果に違いが発生したからといって,上記の一般的な知見が否定されるべきであるということはできない。」
と判断した。
原告は、
「「より不純物の少ない高純度のものが得られるようにするために,より穏和な条件で行える方法が望ましい」と一般化できるものではないから,刊行物1及び2に基づいて,「4-クロロブチル化」剤として,「4-クロロブチルo-ニトロベンゼンスルフォナート化合物」を想到することは,当業者にとって容易とはいえない」
と主張した。
しかし、裁判所は、
「ヘンドリックソン・クラム・ハモンド「有機化学[Ⅰ]第3版」~マクマリー「有機化学(上)第4版」~畑一夫他編「化学実験法」~記載によれば~本願出願前において,「より不純物の少ない高純度のものが得られるようにするために,より穏和な条件で行える方法が望ましい」ことは,化学反応における当業者の技術常識であったことが認められる。そして,上記技術常識を前提とすれば,刊行物2の「o-ニトロベンゼンスルホナートもトシラートより優れた脱離基である.」との記載から(甲2),当業者は,不純物の少ない高純度のものが得られるようにするために,引用発明において,p-メチルベンゼンスルフォナートより優れた脱離基であることが周知であるo-ニトロベンゼンスルフォナートを導入して本願発明の相違点Aに係る構成に到達することに困難はないというべきである。」
と判断した。
2. 取消事由2(本願発明の容易想到性の判断の誤り-引用発明に刊行物2記載の発明を適用した誤り)について
原告は、
「炭素原子のアルキル化と酸素原子のアルキル化とでは,通常,異なるアルキル化剤が用いられ,その反応機構も異なっているから,炭素原子をアルキル化する刊行物2記載の反応は,(酸素原子をアルキル化する)引用発明の化合物を用いた反応(及び本願発明の化合物を用いた反応)とは作用,機能の共通性がなく,当業者が引用発明に刊行物2記載の発明を適用して,本願発明を容易に想到し得るとはいえない」
と主張した。
しかし、裁判所は、
「刊行物2~のみならず,化学大辞典編集委員会編「化学大辞典1」~ヘンドリックソン・クラム・ハモンド「有機化学[Ⅰ]第3版」~と記載されることから,「スルホン酸エステル」を利用した「アルキル化」が,炭素原子のアルキル化反応に限定されず,酸素原子のアルキル化反応も含まれることは当業者にとって周知ということができる。そうすると,当業者であれば~刊行物2にいう「アルキル化剤」が,メタキシレンのような炭素原子のアルキル化に限らず,酸素原子のアルキル化を含むSN1及びSN2型のアルキル化反応一般に用いるアルキル化剤であると理解するものと認められる。」
と判断した。
これに対し、原告は、
「刊行物2の内容は~反応性が高いアルキル化剤になることは,副生成物を生じさせる可能性が高くなることを示唆するものである。」
と主張した。
しかし、裁判所は、
「上記1(2) のとおり,一般に,遷移状態のエネルギーが低く,反応性が大きければ,より穏和な条件の下でも反応が進みやすく,穏和な条件を採用することにより,副反応が少なく,より不純物の少ない高純度のものが得られる可能性が高いことは技術常識といえる。そうすると,刊行物2の「o-ニトロベンゼンスルホナートもトシラートより優れた脱離基である.」との記載から~反応性の高いアルキル化剤を用いたとしても,複数の反応点を有する化合物と反応させた場合に,副生成物を生じさせる可能性が高くなることが示唆されるとはいえない。」
と判断した。
3. 取消事由3(本願発明の効果に係る認定の誤り)について
原告は、
「「脱離基としてより優れたものを用いれば,脱離が容易になって,より穏和な条件で反応を行うことができ,その結果,不純物の少ない高純度のものが得られる」と一般化できるものではないから,本願発明の化合物を用いることにより,化合物7Qの4-ハロゲノブチル化を行った場合に高い純度及び収率で目的化合物を得られることは,当業者の予測を超える格別顕著な効果というべきである」
と主張した。
しかし、裁判所は、
「上記1(2) のとおり~「脱離基としてより優れたものを用いれば,脱離が容易になって,より穏和な条件で反応を行うことができ,その結果,不純物の少ない高純度のものが得られる」ことも,一般的な技術常識ということができる。したがって,より脱離基として優れた本願発明の化合物を用いることにより,化合物7Qの4-ハロゲノブチル化を行った場合に高い純度及び収率で目的化合物が得られることは,当業者であれば予測可能な効果というべきであり,原告の主張は失当である。」
と判断した。
請求棄却。
【コメント】
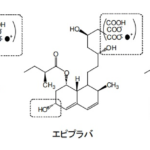
本事件で問題となった化合物は、大塚ホールディングスの主力製品である抗精神病薬エビリファイ®(Abilify)の有効成分アリピプラゾール(Aripiprazole)を合成するための中間体である。
Orangebookによれば、Abilify(aripiprazole)に関する米国特許(5,006,528)は2015年4月に満了することになる。この米国特許番号をもとにINPADOC patent familyサーチをしてみると、Abilifyの有効成分を保護する化合物特許は、BR, CN, DK, EP(Designated State(s): CH DE ES FR GB IT LI NL SE), HK, JP, KR, MX, USに出願/特許されていることがわかる。
一方、本件で問題となった中間体に関する出願は、日本出願公開番号(JP2002-193915)をもとにINPADOC patent familyサーチをしてみても、日本以外の国に出願されたという情報は出てこない。
製造中間体に関する特許出願の価値についての一般的な考え方:
- ひとつ目の考え方は、ジェネリックの参入を排除できるかもしれないという点である。しかし、特許の存在しない国での中間体の製造や最終化合物の製造に対して排除することはできないから、ジェネリックが海外から日本へ輸入されてしまえば、たとえ中間体の特許権を日本で保有していたとしても、ジェネリックの参入に対して直接権利行使することはできない。この観点からすれば、ジェネリックメーカーの製造拠点が存在する国だけに限らず、中間体・原薬製造メーカーが存在する多くの国々で中間体特許を取得しない限り、中間体特許はジェネリック参入阻止に対して現実的な価値があるとはいえないかもしれない。
- 二つ目の考え方は、競業会社(competitor)のFTO(freedom-to-operate)に対する牽制である。特に、競業会社の最終化合物の化学構造が自分たちのそれと類似しており、同一の(または類似の)製造中間体を経由して最終化合物を製造せざるを得ない場合や、価格・安全性・入手可能性等の理由からその中間体を経由することに大きなメリットがある場合である。しかし、この考えも、上記ジェネリック参入阻止に対する価値と同様に、多くの国々で中間体特許を取得しない限り、中間体特許は競業会社牽制として十分有効であるとはいえないかもしれない。
- 三つ目の考え方は、第三者に先を越されて中間体特許を取られてしまうと自らの中間体製造・使用の自由度(FTO)が低くなってしまうというリスクを未然に回避するために、出願することによって中間体を公知にすることである。
参考:
- 大塚HD有価証券報告書(2011.11.10 2012年3月期(第4期)第2四半期報告書)によると、大塚製薬㈱は、米国において「エビリファイ」(「ABILIFY」)のジェネリック医薬品の販売承認申請がなされたことを受けて、承認申請をしていた企業を相手方とする特許侵害訴訟を提起し、この訴訟について、平成22年11月15日付の第一審判決において、大塚製薬㈱は勝訴しているが、この勝訴判決に対して、Teva Pharmaceuticals USA, Inc.他4社から米国連邦巡回控訴裁判所に控訴が提起されており、現在も係属中とのこと。
- 大塚製薬プレスリリース: 2012.01.18 抗精神病薬「エビリファイ®」 新しい適応症「双極性障害における躁症状の改善」および新剤形「エビリファイ®OD錠」が承認
大塚製薬は、2012年1月18日に抗精神病薬エビリファイOD錠3mg・OD錠6mg・OD錠12mg・OD錠24mgの製造販売承認を取得し、近々発売する予定。


コメント