アクトス(ACTOS)併用の進歩性判断における効果の格別顕著性: 無効2010-800087及び無効2010-800088
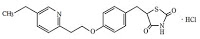 沢井製薬が請求した、武田薬品が有する「ピオグリタゾンと他の糖尿病薬との併用」に関する特許(特許3148973及び特許3973280)の無効審判(無効2010-800087及び無効2010-800088)について、特許庁は一部クレームについては無効としたが、他のクレームについての無効請求は成り立たないとした。各特許における特許庁の判断の要旨は下記の通り。
沢井製薬が請求した、武田薬品が有する「ピオグリタゾンと他の糖尿病薬との併用」に関する特許(特許3148973及び特許3973280)の無効審判(無効2010-800087及び無効2010-800088)について、特許庁は一部クレームについては無効としたが、他のクレームについての無効請求は成り立たないとした。各特許における特許庁の判断の要旨は下記の通り。
【特許3148973】
「ピオグリタゾンと、アカルボース、ボグリボースおよびミグリトールから選ばれるα-グルコシダーゼ阻害剤とを組み合わせてなる糖尿病または糖尿病性合併症の予防・治療用医薬」に関するクレームについて、特許庁は、請求人が提出した刊行物(甲第1~4号証)は、
①いずれも将来的な糖尿病治療を前提とするものと認められる。
②ピオグリタゾンとα-グルコシダーゼ阻害剤であるアカルボース,ボグリボース又はミグリトールとを併用については単にそのことが記載又は示唆されているにとどまる。
③当該併用により実際に糖尿病治療が行われたことや,その併用について糖尿病治療に係る薬理効果を実際に確認したことについて何ら記載するものではない。
④いずれもピオグリタゾンとα-グルコシダーゼ阻害剤であるアカルボース,ミグリトール又はボグリボースとの併用に係る医薬につき,当業者が直ちにその有用性を理解することができるように発明として記載されていると言うことはできない。
という理由から、ピオグリタゾンとα-グルコシダーゼ阻害剤であるアカルボース、ボグリボース又はミグリトールとの組み合わせに係る薬理効果の実証を伴わないこれら記載のみからでは、これら刊行物(甲第1~4号証)において本件発明が記載されているとは認められないと判断した。
一方、進歩性判断については、
「ピオグリタゾンとα-グルコシダーゼ阻害剤であるアカルボース,ミグリトール又はボグリボースとを併用することにより実際に糖尿病治療が行われたことや,その併用について糖尿病治療に係る薬理効果を実際に確認したことについては何ら記載はなされていなくとも,~ピオグリタゾンとアカルボースとの組み合わせ,又は,ピオグリタゾンとボグリボースとの組み合わせとする動機付けを,当業者に与えるに足るものであると言うことはできる」
として、本件発明に係る糖尿病治療薬の構成自体は、これら刊行物(甲第1~4号証)の記載から当業者が容易に想到することができたと言うべきであると判断した。
しかしながら、本件発明の効果について、
①その作用機序の組み合わせが全く試みられていないという状況の下では,実際の効果は現実に使用してみなければ分からないという認識が,当業者には一般的であると認められる。
②糖尿病に対する薬剤の併用治療に関し,本件特許の優先権主張の日前において,異なる作用機序の薬剤を併用して用いれば例外なく,相加的又は相乗的な効果が必ずもたらされることを当業者が認識していたという事実を認めるに足る根拠は全く見出せない。
③請求人が提出した甲第1~4号証に記載された技術的事項は上記のとおりいずれも,併用すれば効果の高い治療が可能となるかもしれない,という単なる期待の域を出ないものであり、相加的又は相乗的な効果をもたらすかもしれないという期待があることを単に記載するにとどまり,いずれの証拠も異なる作用機序に基づく糖尿病治療薬の併用は相加的又は相乗的な効果を必ずもたらすことを裏付けるものでは何らない。
④その併用により相加的又は相乗的な効果が奏されるか否かは,本件特許の優先権主張の日前において,当業者をしても実際に試験を行って逐一その確認をしてみないことには直ちに予測し得るものではない,という技術水準にあったと認められる。
⑤本件特許明細書の実験例1において示される併用効果が相加効果又は相乗効果のいずれであるのかまでは直ちには判断し得ないとしても,ピオグリタゾンとα-グルコシダーゼ阻害剤であるボグリボースとの併用による本件発明1の効果は,甲第1~4号証における記載からは当業者が予測できない格別顕著なものであると言うべきである。
とし、本件発明に係る糖尿病治療薬は、これら刊行物の記載から当業者が容易に想到することができたとは認められないと判断した。
【特許3973280】
「ピオグリタゾンと、グリメピリドとを組み合わせてなる糖尿病または糖尿病性合併症の予防・治療用医薬」に関するクレームについて、特許庁は、上記特許3148973と同様の判断により、無効請求は成り立たないと判断した。
一方、「ピオグリタゾンと、ビグアナイド剤とを組み合わせてなる糖尿病または糖尿病性合併症の予防・治療用医薬」に関するクレームについては、実施可能要件及びサポート要件に違反してなされたものであると判断し、それらクレームについては無効とした。
【コメント】
明細書に薬理試験結果が示されていた併用は、①塩酸ピオグリタゾンとα-グルコシダーゼ阻害剤であるボグリボースとの組み合わせ(実験例1)、および②塩酸ピオグリタゾンとSU剤であるグリベンクラミドとの組み合わせ(実験例2)、のみであったため、ピオグリタゾンとビグアナイド剤との併用クレームを実施可能要件違反及びサポート要件違反と判断した特許庁の判断は妥当に思えるが、進歩性の判断、特に効果が顕著であるかどうかの判断が果たして妥当なものなのかどうか・・・。
特許庁の判断は、「動機付けはあっても、試験してみなければ効果があるのかどうか分からないものについて試験をした結果、一定の効果が認められれば、効果の程度にかかわらず、効果につき格別顕著性がある」と言っているように思えのだが。
そして、本件明細書に記載されていた併用投与による効果を示す試験結果は、それぞれの単独投与と比較したものだけであり、他の組み合わせと比較したものではないという点も、これまでの下記判決と整合するのかどうか気になるところである。
- 2005.06.02 「ゼファーマ v. 特許庁長官」 知財高裁平成17年(行ケ)10459
- 2005.11.08 「興和 v. 特許庁長官」 知財高裁平成17年(行ケ)10389
- 2006.01.25 「メディカライズ v. 特許庁長官」 知財高裁平成17年(行ケ)10438
- 2007.05.16 「ロレアル v. 特許庁長官」 知財高裁平成18年(行ケ)10291
- 2006.10.26 「Takeda事件」 EPO審決T0512/02
本件は、進歩性判断について、ぜひ知財高裁に出訴して再検討されるべきだろう。なお、特許3148973は存続期間延長登録されており(出願番号2002-700098、2002-700099)、存続期間満了日は2017年11月15日となっている(20年目は2016年6月18日)。
一方、特許3973280は存続期間延長登録出願(出願番号2010-700127、2010-700128)されたがこちらはいずれも拒絶査定(発送日2011年2月15日)、その他、分割出願(特開2007-191494)も拒絶査定となっている(発送日2011年2月1日)。
アクトス(ACTOS; 有効成分:塩酸ピオグリタゾン(Pioglitazone Hydrochloride))の効能効果は下記のとおり。
2型糖尿病
ただし、下記のいずれかの治療で十分な効果が得られずインスリン抵抗性が推定される場合に限る。
1.①食事療法、運動療法のみ②食事療法、運動療法に加えてスルホニルウレア剤を使用③食事療法、運動療法に加えてα-グルコシダーゼ阻害剤を使用④食事療法、運動療法に加えてビグアナイド系薬剤を使用
2.食事療法、運動療法に加えてインスリン製剤を使用
メタクト配合錠LD/メタクト配合錠HD(有効成分: ピオグリタゾン塩酸塩(Pioglitazone Hydrochloride)およびメトホルミン塩酸塩(Metformin Hydrochloride))は昨年7月から日本で販売開始されている。
参考(追記):
-
- 後の知財高裁判決は下記のとおり。


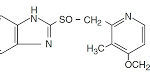
コメント