明細書に具体的に記載されていない効果: 知財高裁平成20年(行ケ)10353
「チアゾリジンジオンおよびスルホニルウレアを用いる糖尿病の治療」に関する出願(WO98/57649; 特表2001-523270)が進歩性無しを理由に拒絶とされた審決取消訴訟。
請求項1:
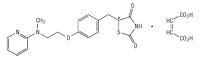
糖尿病および糖尿病関連症状の治療に用いられる医薬組成物であって,2ないし8mgの5-[4-[2-(N-メチル-N-(2-ピリジル)アミノ)エトキシ]ベンジル]チアゾリジン-2,4-ジオン(化合物I)またはその医薬上許容される塩;およびグリベンクラミド,グリピジド,グリクラジド,グリメピリド,トラザミド,トルブタミドまたはレパグリニドから選択されるインスリン分泌促進物質,および医薬上許容される担体を含む医薬組成物。
(1) 引用発明の内容
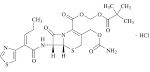
ピオグリタゾンとグリベンクラミドとを組み合わせてなる,糖尿病時の血糖値の上昇を抑制する医薬。
(2) 一致点
糖尿病および糖尿病関連症状の治療に用いられる医薬組成物であって,インスリン感受性増強剤とインスリン分泌促進物質としてのグリベンクラミドを含む医薬組成物である点。
(3) 相違点
相違点1
本願発明は医薬上許容される担体を含むのに対し,引用発明は医薬上許容される担体を含むことが特定されていない点。
相違点2
本願発明では,インスリン感受性増強剤が2ないし8mgの5-[4-[2-(N-メチル-N-(2-ピリジル)アミノ)エトキシ]ベンジル]チアゾリジン-2,4-ジオン(化合物I)であるのに対し,引用発明では,インスリン感受性増強剤がピオグリタゾンであり,その含有量が特定されていない点。
【要旨】
1. 相違点2についての容易想到性の判断の誤りについて
原告は、
「①引用例は,本願発明が規定する,化合物(I)またはその医薬上許容される塩と,グリベンクラミドをはじめとする特定のインスリン分泌促進剤という特定かつ具体的な組合せを教示ないし示唆するものではない,②引用例の表2の動物実験データは良好なものなので,当業者がピオグリタゾンと異なるインスリン感受性増強剤を用いる動機付けは存在しない」
などと主張した。
しかし、裁判所は、
「本願発明に用いるロシグリタゾンは,前記引用例の記載において,好適なインスリン感受性増強剤として例示された10数個程度の化合物のうちの一つであり,これを上記ピオグリタゾンに代えて上記グリベンクラミドと組み合わせることに格別の困難は認められない。」
と判断した。
また、原告は、
「本願発明の化合物(I)の最適用量の決定は,数多くの臨床データを積み重ね,これらを十分に精査し,副作用の危険性をも考慮してなされたものであり,そこで用いられた手法は通常のものであったとしても,臨床試験に着手してから結論に至るまでには,多大な労力,費用,時間が費やされたのであるから,当業者が適宜定め得るとはいえない」
と主張した。
しかし、裁判所は、
「本願発明の化合物(I)すなわちロシグリタゾンの最適用量の決定に多大な労力,費用,時間が費やされたとしても,通常想定されることであり,ロシグリタゾンの用量を決定したことに,当業者が格別の創意を要したものとはいえない。そして,「2ないし8mg」という用量も,医薬化合物の用量として当業者が想定し得る通常のものといえるから,当業者が容易になし得たものである。なお,原告は,上記用量の根拠として臨床実験データ(甲5の1,2)を提出しているが,上記用量を決定するために通常行なわれる実験にすぎず,上記判断を左右するものではない。」
と判断した。
2. 本願発明の顕著な作用効果の看過について
本願明細書には以下の記載がある。
ア「今回,驚くべきことに,インスリン分泌促進物質と組み合わされた化合物(Ⅰ)が血糖制御に対して特に有効な効果を発揮することが示された。それゆえ,かかる組合せは糖尿病,特にⅡ型糖尿病および糖尿病関連症状の治療に特に有用である。その治療を行う場合も最小限の副作用しか生じないことが示されている。」(6頁12~16行)
イ「本発明治療により提供される血糖制御に対する特に有益な効果は,個々の有効成分の合計に関して期待される対照効果に対する相乗効果であることが示される。慣用的方法,例えば,絶食時の血漿グルコースまたは糖鎖付加ヘモグロビン(HbA1c)のごとき典型的に使用される血糖制御指数により血糖制御を特徴づけてもよい。」(10頁8~13行)
特許庁は、
「同効果は,本願明細書に具体的に記載されていない効果であり,これをもって本願発明の進歩性の根拠とすることはできない」
と主張した。
しかし、裁判所は、以上の記載から、
「本願発明におけるインスリン分泌促進物質と組み合わされた化合物(Ⅰ)が血糖制御に対して有効であるという作用効果を奏することが認められる。」
と認定し、本願発明の上記作用効果が、引用発明から予測されない顕著な作用効果といえるか否かについて検討した。
原告は、
甲6(スルホニルウレア(グリピシド))とロシグリタゾンを併用投与した試験)及び甲7(スルホニルウレアとピオグリタゾンを併用投与した試験)等に示された結果を総合すると、
「本願発明には,長期間にわたって血糖値をうまく制御することができ,患者が低血糖症に陥ることがなく,しかも血圧の適度な低下もみられることは明らかであり,このような効果は,引用発明からは予測もできない顕著な作用効果を奏するものといえる。」
と主張した。
しかし、裁判所は、
「甲7の実験ではスルホニルウレアの物質を特定しておらず,それがグリベンクラミドとピオグリタゾンとの併用投与の場合(引用発明)であるということはできない。~HbA1cの改善の割合はむしろ後者の方が高くなっている。~甲6の実験と甲7の実験とを対比した場合,少なくとも治験の対象となる患者の病状や投与量の増加割合といった試験条件が異なるものである」
ことから、本願発明の血糖制御の作用効果は,引用発明から予測できない顕著な作用効果ということはできないと判断した。
請求棄却。
【コメント】
本願発明の化合物IはRosiglitazone(ロシグリタゾン)。インスリン抵抗性改善型2型糖尿病治療薬「マレイン酸ロシグリタゾン」として海外で販売(製品名: Avandia)。
「作用効果に関して薬理データ等の具体的記載が明細書には存在しないから進歩性の根拠とならない」という特許庁の主張について、裁判所は、触れることなく、明細書中の「血糖制御に対して特に有効な効果を発揮することが示された~個々の有効成分の合計に関して期待される対照効果に対する相乗効果であることが示される。」等の定性的な記載に基づいて「血糖制御に対して有効であるという作用効果を奏することが認められる」とし、血糖制御の作用効果に関して出願後に提出された具体的な証拠資料を参酌したうえで、進歩性の判断をした(進歩性は結局否定されたが)。医薬発明の”進歩性”判断に、明細書に具体的な薬理データを要求する(定性的な記載はダメとする)特許庁の主張、言わば”進歩性主張のための明細書記載要件”について、そのような要件は特許法29条2項には規定されていない(薬理データは実施可能要件で要求されるかもしれないが、進歩性判断とは関係ない)という立場のもと、裁判所は本事案を判断した、と理解したい。
関連:
参考:
- 審査基準 第II部第2章 新規性・進歩性 2.5論理づけの具体例 (3)引用発明と比較した有利な効果(抜粋)引用発明と比較した有利な効果が明細書等の記載から明確に把握される場合には、進歩性の存在を肯定的に推認するのに役立つ事実として、これを参酌する。②意見書等で主張された効果の参酌
明細書に引用発明と比較した有利な効果が記載されているとき、及び引用発明と比較した有利な効果は明記されていないが明細書又は図面の記載から当業者がその引用発明と比較した有利な効果を推論できるときは、意見書等において主張・立証(例えば実験結果)された効果を参酌する。しかし、明細書に記載されてなく、かつ、明細書又は図面の記載から当業者が推論できない意見書等で主張・立証された効果は参酌すべきでない。


コメント