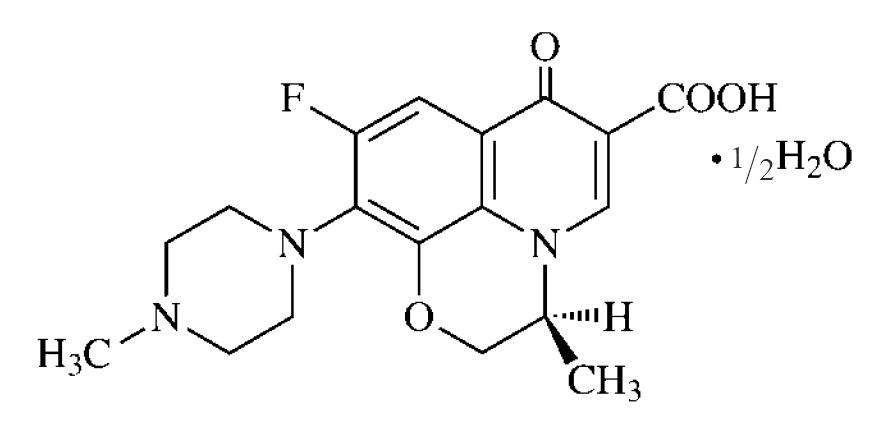
 2009年4月22日、第一三共は、広範囲経口抗菌製剤「クラビット®錠250mg・錠500mg・細粒10%」(一般名: レボフロキサシン水和物)の製造販売承認を取得した。クラビット 500mg 1日1回投与法は、従来の100mg 1日3回投与法と比較して最高血中濃度を上げることにより、殺菌作用が増強されると共に耐性菌の出現を抑制することが期待できるとのこと。クラビット製剤はこれまで1錠又は細粒1g中当たり有効成分(レボフロキサシン水和物)が100mgの製剤しかなく、しかも用法・用量は、通常、成人に対して、レボフロキサシン水和物として1回100mgを1日2~3回経口投与とされていた。
2009年4月22日、第一三共は、広範囲経口抗菌製剤「クラビット®錠250mg・錠500mg・細粒10%」(一般名: レボフロキサシン水和物)の製造販売承認を取得した。クラビット 500mg 1日1回投与法は、従来の100mg 1日3回投与法と比較して最高血中濃度を上げることにより、殺菌作用が増強されると共に耐性菌の出現を抑制することが期待できるとのこと。クラビット製剤はこれまで1錠又は細粒1g中当たり有効成分(レボフロキサシン水和物)が100mgの製剤しかなく、しかも用法・用量は、通常、成人に対して、レボフロキサシン水和物として1回100mgを1日2~3回経口投与とされていた。
- 2009.04.22 第一三共プレスリリース: 広範囲経口抗菌製剤「クラビット®錠250mg・錠500mg・細粒10%」製造販売承認取得のお知らせ
今回の承認による後発品との差別化が「クラビット」のライフサイクル延命化に功を奏するか、今後の「クラビット」の売れ行きに注目したい。しかし、とにかくまず注目すべきは現在争われている訴訟の行方である。
- 2009.04.09 「Daiichi Sankyo Files Patent Infringement Actions against 11 Generics Companies for CRAVIT® TABLETS and FINE GRANULES」
- 2009.03.23 「Daiichi Sankyo Files Patent Infringement Actions against 13 Generics Companies for CRAVIT® TABLTETS and FINE GRANULES」
- Levofloxacin – Daiichi’s patent term extension revoked in appeal proceedings.


コメント