2020年4月14日、協和キリンはアニュアルレポート2019年12月期(第97期)を発表しました。
本記事では、現時点での協和キリンの知的財産活動の景色をアニュアルレポート2019や他の公表情報・過去記事で振り返ります。
次期(2020年12月期)の業績見通し・・・日本において主力製品であるネスプのオーソライズドジェネリックであるダルベポエチン アルファ注シリンジ「KKF」への切り替えや薬価基準引き下げの影響などを受けることが予想されるものの、2018年に米国および欧州において発売を開始したCrysvitaおよびPoteligeo、2019年に米国で発売を開始したNourianzのグローバル戦略品の伸長が見込まれることから、売上収益は当期に比べ増収となる見通しです。
2020.04.14 アニュアルレポート2019年12月期(第97期)(p60)より
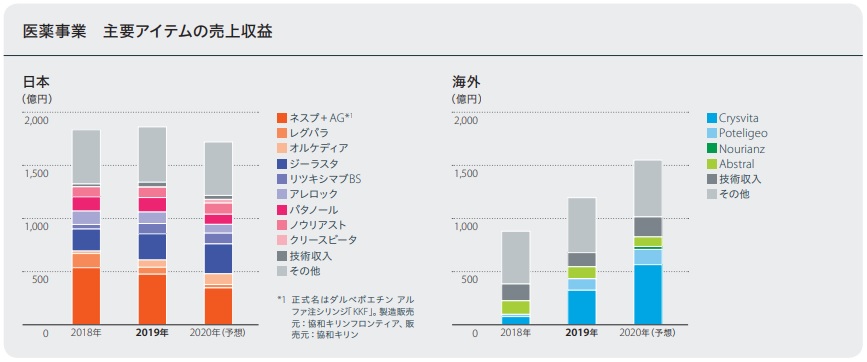
1.ネスプ®の特許期間満了への対応
ダルベポエチン アルファを有効成分とする持続型赤血球造血刺激因子製剤ネスプ®は、2007年の国内発売以来、協和キリンの主力製品として成長し続けてきましたが、基本特許満了によるダルベポエチン アルファ・バイオシミラーの参入に対抗するため、協和キリンは、ネスプ®のオーソライズドジェネリック(バイオセイム)となる「ダルベポエチン アルファ注シリンジ「KKF」」の投入(2019年8月に発売)に踏み切りました(2019.08.16 協和キリン press release: 持続型赤血球造血刺激因子製剤『ダルベポエチン アルファ注シリンジ「KKF」』国内製造販売承認取得のお知らせ)。
J-PlatPatによると、ネスプ®を保護する特許として4件の日本特許と存続期間延長登録出願の存在がわかります(表1)。現存する2件の特許は製剤特許またはプレフィルドシリンジに関する特許です。基本特許と思われる特許2938572は2019年8月16日に存続期間が満了しました。2019年11月から、複数のメーカーがダルベポエチン アルファ・バイオシミラーを販売しています。
| 特許番号 | 発明の名称 | 出願日 | 延長登録出願番号 | 存続期間満了日 |
| 4141156 | プランジャ後退制限機構付きプレフィルドシリンジ | 2002.03.15 | 2015-700035 2015-700034 2015-700033 2015-700032 2015-700031 2015-700030 2015-700029 2015-700028 2015-700027 2014-700301 | 2027.03.15 |
| 4493334 | HSA非含有組成物中のNESP/EPOの安定化剤としてのL-メチオニン | 2002.08.29 | 2015-700044 2015-700043 2015-700042 2015-700041 2015-700040 2015-700039 2015-700038 2015-700037 2015-700036 | 2025.11.24 |
| 3073905 | ヒトエリスロポエチン類似体 | 1990.10.09 | 2010-700131 2007-700064 | 2015.10.09 消滅 |
| 2938572 | エリトロポエチン類似体 | 1994.08.16 | 2010-700132 2007-700063 | 2019.08.16 消滅 |
2.グローバル戦略品クリースビータ®と知的財産権による保護
協和キリンは、クリースビータ®(Crysvita®)を成長キードライバーであるグローバル戦略品の一つと位置付け、価値最大化を図ることで、経営目標の達成を目指しています。有効成分であるブロスマブ(遺伝子組換え)は、線維芽細胞増殖因子23(FGF23)を標的とするヒト型IgG1モノクローナル抗体であり、協和キリンにより創製されました。日本では、クリースビータ®として2019年9月20日に「FGF23 関連低リン血症性くる病・骨軟化症」を効能・効果として、承認を取得しました(再審査期間は10年:2019年9月20日~2029年9月19日(希少疾病用医薬品))。欧米ではCrysvita®として2018年から販売されています。
J-PlatPatによると、クリースビータ®を保護する日本特許として1件の特許と存続期間延長登録出願の存在がわかります(表2)。これらの存続期間延長登録出願において5年の延長が登録されれば、延長された特許権の存続期間満了日は2033年2月14日となります。
| 特許番号 | 発明の名称 | 出願日 | 延長登録出願番号 | 存続期間満了日 |
| 4800396 | 抗FGF23抗体及びそれを含む医薬組成物 | 2008.02.14 | 2019-700725 2019-700724 2019-700723 | 2028.02.14 +5年? =2033.02.14? |
日本特許4800396の特許ファミリーである米国特許7,883,705及び9,290,569の審査書類内容を眺めていくと、現在、米国におけるCrysvita®の特許期間延長出願が、Indiana University Research and Technology Institute及びLudwig-Maximilians-Universtat Munchenから米国特許7,314,618(満了日を2022年5月8日から2027年5月8日とする5年間の延長申請)について、協和キリンから米国特許7,883,705(満了日を2029年2月5日から2032年4月17日とする5年間の延長申請)及び9,290,569 (満了日を2029年2月5日から2030年6月21日とする5年間の延長申請)について、それぞれ提出されていることがわかりました。

米国での特許延長は1つだけ・・・どの特許を選択する(される)のでしょうか・・・
各国での特許期間延長手続きが完了すれば、Crysvita®(クリースビータ®)の基本特許の満了日がそれぞれ見えてくるでしょう。
3.ジーラスタ®と知的財産権による保護
持続型G-CSF製剤ジーラスタ®(一般名:ペグフィルグラスチム(遺伝子組換え))は、顆粒球コロニー形成刺激因子(G-CSF)であるフィルグラスチム(遺伝子組換え)の血中半減期を延長する目的でアムジェン社が創製した、ポリエチレングリコール1分子(分子量約20,000)をフィルグラスチムのN末端に共有結合した修飾タンパク質です。キリン・アムジェン社から導入し、日本では、「がん化学療法による発熱性好中球減少症の発症抑制」の効能・効果で2014年9月26日に承認を取得しました(再審査期間は8年:2014年9月26日~2022年9月25日)。米国での販売名はNeulasta®としてアムジェン社が販売。
J-PlatPatによると、ジーラスタ®を保護する日本特許として2件の日本特許と存続期間延長登録出願の存在がわかります(表3)。そのうち、現在も存続しているのはプレフィルドシリンジに関する特許4141156のみとなります(延長登録により存続期間満了日は2027年3月15日)。
| 特許番号 | 発明の名称 | 出願日 | 延長登録出願番号 | 存続期間満了日 |
| 4141156 | プランジャ後退制限機構付きプレフィルドシリンジ | 2002.03.15 | 2014-700301 | 2027.03.15 |
| 3177251 | N末端化学修飾タンパク質組成物および方法 | 1995.02.08 | 2014-700300 | 2020.02.08 消滅 |
ジェネリックメーカーは、プレフィルドシリンジに関する特許4141156を回避することができれば、ジーラスタ®の再審査期間が終了する2022年9月25日以降にジーラスタ®のバイオシミラーの申請、承認を取得する可能性があり得ます。
協和キリンは、2020年2月20日に、ジーラスタ®の自動投与デバイスに関する国内臨床試験を開始したと発表しました(2020.02.20 協和キリン press release: ジーラスタ®の自動投与デバイスに関する国内臨床試験開始のお知らせ)。アムジェン社は海外ですでに同様なウェアラブル・デバイス(Neulasta®Onpro® kit: https://www.neulasta.com/onpro/)を販売しており、関連すると思われる出願を日本にもしているようです。このように患者の通院負担を軽減させるためのデバイス技術の承認を得ること及びそのような技術に関する知的財産の権利化を適切に進めていくことは、ジーラスタ®の製品競争力を高めることになると思われます。
4.リツキシマブ・バイオシミラー参入と特許紛争
協和キリンは、抗CD20モノクローナル抗体リツキシマブ(遺伝子組換え)製剤のバイオシミラーである「リツキシマブBS点滴静注100mg、500mg「KHK」」を2018年1月に国内で販売を開始し、2019年において順調に売り上げを伸ばしているようです。サンドとのライセンス契約に基づき、協和キリンが日本における本剤の販売およびマーケティング活動を担っています(2016.01.25 協和キリン press release: リツキシマブ・バイオシミラーの日本での販売に関するサンド社とのライセンス契約締結について)。

2019年では、リツキシマブについて侵害訴訟がありましたね・・・
5.協和キリンの特許分類(日本)
開発パイプラインを見ると、自社由来の開発品のほとんどが抗体で、協和キリンは、POTELLIGENT®やCOMPLEGENT®といった独自に確立した強活性抗体作製技術や完全ヒト抗体作製技術等による抗体医薬品の研究開発力という強みを持っています(https://www.kyowakirin.co.jp/antibody/index.html)。
日本において2010年~2019年に登録になった協和キリンの特許の分類コードランキング(J-PlatPat)を調べると、以下のとおり、遺伝子工学、タンパク質、細胞、抗体といったバイオ技術に関連した発明が大きな比率を占めていることがわかります(表4)。
| 順位 | 件数 | FI | 説明 |
| 1 | 100/269 | A61K31 | 有機活性成分を含有する医薬品製剤[2] |
| 1 | 100/269 | C12N15 | 突然変異または遺伝子工学;遺伝子工学に関するDNAまたはRNA,ベクター,例.プラスミド,またはその分離,製造または精製;そのための宿主の使用(突然変異体または遺伝的に処理された微生物,C12N1/00,C12N5/00,C12N7/00;植物新種A01H;組織培養技術による植物の増殖A01H4/00;動物新種A01K67/00;遺伝子疾病の治療のために生体の細胞内に挿入する遺伝子物質を含有する医薬品製剤の使用,遺伝子治療A61K48/00;ペプチド一般C07K)[3,5,6] |
| 3 | 78/269 | A61P35 | 抗腫瘍剤[7] |
| 4 | 77/269 | C12P21 | ペプチドまたは蛋白質の製造(単細胞菌体蛋白質C12N1/00)[3] |
| 5 | 68/269 | C07K16 | 免疫グロブリン,例.モノクローナル抗体またはポリクローナル抗体[6] |
| 6 | 66/269 | C12N5 | ヒト,動物または植物の細胞,例.セルライン;組織;その培養または維持;そのための培地(組織培養技術による植物の増殖A01H4/00)[3,5] |
| 7 | 60/269 | A61K39 | 抗原または抗体を含有する医薬品製剤(免疫分析用物質G01N33/53)[2] |
| 8 | 59/269 | A61P43 | グループA61P1/00~A61P41/00に展開されていない特殊な目的の医薬[7] |
| 9 | 52/269 | A61P29 | 非中枢性鎮痛剤,解熱剤,抗炎症剤,例.抗リューマチ剤;非ステロイド系抗炎症薬(NSAIDs)[7] |
| 10 | 49/269 | A61K47 | 使用する不活性成分,例.担体または不活性添加剤,に特徴のある医薬品製剤;活性成分と化学結合した標的剤または修飾剤[2] |

抗体医薬品ではないけれど、パタノール®に関する特許では進歩性の判断について最高裁まで争いましたね・・・差戻し審理で決着はまだ・・・特許は2021年5月3日に満了しますね・・・
6.まとめ
成長ドライバーであるグローバル戦略品の筆頭Crysvita®(クリースビータ®)が2030年代初め?に想定される特許期間満了を迎える前に、それに続く自社開発パイプライン(特に強みである抗体医薬品でしょうか)をどれだけ充実させて成功に結び付けていくかが、協和キリンにとっての重要な課題と思われます。また、ほとんどの主力品がバイオ医薬品、すなわち注射剤であることから、投与デバイス(アプリ)の開発や技術導入・提携にも効果的に投資・知的財産を活用していくことができれば協和キリン製品全体の価値向上につながるかもしれません。


コメント
米国におけるCrysvita®の特許期間延長出願が以下3つそれぞれ提出されていたが、以下のとおり選択された。
【追加情報】
2023年11月22日、国内初の持続性G-CSF製剤ジーラスタ®のバイオ後続品(BS)が薬価収載され、持田製薬とニプロが即日発売しました。
予想通り、プレフィルドシリンジに関する特許4141156を回避、ジーラスタ®の再審査期間が終了した2022年9月25日以降の参入となりました。
https://ssl4.eir-parts.net/doc/4534/tdnet/2366354/00.pdf
https://www.nipro.co.jp/assets/document/newsrelease/231122.pdf