
「創薬ちゃん」さま主催の「創薬 (wet) Advent Calendar 2024」参加記事(12/3)です。
特許的な視点の話題提供ですが、ひろ~い意味では創薬関連(wet?)ということで・・・。
2022年5月9日の弊ブログ記事「重水素化医薬品の特許的視点 - Austedo®(deutetrabenazine)とCTP-543(deuterated ruxolitinib)を例として –」では、FDAが承認した初の重水素化医薬品—Austedo®(deutetrabenazine)—とConcert社が開発している—CTP-543(deuterated ruxolitinib)(以下、「deuruxolitinib」)—の特許状況を通じて、既存薬を基にした重水素化医薬品の開発における課題を特許的視点から紹介しました。
具体的には、deuruxolitinibについて以下の点を述べました。
- 特許の無効リスク: オリジナル化合物であるruxolitinibを開発したIncyte社が、特許無効手続きに着手していること。
- 事業自由度(FTO)の問題: 重水素化化合物の独占期間を確保できたとしても、Incyte社が保有するruxolitinibの特許やColumbia大学が保有する特許との関係でFTO上の問題が生じる可能性。
それから2年以上が経過し、今年下半期に米国で重要な動きがありましたので、以下に簡単にご紹介します。
LEQSELVI®のFDA承認と特許状況
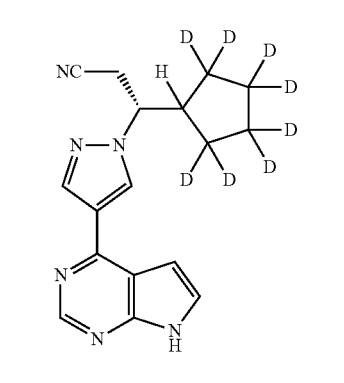 2024年7月25日、Sun社(2023年3月にConcert社を買収)は、deuruxolitinib phosphateを有効成分とする重症円形脱毛症治療薬LEQSELVI®の新薬承認をFDAから取得しました。
2024年7月25日、Sun社(2023年3月にConcert社を買収)は、deuruxolitinib phosphateを有効成分とする重症円形脱毛症治療薬LEQSELVI®の新薬承認をFDAから取得しました。
- 2024.07.26 Sun社 press release: U.S. FDA Approves LEQSELVI™ (deuruxolitinib), an Oral JAK Inhibitor for the Treatment of Severe Alopecia Areata
現時点でオレンジブックに収載されているLEQSELVI®を保護する特許は以下の3つです:
- 特許番号10,561,659(満了日: 2037年5月4日)
- 特許番号11,919,907(満了日: 2041年5月21日)
- 特許番号12,076,323(満了日: 2037年5月4日)
Incyte社による差止め仮処分命令
しかし、問題は依然として残されていました。
Incyte社が保有する米国特許9,662,335(前記弊ブログ記事で取り上げた特許)に基づく特許権侵害の主張が裁判所に認められ、2024年11月1日にLEQSELVI®の販売差止め仮処分命令が発せられました。
- 情報源: Incyte wins injunction to block launch of Sun Pharma’s JAK inhibitor Leqselvi (2024.11.04 FIERCE Pharmaより)
この結果、Sun社は、同社に好ましい判決が下るか、Incyte社の特許が満了する2026年12月まで、LEQSELVI®の販売を中止せざるを得ない状況に追い込まれています。
Sun社はすぐに控訴する方針を発表しました。
FTO確保の重要性
今回の事態は、2年以上前に指摘したリスクが現実化したものです。
このような現状を踏まえると、既存薬を基にした重水素化医薬品を開発する際には、FTOの確保が何より重要であることが改めて示されました。
LEQSELVI®のように重水素化化合物の独占期間を得ることができても、オリジナルの既存薬を保有する競合企業が継続出願を通じてその重水素化化合物を網羅または補足する可能性が残されている場合、FTOに致命的な問題が生じる可能性があります。
したがって、既存薬を基に重水素化医薬品を開発する場合には、以下の点を十分に考慮する必要があります:
- オリジナルの既存薬に関連する特許ファミリーの存続期間を見極める。
- 第三者特許との関係で特許クリアランスを徹底的に実施する。
- 潜在的リスクに対して効果的な対策を講じる。
特に、第三者特許の満了時期や継続出願による影響を事前に把握し、必要に応じた交渉の可能性も見定めながらFTOを確保するためのクリアランス対策を早期から練っていくことが重要といえます。



コメント