1.はじめに
本件(大阪地裁令和4年(ワ)3344)は、沢井製薬が骨粗鬆症治療薬「テリボン®皮下注用56.5μg」(有効成分:ヒト副甲状腺ホルモン(PTH)の活性部分であるN端側1-34ペプチド断片のテリパラチド酢酸塩)の後発医薬品を製造・販売したことに対し、その製品が旭化成ファーマの特許権を侵害しているとして、旭化成ファーマが販売差止め及び損害賠償を求めた訴訟である。
旭化成ファーマの特許権は、無菌注射剤の製造施設内でのPTHペプチド含有凍結乾燥製剤の製造方法に関するものである。
沢井製薬は、特許の無効を主張し、その理由として、引用文献に明示はされていないものの、製造工程上で必然的に内在すると考えられる酸化抑制(オゾンとの接触抑制)の構成が、引用発明の構成により当然に実現されているとした。
これに対し、大阪地裁は、引用文献にはそのような目的に関する技術思想が開示されているとは認められないと判断。沢井製薬の特許無効の主張を退け、後発医薬品の製造・販売差止め、製品の廃棄、損害賠償金の支払いを命じる判決を下した。
本記事では、本件判決の内容を紹介するとともに、沢井製薬の特許無効の主張を踏まえ、引用文献に明示されていないが必然的に内在する「作用」又は「効果」の構成が本件発明との相違点であるかどうか判断する際には、その「作用」又は「効果」で表現された構成に隠された具体的な「手段」まで明らかにした上でその「手段」の対比を試みることが重要なのではないかと論ずる考察を試みた。
しかし、結果としては思いついたままの感想を述べるにとどまる内容となった。
2.事件の背景
沢井製薬は、2022年2月15日、旭化成ファーマが販売する骨粗鬆症治療薬「テリボン®皮下注用56.5μg」(有効成分:ヒト副甲状腺ホルモン(PTH)の活性部分であるN端側1-34ペプチド断片のテリパラチド(Teriparatide)酢酸塩)の後発医薬品「テリパラチド皮下注56.5μg『サワイ』」(以下「被告製品」)の製造販売承認を取得した。その後、薬価基準収載を経て、同年9月9日より被告製品の販売を開始した。
本件訴訟(大阪地裁令和4年(ワ)3344)は、旭化成ファーマ(原告)が有する特許「高純度PTH含有凍結乾燥製剤及びその製造方法」(特許第6025881号、以下「本件特許」)を巡るものである。
旭化成ファーマは、沢井製薬(被告)が本件発明1及び13(併せて「本件発明」)の技術的範囲に属する方法で被告製品を製造・販売したことが特許権侵害に当たると主張し、以下の請求を行った。
- 被告製品の製造・販売の差止め
- 製品の廃棄
- 薬価基準収載申請の取下げ又は削除願の提出
- 損害賠償金等の支払い(民法709条に基づく)
なお、沢井製薬は、口頭弁論終結時において、被告製品の製造販売を中止している。
本件発明は、無菌注射剤の製造施設内におけるPTHペプチド含有凍結乾燥製剤の製造方法存に関するものであり、構成要件は、次のとおり分説される。
(1)本件発明1(請求項1)
1B: PTHペプチド含有溶液調製工程の開始から凍結乾燥手段への搬入工程終了の間の工程のうち、少なくとも搬入工程を含む1以上のグレードAの環境を有する工程において、
1C: PTHペプチド含有溶液と同無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制することを特徴とする方法であって、
1D: 同PTHペプチド含有凍結乾燥製剤とは、当該製剤中のPTHペプチド量と全PTH類縁物質量の和に対するいずれのPTH類縁物質の量も1.0%以下であり、
1E: 及びPTHペプチド量と全PTH類縁物質量の和に対する全PTH類縁物質量が5.0%以下であることを少なくとも意味する、
1F: PTHペプチド含有凍結乾燥製剤の製造方法。
(2)本件発明13(請求項13)
13B: 請求項1乃至12のいずれか1項に記載の方法。
沢井製薬は、被告製品の製造方法(以下「被告方法」)が構成要件1A、1B、1Dから1F、及び13Aを充足することについて争わなかった。一方で、本件発明の技術的範囲への属否(争点1)及び無効理由の有無(争点2)について、もっぱら構成要件1Cに焦点を絞った主張を展開した。
3.裁判所の判断
大阪地方裁判所第21民事部(以下「裁判所」)は、原告の主張する被告製品の製造・販売等の差止め、製品の廃棄、損害賠償金支払いの請求を一部認容し、主文のとおり判決を下した。
1 被告は、別紙1「物件目録」記載の製品を、別紙3「被告方法の構成」の「裁判所の認定」欄記載の方法で製造、販売、又は販売の申出をしてはならない。
2 被告は、別紙1「物件目録」記載の製品を廃棄せよ。
3 被告は、原告に対し、30億6491万6243円及び内19億6875万円に対する令和5年8月28日から、内10億9616万6243円に対する同年11月14日から各支払済みまで年3パーセントの割合による金員を支払え。
4 原告のその余の請求をいずれも棄却する。
5 訴訟費用はこれを20分し、その3を原告の、その余を被告の負担とする。
以下、争点1(技術的範囲への属否)、争点2(無効理由の有無)及び争点3(差止め及び薬価基準収載申請取下げ等の必要性)に関する裁判所の判断を紹介する。
(1)技術的範囲への属否(争点1)
被告方法が構成要件1C(「PTHペプチド含有溶液と同無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制することを特徴とする方法であって」)の構成を有する場合、被告方法は、本件発明の各技術的範囲に属することになる。
裁判所は、構成要件1Cの充足性について検討し、被告方法では、搬入工程を含む工程において、PTHペプチド含有溶液と無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触が抑制されるから、被告方法は構成要件1Cを充足すると判断した。
沢井製薬は、構成要件1Cの「0.1ppm以下のオゾンとの接触を抑制すること」とは、本件発明の目的をそのまま抽象的に記載するのみで、クレーム上、具体的な構成は特定されておらず、このような広すぎる抽象的なクレームは、明細書に記載された具体的な構成に限定解釈されるべきである旨主張した。
しかし、裁判所は、以下のとおり、沢井製薬の主張は採用することができないと判断した。
「構成要件1Cは、PTHペプチド含有溶液と無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制することを規定するのみで、その手段について特定の方法に限定するものではなく、本件発明の他の構成要件において、これを限定する記載はない。
また、本件明細書には、PTHペプチド含有溶液と無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制する手段は特に限定されないことが明記されており(【0124】、【0125】)、同手段の例示として、PTHペプチド含有溶液周辺の空気の流動性や流動量を抑制すること(【0125】)及びPTHペプチド含有溶液周辺を不活性化ガスで置換すること(【0125】、【0135】)が記載されている。
このような構成要件及び本件明細書の記載内容に照らすと、本件発明1において、PTHペプチド含有溶液と無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制する手段は限定されておらず、何らかの方法によりこれを実現すれば足りるものと解される。」
(2)無効理由の有無(争点2)
ア 明確性要件(争点2-1)
沢井製薬は、
「構成要件1Cにおける、PTHペプチド含有溶液と無菌注射剤製造施設内空気に含まれるオゾンとの接触を抑制することは、請求項の記載において、その具体的な構成が特定されていないところ、本件特許の優先日前には、窒素を使用して空気環境との接触を抑制することにより薬液の酸化を防止する方法について、様々な技術が存在することが知られていたから、空気環境との接触を抑制する方法のうち、如何なる方法であれば、本件発明に対する侵害が成立し、如何なる方法であれば侵害が成立しないのかが不明確となり、第三者に不測の不利益を及ぼすことになるとして、本件発明は明確性要件に適合しない」
旨を主張した。
しかし、裁判所は、構成要件1Cの記載が第三者に不測の不利益を及ぼすほどに不明確であるとはいえず、本件発明に明確性要件違反があるとは認められないと判断した。
イ サポート要件(争点2-2)
沢井製薬は、
「本件発明は、構成要件1Cの構成によって、高純度のPTHペプチド含有凍結乾燥製剤を得ることができるとするものであるが、本件明細書に記載された試験結果からでは、当業者は、薬液とオゾンとの接触を抑制することによって、所期する高純度のPTHペプチド含有凍結乾燥製剤が得られたことを理解することができないとして、本件発明はサポート要件に適合しない」
旨を主張した。
しかし、裁判所は、当業者は、本件明細書の記載及び技術常識に照らし、本件発明が本件明細書に記載された発明であって、前記の本件明細書の各記載により、高純度のPTHペプチド含有凍結乾燥製剤の製造方法を提供するという本件発明の課題を解決できると認識することができるものと認められ、本件発明にサポート要件違反があるとはいえないと判断した。
ウ 乙1発明に基づく本件発明1の進歩性欠如の有無(争点2-3)
裁判所は、以下のとおり、乙1公報(特表平10-508817号)記載の特許請求の範囲、従来技術の課題、発明の目的や効果、実施例からしても、乙1公報記載の発明は、薬液を無菌状態で移送することに着目した発明であって、薬液が周辺空気と接触することによって酸化することを抑制することを示唆するような発明であるとは認められないと認定した。
「確かに、乙1公報の特許請求の範囲のとおり、乙1発明では、滅菌「不活性」保護ガス(窒素)が使用され、これには酸化抑制効果があるが、これは薬剤を無菌状態で移送することを目的としていると解されるのであって、上記の発明の詳細な説明に鑑みれば、当業者が、周囲空気との接触による酸化の抑制を目的としていると認識するとは認め難い。被告が主張するような、窒素等の不活性ガスは滅菌されなければ「滅菌不活性保護ガス」にはならない、薬剤と周囲空気との接触を抑制し、不活性ガスを充填することによって薬剤の酸化防止を図ることができる、との技術常識が存在したとしても、乙1公報に、酸化抑制効果を意図した具体的な記載がなく、薬液と周囲空気との接触の抑制による酸化の抑制との技術思想が開示されているとは認められない。そして、・・・乙1公報記載の実施例は「二酸化炭素に敏感なオメプラゾール」に関するものであるところ、オメプラゾールが、酸化防止を要する薬剤ではなく、「無菌状態で移送しようとしている」非密封容器内の薬剤の例として挙げられていることも踏まえると、当業者が、このような実施例を周囲空気との接触による酸化の抑制を要する薬剤の例と解するとは認められない。」
以上を踏まえ、裁判所は、本件発明1では、PTHペプチド含有溶液と無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制することを特徴とする方法である旨定められているのに対し、乙1発明では、無菌薬剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制することを特徴とする方法である旨の記載がない点で相違する(以下「相違点1-3」)と認定した。
沢井製薬は、相違点1-3に関する容易想到性につき、以下の点を指摘した。
- (ア) 乙1発明は、薬液を凍結乾燥機へ搬入する工程において、薬液が空気環境 (周囲空気)等にさらされて薬剤の衛生度が悪影響を受けることを防止し、空気環境 (周囲空気)との接触により薬液が酸化されることを防止するため、窒素を非密封薬剤容器を覆うように絶えず均等に分布させるように一定の流量で導入する方法を採用し、空気環境(周囲空気)との接触を抑制した発明であるから、薬剤と無菌薬剤製造施設内空気に含まれるオゾンとの接触を抑制する作用がその構成自体に内在しており、本件発明1の「オゾンとの接触を抑制することを特徴とする方法」は、乙1発明の構成により当然に実現している。
- (イ) 本件特許の優先日前の技術常識から、乙1発明をPTHペプチド凍結乾燥製剤の製造に適用する当業者は、乙1発明の構成が、薬液のオゾンとの接触抑制のためにも作用すると当然に理解・認識する。
- (ウ) 本件発明1の「薬液とオゾンとの接触の抑制」との構成は、乙1発明の「薬液と周囲空気との接触の抑制」に必然的に内在しており、相違点1-3の「オゾンとの接触を抑制すること」との構成を乙1発明に適用することに動機付けは不要であるが、仮に何らかの積極的な動機付けが必要であるとしても、「薬液とオゾンとの接触の抑制」は、本件特許の優先日前の技術常識である。
しかし、裁判所は、乙1発明は、薬液を無菌状態で移送することを目的とする発明であって、搬入工程(運搬及び搬入)において、薬液が周辺空気と接触することによる酸化を抑制することを目的とする発明であるとは認められないから、これを前提とする前記(ウ)の主張は採用できないし、同様に、薬剤と無菌薬剤製造施設内空気に含まれるオゾンとの接触を抑制する作用がその構成自体に内在するという同(ア)の主張も採用できないと判断した。
さらに、裁判所は、以下のとおり、当業者は、乙1発明及び技術常識から、PTHペプチド含有溶液と無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制することを理解し認識するとはいえず、沢井製薬の前記主張は採用することができないとして、本件発明1は、乙1発明に技術常識を適用することにより、当業者が容易に想到し得たものではないと判断した。
本件発明は、PTHペプチドを含有する製剤は特に高純度であることが必要とされるという従来技術の課題に加え、本件発明の発明者らが、PTHペプチド含有凍結乾燥製剤を工業的に製造しようとするとPTH類縁物質を含んだ製剤が製造されることを知見したことによるものであるところ、乙1公報に工業的製造を前提とする前記課題に関する記載や示唆はなく、本件特許の優先日前において、前記知見が技術常識であったことを裏付ける資料もないから、乙1公報に接した当業者が、PTH含有凍結乾燥製剤の搬入工程においてPTH類縁物質が生成されるという課題を認識することにはならず、PTHペプチド含有溶液と無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制することに関する動機付けがあるとはいえない。
エ 乙2発明に基づく本件発明1の進歩性欠如の有無(争点2-4)
沢井製薬は、乙2公報(特表平9-506869号)の記載から、乙2発明は、PTHペプチド含有溶液の周囲空気との接触による酸化を防止する構成を客観的に備えた発明であって、薬液とオゾンとの接触の抑制は、薬液と周囲空気との接触の抑制により必然的に内在して実現されていると主張した。
しかし、裁判所は、
「乙2公報記載の特許請求の範囲、従来技術の課題、乙2発明の目的、実施例の方法に照らすと、乙2発明は、PTHペプチド含有凍結乾燥製剤の製造方法であって、賦形剤 (マンニトール)と緩衝剤 (クエン酸塩源)を配合することにより、製造後の保存安定性を有する副甲状腺ホルモン製剤を提供することを目的とするものであって、PTHペプチド含有溶液調製工程の開始から凍結乾燥手段への搬入工程終了の間のうち、少なくとも搬入工程(運搬及び搬入)を含む工程において、薬液が空気環境と接触することを抑制し、薬液の酸化を防止する構成を有するものとは認められないし、PTHペプチド含有溶液の周囲空気との接触による酸化を防止する構成を客観的に備えた発明とも認められない。したがって、乙2発明が酸化防止構成を備えていることを前提とする被告の前記主張は採用することができない。」
と判断し、以上を踏まえ、本件発明1では、少なくとも搬入工程を含む1以上の工程においてPTHペプチド含有溶液と無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制するのに対し、乙2発明には、無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制することが明記されていない点で相違する(以下「相違点2-3」)と認定した。
沢井製薬は、相違点2-3に関する容易想到性につき、以下の点を指摘した。
- 乙2発明は、PTHペプチドを含有する溶液をガラスバイアルに無菌的に充填したものをトレイに載せて、予め-50℃に冷却した、無菌の、窒素でパージした凍結乾燥機内に搬入することによって、搬入工程において、無菌注射剤製造施設内空気との接触を抑制する方法を開示するから、乙2発明には、PTHペプチドと、無菌注射剤製造施設内空気に含まれるオゾンとの接触を抑制する作用がその構成自体に内在しており、本件発明1の「オゾンとの接触を抑制することを特徴とする方法」は、乙2発明の構成により当然に実現している
- 本件特許の優先日前の技術常識から、乙2発明に接した当業者は、乙2発明の搬入工程(凍結乾燥機内にトレイを搬入する工程)において、薬液が空気環境と接触することを抑制し、薬液の酸化を防止する構成が、PTHペプチドのオゾンとの接触抑制のためにも作用するものと当然に理解し、オゾンとの接触抑制を目的の一つに含むものと理解・認識する
しかし、裁判所は、
「乙2公報に工業的製造を前提とする前記課題に関する記載や示唆はなく、本件特許の優先日前において、前記知見が技術常識であったことを裏付ける資料もないから、乙2公報に接した当業者が、PTH含有凍結乾燥製剤の搬入工程においてPTH類縁物質が生成されるという課題を認識することにはならず、PTHペプチド含有溶液と無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制することに関する動機付けがあるとはいえない。
したがって、当業者が、乙2発明及び技術常識から、乙2発明の搬入工程(凍結乾燥機内にトレイを搬入する工程)において、薬液が空気環境と接触することを抑制し、薬液の酸化を防止する構成が、PTHペプチドのオゾンとの接触抑制のためにも作用するものと当然に理解し、オゾンとの接触抑制を目的の一つに含むものと理解・認識するものとはいえず、被告の前記主張は採用することができない。」
として、本件発明1は、乙2発明に技術常識を適用することにより、当業者が容易に想到し得たものではないと判断した。
(3)差止め及び薬価基準収載申請の取下げ又は削除願の提出請求の必要性の有無(争点3)
裁判所は、沢井製薬が薬機法に基づきテリボン®の後発医薬品(被告製品)の製造販売を開始した行為について、これが継続されれば旭化成ファーマ(原告)に損害を及ぼすおそれがあると認定した。そのため、本件発明を侵害する方法で製造された被告製品の製造・販売を差し止める必要があると判断した。
一方、裁判所は、沢井製薬が本件発明の技術的範囲に属さない方法で後発医薬品を製造・販売することは許容されるべきであり、薬価基準収載品目削除願の提出を求めることは必要性を欠くと判断した。これは、旭化成ファーマ(原告)に過度の保護を与え、沢井製薬に大きな不利益を生じさせる可能性があるためである。
さらに、裁判所は、沢井製薬が既に製造した被告製品について、いずれも特許発明を侵害する方法で製造されたものであると認定した。そのため、これらの製品の廃棄を命じることに特段の限定は付さないと判断した。
4.コメント
(1)「作用・効果」の構成に隠されている具体的な「手段」
本件発明の構成要件1C「PTHペプチド含有溶液と同無菌注射剤製造施設内空気に含まれる0.1ppm以下のオゾンとの接触を抑制することを特徴とする方法であって」は、具体的な「手段」を規定した構成で表現されておらず、オゾンとの接触(酸化)を抑制するという作用又は効果を発揮できる何らかの方法、すなわち「作用」又は「効果」で規定した構成で表現されている。
本判決において、裁判所は、乙1発明について、「滅菌不活性保護ガス(窒素)が使用され、これには酸化抑制効果がある」と認定した一方で、「薬液を無菌状態で移送することを目的とする発明であり、酸化を抑制することを目的とする発明であるとは認められない」と判断した。
本件明細書の記載によると、構成要件1Cには、不活性ガス(具体的には窒素)を用いて凍結乾燥手段内を置換するという「手段」が含まれている。一方で、乙1発明も窒素を用いた手段を採用しており、この点では一致していると言える。
にもかかわらず、裁判所は構成要件1Cの文言を形式的に捉えるにとどまり、その中身である具体的な「手段」にまで踏み込んで対比検討しなかったため、この点を相違点として認定した判断は、十分に議論が尽くされたとは言い難いように思われる。
これは、構成要件が「手段」ではなく「作用」又は「効果」を表現している場合に、実際には引用発明と同じ「手段」であったとしても、あたかも新規の構成であるかのように見せることが可能となることを示唆している。このような表現方法は、出願人(又は代理人)が特許取得を目的として戦略的に採用するテクニックと見ることもできる。
(2)新規性・進歩性の判断と技術的範囲の判断における矛盾の可能性
本件判決において、裁判所は、引用文献に特許発明の構成要素である作用又は効果が内在していたとしても、それが明示又は意図されていない場合には特許発明の進歩性を否定する根拠にはならないとの判断を示した。
もし乙1発明がオメプラゾールではなくヒトPTH(1-34)に関するものであった場合、新規性や進歩性についてどのように判断されていただろうか。本件で新規性の欠如は争点ではなかったが、裁判所が引用文献における「目的」の違いを理由に「技術的思想が開示されているとは認められない」とした点から、引用発明に作用や効果が内在していたとしても新規性を否定する根拠にはならない、という立場を明確にしたように見受けられる。
このように、引用文献に内在するが明示的に記載されていない作用又は効果が新規性や進歩性を否定する材料とならない場合が多いのは、特許法が発明の創作性を重視する基本原則に基づいているためと考えられる。
本件発明の技術的範囲の属否判断において、被告である沢井製薬が「薬液を無菌状態で移送すること」を意図したものであり、特許発明の「酸化抑制」を意図していない(ただし結果的にはその作用又は効果を実現している)と主張したのかどうかは、判決文からは明らかではない。
裁判所は本件発明の技術的範囲に属すると判断したが、被告方法が特許発明の構成要件1C(「酸化抑制」を特徴とする方法)で規定される「酸化抑制」を目的とするものではなく、「薬液を無菌状態で移送すること」を目的とするものであった場合、それでも被告方法は本件発明の技術的範囲に属すると判断されるのだろうか。
本件では、特許の無効理由の判断では引用文献との「目的」を重要視する一方で、発明の技術的範囲の属否判断では被告方法での当該工程における「目的」が全く議論されていないことには、議論を尽くしていないバランスを欠いた判決のようにも思える。この判断は、発明の構成要件が被告方法の実施に意図せず内在している場合も技術的範囲に含まれると解釈される場合があることを意味するのだろうか。
このように、引用文献において内在する作用や効果としてその構成が実施されていても「目的」が異なるならば新規性・進歩性を否定しない一方で、第三者の行為においては内在する作用や構成としてその構成を意図せず実施していた場合には技術的範囲に含まれるかもしれないと判断されるのは、一見すると矛盾しているようにも見える。
新規性・進歩性の判断と技術的範囲の判断とは法的には異なるものであるため、このような運用は矛盾ではないと解釈されるかもしれない。しかし、特許制度を利用する者の視点では、不公平感や一貫性の欠如を感じる可能性がある。
用途発明での「ラベル論」の考え方は、このような製造方法の発明における構成についても適用可能なのだろうかという疑問もある。
上述の点に関して、特許法の運用における矛盾に見える点を整理し、特許制度の透明性及び特許性や権利侵害についての予見可能性を高める観点から、さらに議論の余地があるのではないだろうか。
内在理論に関連した記事:
- 2022.07.27 ブログ記事: 「内在同一の問題」 -製薬・バイオテクノロジー分野における新たな科学的発見と公衆衛生との間で揺れる特許保護のジレンマ-
- 2021.06.15 ブログ記事: 2021.05.17 「メルク・シャープ・アンド・ドーム v. ワイス」 知財高裁令和2年(行ケ)10015
(3)沢井製薬はなぜ事前に無効審判で争わなかったのか
2016年10月21日に登録された本件特許(特許第6025881号)は、優先日が2011年6月7日、原出願日が2012年5月31日である。一方、テリボン®の製造販売承認日は2011年9月26日であることから、旭化成ファーマは、テリボン®の保護期間を最大化するため、戦略的に出願時期を調整したと考えられる。本件特許の存続期間満了日は2032年5月31日である。
2017年5月15日に特許異議の申し立てがあったが、特許庁は特許維持の決定を下した(異議2017-700474: 確定日2017年8月15日)。異議申立人は個人であり、沢井製薬との関係は不明である。
沢井製薬は、2022年2月15日にテリボン®の後発医薬品(被告製品)の承認を取得し、同年9月9日から販売を開始した。本件特許に対して、沢井製薬を含む第三者から無効審判の請求はこれまで行われていない。
沢井製薬はテリボン®に関連する特許群に対し2018年から積極的に無効審判を請求し、特許クリアランスを進めてきた実績がある(ブログ記事参照: 2022.06.22 「日医工 v. 旭化成ファーマ」 知財高裁令和3年(行ケ)10115 骨粗鬆症治療剤テリボン®(テリパラチド酢酸塩)の週1回投与特許を巡る裁判⑧)。

このように、テリボン特許網の切り崩しを早くから着手してきた沢井製薬が、なぜ、本件特許に対しては後発医薬品販売後まで無効審判を請求しなかったのかは疑問である。
考えられる理由としては、以下のような可能性が挙げられる。
- 証拠収集の困難性: 構成要件1Cを充足する工程の侵害を旭化成ファーマが証明することが困難であり、訴訟には至らないと判断していた可能性。
- 「目的」の不一致: 被告方法が特許発明の「酸化抑制」を意図したものではなく、「薬液を無菌状態で移送すること」を目的とした当然の工程であるため、特許権侵害に問われないと考えていた可能性。
製造方法における証拠収集がどのように行われたかについては、判決文では詳細が省略されており不明である。
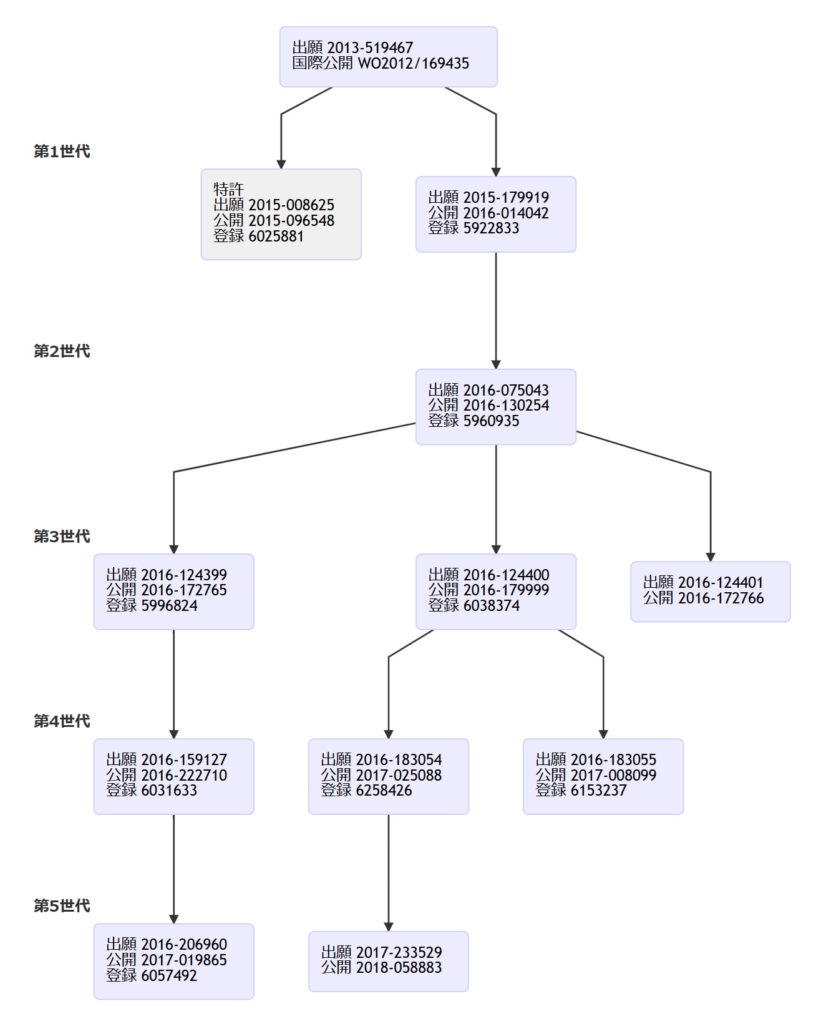
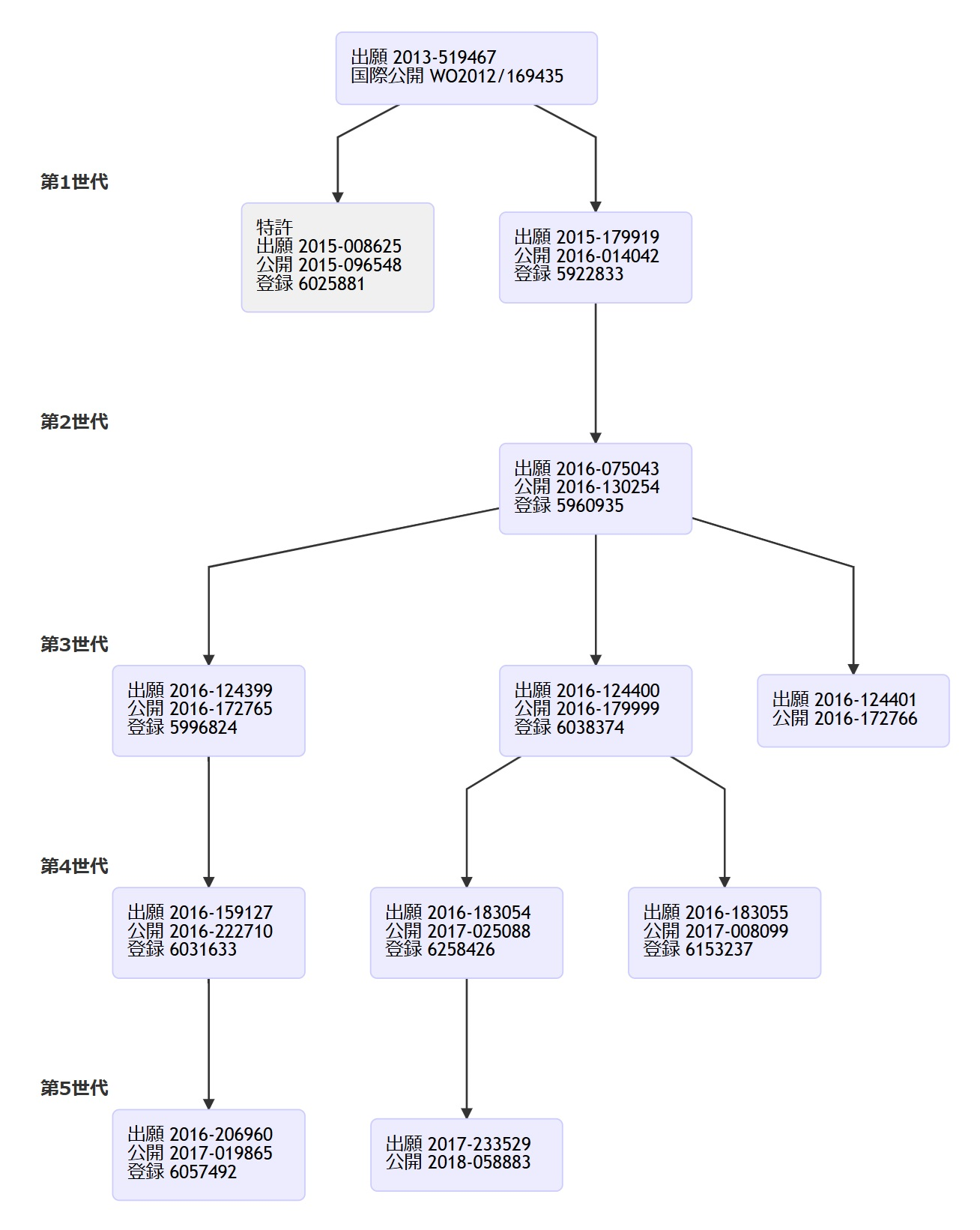
本件特許(特許第6025881号)は、特願2013-519467(PCT/JP2012/064229、国際公開番号: WO2012/169435)から派生した分割出願に基づくものである。同様に派生した分割出願ファミリーによって構築された特許群は、テリボン®を後発医薬品の脅威から守るための防衛網を形成している。
これらの特許群に対しても登録後に個人から異議申し立てがなされたが、いずれも特許維持の決定が下されている。本件特許以外の特許群について、旭化成ファーマと沢井製薬の間で特許権侵害をめぐる争いが生じていないかについては不明である。
参考: 特許第6025881号の分割出願ファミリー
5.おわりに
本件特許権に基づき、大阪地裁は、2023年9月4日、被告製品の製造・販売差止め及び製品の引渡しを命じる仮処分決定(原々決定)を下した(原々決定)(参照: 2023.09.05ブログ記事「旭化成ファーマ テリボン®皮下注用56.5μgの後発品を巡る特許権侵害訴訟で大阪地裁が沢井製品の製造販売差止の仮処分命令を発出」)。沢井製薬は、これに対し保全異議を申し立てたが、大阪地裁は原々決定を認可する決定(原決定)を行った。その後、沢井製薬は、原決定を不服として知財高裁に保全抗告を行ったが、旭化成ファーマの申立てについて認容した原々決定及び原決定を支持し、沢井製薬の抗告を棄却している(参照: ブログ記事: 2024.10.22 「沢井製薬 v. 旭化成ファーマ」 知財高裁令和6年(ラ)10001 ― 仮処分決定を不服とする保全異議申立却下決定に対する保全抗告事件 ―)。
この知財高裁の判断を見る限り、沢井製薬が本件を不服として知財高裁に控訴したとしても、沢井製薬にとって状況は厳しいと言えそうである。
テリボン®は、旭化成ファーマの主力品であり、2025年度は400億円の売上に達する勢いを見せている。
後発医薬品の承認を受けたのは沢井製薬のみであるが、同社は現在、出荷及び供給を停止している状況である。
本件特許の存続期間満了日が2032年5月31日であることを考えると、それまで後発医薬品が参入できない場合、この特許は非常に高い価値を持つものといえるだろう。
本判決については、これまで述べたように議論の余地がある。しかし、旭化成ファーマが製造工程の課題を発見し、技術的思想として昇華させ、技術的作用・効果を巧みにクレーム化して特許を取得した戦略は、後発医薬品の参入を阻む特許障壁を築き上げた点で評価に値する。このような戦略は、特許を取得する立場から見て、非常に参考となる。
参考:
- 2024.09.27 旭化成ファーマ press release: テリボン®皮下注用56.5μgに関する特許権侵害訴訟の判決について
- 2024.05 沢井製薬: テリパラチド皮下注用56.5μg「サワイ」の供給に関するお詫びとお願い

コメント
その「作用」又は「効果」で表現された構成に隠された具体的な「手段」まで明らかにした上でその「手段」の対比を試みることが重要
という考え方に同感です.
多分ですが,比較例を低く設定しているのであるから,その低い比較例における課題を,実施例における課題とは別により詳細に認定することにより,構成に隠された具体的な手段が明確になるのではないでしょうか
自分はその論理建てに成功していませんが.
コメントありがとうございます!