1.はじめに
株式会社ヘリオス(以下「ヘリオス」)、国立研究開発法人理化学研究所(以下「理研」)及び国立大学法人大阪大学(以下「大阪大学」)が共同保有する発明の名称を「網膜色素上皮細胞の製造方法」とする本件特許(第6518878号)に係る特許権に対して、2021年7月13日に、高橋政代氏(以下「高橋氏」)を代表取締役とする株式会社ビジョンケア(ビジョンケア)及び株式会社VC Cell Therapy(以下「VCCT社」)が、特許法第93条第2項の規定により公共の利益のための通常実施権を設定すべき旨の裁定を請求した事案(裁定請求2021-1。以下「本裁定請求」)について、2024年5月30日、当該特許権の実施権者である住友ファーマ株式会社(以下「住友ファーマ」)も含めた上記当事者間で和解が成立したことが、特許庁のウェブサイトや各当事者のプレスリリースにて発表されました。
参照:
- 2024.05.30 特許庁ウェブサイト: 裁定請求2021-1の取下げについて
- 2024.05.30 ビジョンケア press release: 裁定請求第1号(2021-1)「網膜色素上皮細胞の製造方法」の 特許使用に関する裁定請求の和解成立のご報告
- 2024.05.30 VCCT社 press release: 裁定請求第1号(2021-1)「網膜色素上皮細胞の製造方法」の特許使用に関する裁定請求の和解成立のご報告
- 2024.05.30 ヘリオス press release:裁定請求事案の終結に関するお知らせ
- 2024.05.30 住友ファーマ press release: 裁定請求事案の終結に関するお知らせ
- 2024.05.30 弁護士法人内田・鮫島法律事務所 お知らせ: 裁定請求事件の和解成立及び記者発表につきまして
和解の内容は、ヘリオス、理研及び大阪大学(被請求人ら)は、ビジョンケア及びVCCT社(請求人ら)が関与して⾏う網膜色素上皮(Retinal Pigment Epithelium: RPE)不全症(萎縮型加齢⻩斑変性及び滲出型加齢⻩斑変性の⼀部(RPE萎縮が⼤きく残るタイプ)を含む)を対象とした⾃由診療(以下「本⾃由診療」)において、請求⼈らが本特許権を実施して⾏う⾃家iPS細胞由来の網膜色素上皮細胞(以下「RPE細胞」)(MastCT-02)の製造、譲渡(本⾃由診療を⾏う医療機関に対するものに限る)、使⽤(前述の譲渡を受けた医療機関による使⽤を含む)に対して、以下の条件において、本特許権を権利⾏使しないことを約するというものです。
(1) 権利不⾏使期間 本和解契約成⽴後本特許権の存続期間満了まで
(2) 実施症例数30例まで(ただし、請求⼈らによる治療数が上記期間終了までに同症例数に達した場合には、その旨を被請求⼈らに伝えて症例数の増加を申し⼊れる)
また、請求⼈ら及び髙橋氏とヘリオス及び住友ファーマとは、互いに、今後⾏う事業(請求⼈らについては本⾃由診療、ヘリオス及び住友ファーマについては本特許権を実施して⾏う医薬品製造販売事業)について⼲渉しないことや、請求⼈ら及び髙橋氏は、ヘリオスが理研及び⼤阪⼤学との間で本特許権についての独占的実施契約の交渉を進めることを妨害せず、ヘリオス及び住友ファーマが本特許権を実施して⾏う治験並びにその後の医薬品製造及び販売に向けての⼀連の⾏為について上記実施に関わる関係者(治験実施施設、委託先及び顧客並びにその候補者を含む)と⼀切交渉しないこと等も定められています。
なお、公開された和解契約書には、和解金や実施料といった金銭支払義務条項は見当たりません。
裁定による通常実施権(いわゆる「強制実施権」)が日本史上初めて設定される事例となるかもしれないということで、その判断がどうなるのか注目されていましたが、和解に至ったことより裁定での決着は回避されました。
本記事では、本裁定請求の対象となった本件特許(第6518878号)の内容や世界初のiPS細胞の臨床応用となったRPE細胞を用いた再生医療の臨床研究との関係、そして本裁定請求から和解に至るまでの経緯を、関連する法改正の紹介も含めて振り返ります。また、公共の利益のための通常実施権設定の裁定の要件とは一体どのようなものなのか過去の資料等を確認し、この裁定請求事件の経過を通じて浮かび上がった公共の利益のための通常実施権設定の在り方・課題についてまとまりのない思いついたままの個人的感想を述べたいと思います。
2.本件特許の内容
 発明の名称を「網膜色素上皮細胞の製造方法」とする本件特許(第6518878号)に係る発明者は、澤田昌典氏(ヘリオス)、高橋政代氏(理研)、関口清俊(大阪大学)の3名(括弧内所属名は出願時)であり、特許権者は、ヘリオス、理研及び大阪大学となっています。
発明の名称を「網膜色素上皮細胞の製造方法」とする本件特許(第6518878号)に係る発明者は、澤田昌典氏(ヘリオス)、高橋政代氏(理研)、関口清俊(大阪大学)の3名(括弧内所属名は出願時)であり、特許権者は、ヘリオス、理研及び大阪大学となっています。
本件特許は、2014年10月9日を国際出願日とする特許出願(特願2015-541641号)に係るものであって、2019年5月10日に設定登録がなされました。
存続期間満了日は2034年10月9日です。
本件特許(第6518878号)の特許公報の記載によると、本発明の目的は、
「多能性幹細胞からの網膜色素上皮細胞への分化誘導効率が改善され、簡易な操作で高い純度の網膜色素上皮細胞を短期間で得ることができる網膜色素上皮細胞の製造方法、細胞を安定に増殖培養できる網膜色素上皮細胞の培養法、及び移植治療に有用な網膜色素上皮細胞を用いた毒性・薬効評価法並びに網膜疾患治療薬を提供すること」(【0007】)
であり、
「本発明者らは上記目的を達成するために鋭意検討した結果、ヒト多能性幹細胞をラミニンE8でコーティングした培養基材上で培養すると、播種した多能性幹細胞が培養基材へ速やかに接着し、早い段階から多量の色素細胞の生成が認められ、網膜色素上皮細胞の収量を著しく向上でき、しかも、培地交換時に細胞を失いにくく、純化工程を簡略化でき且つ短期間で高い純度の細胞集団が得られることを見出した。これにより、多能性幹細胞を網膜色素上皮細胞へ分化誘導する上での課題であった操作性及び経済性が著しく改善され、目的の網膜色素上皮細胞を安定に効率よく製造できることを見出し、本発明を完成させた。」(【0008】)
とのことです。
本件特許に係る特許請求の範囲は以下のとおりです。
【請求項1】
ラミニン511E8フラグメントがコーティングされた培養基材上でヒト多能性幹細胞を接着培養する工程を含む、網膜色素上皮細胞の製造方法であって、接着培養する工程が、分化誘導因子の存在下で行われる、方法。
【請求項2】
ヒト多能性幹細胞が、ヒトiPS細胞である、請求項1に記載の方法。
【請求項3】
ラミニン511E8フラグメントがコーティングされた培養基材上で網膜色素上皮細胞を接着培養する工程を含む、網膜色素上皮細胞の増幅方法。
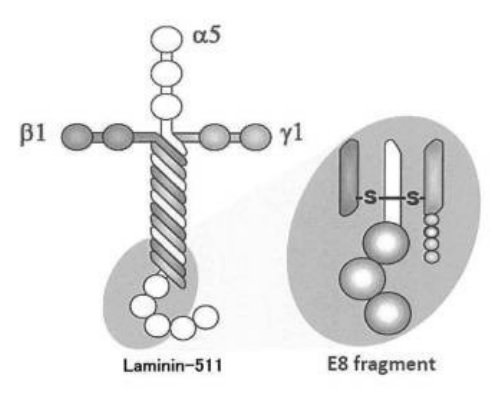
本件特許に係る発明は、明細書に記載された実施例によると、具体的には、iPS細胞を細胞外マトリックスタンパク質であるラミニン511(α5鎖、β1鎖、γ1鎖のヘテロ三量体で構成)のフラグメント(ラミニン511E8フラグメント)でコーティングされた培養基材上で培養することによって、網膜色素上皮細胞(RPE細胞)を作成する方法です。
この技術が発明されたことにより、iPS細胞由来RPE細胞をより効率的、大量且つ安定に作成することが可能になったのであれば、この発明は網膜疾患に対するiPS細胞を用いた再生医療の実用化にとって非常に期待される技術といえるでしょう。
3.iPS細胞由来RPE細胞を用いた臨床研究とライセンス
(1)理研による世界初iPS細胞の臨床応用
本発明に係る出願と並行して、理研は、難病の滲出型加齢黄斑変性患者本人の皮膚細胞から多分化能をもったiPS細胞を作製し、それを網膜色素上皮細胞(RPE細胞)に分化させシート状にして網膜の黄斑部に移植することによって、痛んだ網膜組織の再生を促し、視機能を維持・回復させるという新しい治療法の開発を目指し臨床研究をスタートしました。本件特許の発明者のひとりである高橋氏は、当時、理研・網膜再生医療研究開発プロジェクトのプロジェクトリーダーとしてこの臨床研究をリードし、2014年に最初の症例となる移植手術を実施しました。この臨床研究は、世界で初めてiPS細胞を臨床応用する事例となりました。
ただし、この時点での臨床研究は、本件特許の発明である「ラミニン511E8フラグメントでコーティングした培養基材上で培養する工程」を利用したものだったのかどうかは明らかでありません。
参考(理研の発表):
- 2013.02.28 「滲出型加齢黄斑変性に対する自家iPS細胞由来網膜色素上皮シート移植に関する臨床研究」の厚生労働省への申請について
- 2013.07.30 「滲出型加齢黄斑変性に対する自家iPS細胞由来網膜色素上皮シート移植に関する臨床研究」の研究開始について
- 2013.07.30 「滲出型加齢黄斑変性に対する自家iPS細胞由来網膜色素上皮シート移植に関する臨床研究」の研究開始に関するコメントについて
- 2014.09.12 第一症例目の移植実施について
- 2014.09.18 「滲出型加齢黄斑変性に対する自家iPS細胞由来網膜色素上皮シート移植に関する臨床研究」第1症例目の被験者の退院について
- 2015.10.02 「滲出型加齢黄斑変性に対する自家iPS細胞由来網膜色素上皮シート移植に関する臨床研究」における第一症例目の移植手術の経過について
- 2016.06.06 「滲出型加齢黄斑変性に対するiPS細胞由来網膜色素上皮細胞移植に関する臨床研究」の4機関による実施体制発足と協定書締結について
- 2017.03.16 加齢黄斑変性に対する自己iPS細胞由来網膜色素上皮シート移植(共同研究グループにヘリオスあり)
- Michiko Mandai, Akira Watanabe, Yasuo Kurimoto, et al. Autologous Induced Stem-Cell-Derived Retinal Cells for Macular Degeneration, N Engl J Med 2017; 376:1038-1046, doi: 10.1056/NEJMoa1608368; Supplementary Appendix: Preparation of iPSC-RPE and safety assessment “The differentiation of iPSCs into RPE and production of iPSC-RPE sheets without artificial scaffold were described previously.3”(この脚注3: Kamao H, Mandai M, Okamoto S, et al. Characterization of human induced pluripotent stem cell-derived retinal pigment epithelium cell sheets aiming for clinical application. Stem cell reports 2014;2(2):205–18; doi: 10.1016/j.stemcr.2013.12.007には、本件特許の発明である「ラミニン511E8フラグメントでコーティングした培養基材上で培養する工程」を利用している旨の記載はないようです)
(2)ヘリオスへのライセンス、開発主体は住友ファーマへ
ヘリオス(旧・株式会社日本網膜研究所)は、iPS細胞由来RPE研究に関する成果の事業化を目的として2011年2月24日に設立された理研認定ベンチャーです。
ヘリオスは、理研との間でiPS細胞を含む多能性幹細胞由来RPE細胞を有効成分として含有する再生医療製品を対象とする全世界を許諾領域とした特許実施許諾契約を締結して独占的ライセンスを受けており、また、2013年12月に、大日本住友製薬(現・住友ファーマ)と加齢黄斑変性等の眼疾患を対象としたiPS細胞由来RPE細胞を用いた国内における共同開発契約及び実施許諾契約を締結し、ヘリオスが所有するRPE細胞に関する一切の技術(特許、ノウハウ等)について、大日本住友製薬が実施許諾を受けること、RPE細胞医薬品については、国内での独占的通常実施権を、その他の製品については全世界の非独占的通常実施権を大日本住友製薬がヘリオスより受け、大日本住友製薬が提供する最大52億円の開発費用を基に国内におけるiPS細胞由来RPE細胞による細胞医薬品の開発を共同で行い、ヘリオスが製造販売承認の取得及び販売を行うことに合意するなど、iPS細胞から分化誘導したRPE細胞移植による加齢黄斑変性の新たな治療法を開発することを目指していました。
参考:
- ヘリオス Homepage: 事業分野-iPSC再生医薬品-加齢黄斑変性; 会社沿革
- 2013.12.02 大日本住友製薬 press release: ヘリオスと大日本住友製薬の再生・細胞医薬事業に関する提携のお知らせ~世界初の iPS 細胞技術を用いた再生・細胞医薬事業に向けた共同開発~
- 2013.12.02 大日本住友製薬 press release: iPS細胞技術の実用化に向けた国内事業提携について
- 2015.06.16 ヘリオス press release: 成長可能性に関する説明資料
- ヘリオス2015年12月期有価証券報告書
しかし、2019年、ヘリオスは、「短期的には体性幹細胞医薬品分野で実施中の2つの治験に集中する・・・。そのため自社のみで3つ目の治験を実施するのではなく、共同開発パートナーのサポートにより製品化に向けて進みたい」との意向から、大日本住友製薬との当初の契約を見直し、大日本住友製薬が主体となってRPE細胞製品の治験を行うことができるようにするなど共同開発契約を変更、また、大日本住友製薬に与えていたRPE細胞製品に関する実施許諾の対象地域を日本(独占)のみから、海外(非独占)も加えるなどの実施許諾契約を変更しました。
参考:
- 2019.06.13 大日本住友製薬 press release: iPS細胞由来網膜色素上皮細胞による治療法の日本における共同開発体制の変更について
- 2019.06.21 ヘリオス press release: 事業現況と短期・中長期成長戦略に関する説明
- ヘリオス2020年12月期 有価証券報告書
以上の経緯をたどり、加齢黄斑変性等の網膜疾患を対象としたiPS細胞由来RPE細胞を用いた国内における開発は、理研からの独占ライセンスを受けてヘリオスが当初計画していましたが、実質的には、ヘリオスからさらにRPE細胞医薬品についての独占的通常実施権(日本)を得た大日本住友製薬が主体となって進めることとなりました。
ヘリオスの2021年12月期 第2四半期決算短信(2021/8/10)によると、「iPS細胞由来網膜色素上皮(RPE)細胞を用いた治療法開発に向けて治験への準備を進め・・・大日本住友製薬株式会社との共同開発体制の変更を決定し、現在は同社が主体となって治験の準備が進められております。」と述べられており、大日本住友製薬の2022年3⽉期第1四半期決算資料(2021/7/29)(p16)によると、「加齢⻩斑変性を適応症として他家iPS細胞由来網膜⾊素上⽪細胞を用いた臨床研究実施中、企業治験開始に向けて準備中 (⽇本)、2021年度治験開始⽬標」とのことでしたが、治験開始時期のスケジュールは以前から大幅な遅れが続いていました。
ヘリオスと大日本住友製薬は、患者ごとに製造する必要があるためコストが高くなる自家iPS細胞ではなく、免疫抑制剤が必要かもしれませんがready-to-use(1ライン)で製造可能な他家iPS細胞から網膜⾊素上⽪細胞を作製することによる再生医療を目指すとしていました。
他家iPS細胞という難しさがあるのかもしれませんが、2014年に自家iPS細胞由来RPE細胞の移植手術が実施されてから本裁定請求がされるまで、既に7年が経過していました。
(3)高橋氏が理研を退職、ビジョンケアへ
理研において網膜再生医療研究開発プロジェクトのプロジェクトリーダーとしてiPS細胞由来RPE細胞を用いた臨床研究をリードしてきた高橋氏(本件特許の発明者の一人)は、2019年7月末に理研を退職し、8月1日にビジョンケアの代表取締役社長に就任しました。
高橋氏も創立者の一人として関わったヘリオス(2013.10.07 医学書院 医学会新聞 瀬尾拡史「この先生に会いたい!! 2つの世界からの視点が,新たな可能性を育む」参照)が、前述の通り、網膜疾患の再生医療の開発を主体で進めないこととなったこと(2019年6月発表)や、ヘリオスの運営方針に関する考え方の差も広がったことから、このままでは網膜疾患の再生医療の実用化が遅れることを懸念し、これまでの経験を活かすことで自らその実用化を早期に実現することを決断したようです。しかし、ビジョンケアがiPS細胞由来RPE細胞を用いた網膜疾患の再生医療の臨床研究を進めれば、将来的にへリオスや大日本住友製薬(現・住友ファーマ)との間で事業が競合する可能性は当然想定されていました(2019.08.05 日本経済新聞「理研退職の高橋政代氏、スタートアップで新治療に挑む 神戸のビジョンケア社長に」参照)。
もし仮に、ビジョンケアが実用化を目指す再生医療が、理研とヘリオスの間、そしてヘリオスと大日本住友製薬の間でそれぞれ締結されている特許権等の独占実施許諾契約の対象特許発明に該当するものであるとしたら、その契約当事者ではないビジョンケアは、理研、そして独占ライセンスを受けているヘリオス及び大日本住友製薬と交渉して実施許諾を得なければ、その再生医療を実現できないという最悪のケースもあり得たわけです。
高橋氏は、理研を退職してビジョンケアの代表取締役社長に就任しましたが、理研-ヘリオス-大日本住友製薬の間でがっちり独占ライセンスの契約が締結されているなかで、ビジョンケアという第三者の立場で網膜疾患の再生医療の実用化という事業自由度を確保していくために、非常に難しい舵取りをせざるを得なかったと想像されます。
4.本裁定請求から和解までの経緯
上述のような背景のもと、高橋氏は本裁定請求をすることを決断するに至ります。
髙橋⽒を代表取締役とするビジョンケア及びVCCT社(以下併せて「請求⼈ら」)は、2021年7⽉13⽇付けで、経済産業⼤⾂に対し、理研、⼤阪⼤学及びヘリオスを被請求⼈として、被請求⼈らが共有する本特許権について、特許法第93条第2項の規定により、公共の利益のための通常実施権を設定すべき旨の裁定を請求(裁定請求 2021-1)しました(2021.10.03 ブログ記事「理研・ヘリオス・大阪大学の「網膜色素上皮細胞の製造方法」特許に公共の利益のための通常実施権の設定を求めてビジョンケアが裁定を請求・・・iPS細胞を用いた世界初の臨床応用からなかなか進まないヘリオス・大日本住友による加齢黄斑変性に対する再生医療の治験」参照)。
本裁定請求を受けて、2021年12月2日に、特許庁において第1回工業所有権審議会 発明実施部会が開催され、工業所有権審議会運営規定第5条に基づき、原則として、会議、議事録及び議事要旨を非公開とすること、そして、会議で使用した資料も非公開とすることが確認されました(2021.12.17 ブログ記事「公共の利益のための通常実施権の許諾を求める裁定の請求2021-1 工業所有権審議会 発明実施部会(第1回)が開催」参照)。

参考:
- https://www.jpo.go.jp/resources/shingikai/kogyo-shoyu/hatumei20211202.html
- 裁定制度の運用要領(昭和50年12月1日決定、平成9年4月24日改正)
- 工業所有権審議会令
- 工業所有権審議会運営規程(平成13年2月20日制定、平成15年6月10日改正)
- 2021.12.02 工業所有権審議会 発明実施部会(第1回)「発明実施部会の運営について」
以後、合計22回の発明実施部会が開催され、第22回発明実施部会(令和5年11月14日~16日)で取りまとめられた答申案が工業所有権審議会総会で審議されることとなりました。そして、計3回の同総会が開催されましたが、いずれの回も議事録や議事要旨については非公開とされ、引き続き議論する旨だけが公表されていました。
なお、裁定手続においては、特許発明の実施事実や計画に関する証拠として、企業情報や技術情報が含まれた書類の提出が求められることがあります。しかしこれまでの制度では、裁定手続に関連する書類の閲覧を制限できなかったため、営業秘密が漏洩する懸念があり、その結果、裁定請求人や特許権者が必要な書類提出を控えてしまい、適切な裁定が難しくなる可能性がありました。
この問題に対処するため、裁定手続において提出された書類に営業秘密が含まれている場合に閲覧を制限できるよう、法改正が行われ、2023年7月3日に施行されました。
この法改正は、まさに、本裁定請求事件のために手当てされたものと言っても過言ではないでしょう(2023.06.08ブログ記事「不正競争防止法等の一部を改正する法律案が国会で可決成立 - 裁定関係書類の閲覧制限についての改正 -」参照)。
上述のように、工業所有権審議会での審議内容は非公開であり、裁定手続において提出された書類に営業秘密が含まれている場合に閲覧を制限できるよう法改正も行われたことによって、本裁定請求が結論に至ったとしても審議内容は公開されず、その理由も謎に包まれたままとなるのではないかと思われましたが、今回和解に至った当事者からの各プレスリリースにおいて、和解に至るまでの経緯についての概要が明らかとなりました。
その概要は以下のとおりであり、本裁定請求に対する各当事者の姿勢や発明実施部会による心証形成と実施権付与の可能性の方向性をうかがい知ることができます。
- 本裁定請求に対し、理研は協議に前向きに応じたいと考えている旨の答弁を行い、大阪大学も本裁定請求に対して特段の意見はない旨の答弁を行ったが、ヘリオスは、本裁定請求を却下又は棄却するとの裁定を求めた。
- 発明実施部会からの要請に応じて、請求人ら及びヘリオス双方から、意見書及び口頭陳述要領書並びに証拠が提出され、ヘリオスから提出された証拠には、同社が日本国内で他家 iPS 細胞由来RPE細胞(開発コード:HLCR011)の共同開発を進めており、本特許権についてヘリオスから独占的通常実施権の許諾を受けることが予定されている住友ファーマからの意見が含まれていた。
- 発明実施部会は、上記の経緯のもと審議を重ね、一定の暫定的心証を形成するとともに、本件事案は当事者間の自主的な協議により解決を図るのが望ましいとの見解に至り、発明実施部会長代理である清水節委員が中心となり、上記部会での審議とは別に非公開義務に反しない範囲内で、請求人ら及び高橋氏並びにヘリオス及び住友ファーマに対して、上記の暫定的心証を踏まえて、本裁定請求の対象のうち、自由診療における自家iPS細胞由来RPE細胞の製造についてのみ実施権を付与する可能性があることを前提として伝えた上で協議を行うことを求めた。
- 上記委員による意見調整のもと協議を重ねた結果、今般、理研及び大阪大学を含めて、本和解の成立に至った。
特許庁は、和解が成立したことについて、以下のコメントを出しました(2024.05.30 特許庁ウェブサイト: 裁定請求2021-1の取下げについて)。
「工業所有権審議会の審議においては、本件は、請求人ら代表者も本件特許の発明者の一人であり、請求人ら代表者と被請求人ヘリオスとは、一時期まで協同して本件特許を利用した眼疾患治療の事業化を目指していたという事案であるので、当事者間の自主的な協議により解決を図るのが望ましいとの意見がありました。また、工業所有権審議会において、当事者から直接意見を聞く中でも、当事者間の自主的な協議による解決を図ることが望ましいという姿勢で対応しました。上記を踏まえると、本件が当事者間の協議において和解が成立したことは、特許法の立法趣旨に合致するものです。」
斎藤健経済産業大臣は、5月31日の閣議後記者会見で、以下のように述べ、和解が成立したことを歓迎しました(2024.05.31 経済産業省ウェブサイト: 齋藤経済産業大臣の閣議後記者会見の概要)。
「昨日当事者間で和解が成立して、請求人から裁定請求取下書が提出されたと特許庁から報告を受けています。裁定制度は、その請求前に当事者間で協議を行うべき旨規定されています。和解により自発的な解決がなされ、新たな事業がこれにより実施される方向性となったことは、発明の利用により産業の発展に寄与するという特許法の趣旨に合致したものであると考えています。再生医療は機能不全の臓器の根本治療につながる技術であり、中でもiPS細胞の研究は我が国が強みを持つ分野です。本件は、眼疾患の再生医療に用いられる細胞をiPS細胞から製造する方法の特許に関するものであり、今後眼科領域をはじめとする再生医療の治療が一層拡大されることを期待したいと思います。」
ビジョンケア及びVCCT社の代表取締役社長である髙橋氏は、以下のように述べています(2024.05.30 ビジョンケア press release: 裁定請求第1号(2021-1)「網膜色素上皮細胞の製造方法」の 特許使用に関する裁定請求の和解成立のご報告; 2024.05.30 VCCT社 press release: 裁定請求第1号(2021-1)「網膜色素上皮細胞の製造方法」の特許使用に関する裁定請求の和解成立のご報告)。
「本和解成立は、おそらくは我が国で初めて、裁定申立の結果、特許権を有しなかった者に特許発明の使用が認められるに至ったことが広く公表可能となった事例であるという意味で大きな意義を持ち、産学連携が推進される昨今において同じ境遇に苦しむ発明者を勇気づけるものとして成果を上げられたと考えています。本裁定請求を通して、我々が強く訴えてきた「公共性の高い特許発明については、それをより良く活用できる者による実施が認めらなければならない」という主張の正当性が、長きにわたる努力により実を結び、皆様にこのような形でお知らせるできることに喜びを感じ、改めまして、本和解のお相手方ならびに温かいご支援をくださった皆様に深く感謝申しあげます。」
ヘリオスは、裁定請求事案の終結に関して、以下のように述べています(2024.05.30 ヘリオス press release:裁定請求事案の終結に関するお知らせ)。
「本和解は、自由診療を対象とする自家iPS細胞由来網膜色素上皮細胞の製造等の実施(30例まで)においてのみ請求人に対して被請求人が本件特許にかかる特許権を行使しないと約するものであり、当社及び住友ファーマは、両社が開発する他家iPS細胞由来網膜色素上皮細胞の事業への影響は軽微であると判断しています。・・・当社は、本件裁定請求事案の終結を受け、他家iPS細胞由来網膜色素上皮細胞の製造に関する本件特許等の技術を用いて、眼疾患に対する新たな治療法の実用化や治験の実施を、共同開発のパートナーである住友ファーマとともに着実に進めてまいります。」
住友ファーマは、裁定請求事案の終結に関して、以下のように述べています(2024.05.30 住友ファーマ press release: 裁定請求事案の終結に関するお知らせ)。
「本和解は、自由診療を対象とする自家 iPS 細胞由来網膜色素上皮細胞の製造等の実施(30 例まで)においてのみ請求人に対して被請求人が本件特許にかかる特許権を行使しないことを約するものであり、当社およびヘリオスとしては、両社が開発する HLCR011 の事業への影響は軽微であると判断しています。当社は、ヘリオスとともに、本特許権を利用して、網膜色素上皮裂孔を有する患者様に対するHLCR011 の臨床試験を進め、早期の実用化につなげることを目指します。」

iPS細胞での再生医療の実用化を待ち望んでいる患者の皆さまのために、当事者努力による和解に至ったことはとても良かったと思います。
5.公共の利益のための通常実施権設定の裁定
さて、公共の利益のための通常実施権の設定の裁定はどのような要件のもとで判断されるのでしょうか。
少し古い資料になりますが、2004年に開催された産業構造審議会知的財産政策部会特許制度小委員会 第7回特許戦略計画関連問題ワーキンググループ(平成16年3月3日)の資料5には「我が国における裁定制度について」詳しくまとめられています。この資料によると、裁定の実績として、「これまで特許権、実用新案権及び意匠権を合わせ計23件(不実施9件、利用関係14件)の裁定請求が行われているが、いずれも裁定に至る前に取り下げられており、裁定により通常実施権が設定された事例はない。」とのことでした。
そして、本裁定請求がされた旨を報じた朝日新聞記事(2021.09.28 特許技術の使用求め裁定請求 iPS細胞初移植の高橋政代氏)によると、「特許庁によると、「公共の利益のための通常実施権」による裁定請求は過去に1度だけで、却下されている。今回裁定の判断がされれば初のケースになるという。」とのことでした。また、神戸新聞記事(2021.09.28 制度初 iPS実用化巡り国に「裁定」請求 元理研の高橋政代氏「5年遅れている」)によると、「特許庁総務課によると、裁定が受理され、審議が始まるのは1972年の制度開始以来初めて。」とのことでした。
(1)公共の利益ための通常実施権設定の裁定とは
現行の特許法第93条は以下のように規定されています。
2 前項の協議が成立せず、又は協議をすることができないときは、その特許発明の実施をしようとする者は、経済産業大臣の裁定を請求することができる。
3 (省略)
2004年に開催された産業構造審議会知的財産政策部会特許制度小委員会 第7回特許戦略計画関連問題ワーキンググループ(平成16年3月3日)の資料5「我が国における裁定制度について」には、この裁定の規定の始まりは明治時代にまで遡る旨の記述があります。
我が国特許法における公共の利益のための裁定に関する規定は、1909年(明治42年)に制定された特許法において、「軍事上祕密ヲ要シ又ハ軍事上若ハ公益上必要ナル場合ニ於テハ特許權ハ之ヲ制限シ又ハ政府ニ於テ之ヲ收用シ、特許ハ之ヲ取消シ又ハ政府ニ於テ其ノ發明ヲ實施スルコトヲ得」(第44条第1項)と規定されたことに始まる。1921年(大正10年)法においても、明治42年法とほぼ同様の規定が維持された(第40条)。
しかし、1959年(昭和34年)法では、特許権の制限や政府による収用、特許の取消に関する規定が削除された。これは公益上の必要に基づくとはいっても国民の権利を制限し、剥奪するのは必要最小限にとどまるべきであり、また種々の事態を想定するも特許権を制限し、収用し、又は取り消すことを必要とする場合はほとんどあり得ないとの理由による。さらに、通常実施権の設定を受けることができるのは、旧法のように政府のみにとどまらず、公共の利益のために特に必要があって特許発明を実施しようとする者は誰でも通常実施権の設定を受けることができるとされた。また、不実施や利用関係の場合と同様、裁定請求に先立ち、協議が必要となった。
その後、1971年(昭和46年)には、許可、認可等の整理に関する法律(昭和46年法律第96号)により、通常実施権の許諾を求める協議の際に必要とされていた通商産業大臣の許可に関する規定が削除され、現在に至っている。
また、同資料によると、特許法第93条第1項における「公共の利益のため特に必要であるとき」の主要な事例としては、次に掲げる場合等が考えられるとされています(外資審議会専門委員会報告(1968年(昭和43年)3月15日)参照)。
○当該特許発明の通常実施権の許諾をしないことにより当該産業全般の健全な発展を阻害し、その結果国民生活に実質的弊害が認められる場合。
1968年に開催された外資審議会専門委員会(委員長 鈴木 武男氏)は、3月15日に「技術導入自由化と特許法、独占禁止法その他技術導入に関連する法律的諸問題」について報告を取りまとめ、同審議会技術導入小委員会に提出しました。当該報告の中では、資本取引及び技術導入自由化に関連し、特許法第93条による強制実施の裁定基準に係る考え方が示されました。主な内容は以下のとおりです。
- 特許法第93条の適用の可能性が考えられる場合として、当該特許発明が国民の生命、健康あるいは公共施設の建設等国民生活に直接関係する重要なものである場合があげられるほか、特定製品の生産または特定方法の実施に不可欠な工程に関する重要な特許発明が独占されることによって、次に掲げるような事態が生じ、その結果国民経済に重大な悪影響がもたらされる場合が考えられる。
-
- 当該特許発明の利用が期待される産業に、企業の倒産等の混乱が生じることにより、大量の失業者が発生するおそれがあること。
- 当該特許発明の利用が期待される産業に、企業の倒産等の混乱が生じることにより、その特許発明が実施できれば利用可能であった巨額の既存設備が廃棄されるおそれがあること。
- 当該特許発明の利用が期待される基幹産業、重要輸出産業又は先端技術分野の産業に、企業の倒産等の混乱が生じることにより、これら産業の健全な経済的・技術的発展を著しく阻害するおそれがあること
- 特許法第93条は特許権に対する重大な制約であるから、その適用は慎重にすべきである。なお、特許法第92条の強制実施によりうる場合には、これを発動すべきではない。
前記資料に基づく要件の考え方は、1968年の外資審議会専門委員会報告の中で示された考え方を踏襲するものであり、既に半世紀が経過しています。国民の生命や健康を取り巻く社会状況や産業・技術・経済は50年以上前に比べれば極めて大きく変化・進展しています。時代の変化に応じて要件を満たすのかどうかも慎重に検討する必要があるでしょう。
(2)本裁定請求は要件を満たしたか
6.強制実施権設定の在り方と浮かび上がった課題
特許法第93条第2項に基づく本裁定請求は、経済産業大臣による裁定に至らなかったものの、その審議過程が和解決着への道を開く重要な役割を果たしました。しかし、この過程を通じて、日本の強制実施権に関する課題が明らかになったようにも思えます。それらの課題として以下の点が挙げられるのではないでしょうか。
(1)まず、緊急性を要する場合、裁定までの迅速性に関する課題が挙げられます。公共の利益のためにその発明の緊急実施が望まれる場合においては、裁定請求後の迅速な審議や判断が必要とされます。例えば、人類にとって深刻な危機となるパンデミックのような緊急事態においては、特許権による行使を一時的に制限して本当に必要とされるワクチンや治療薬等を製造等するために迅速な政府の介入が求められることになるかもしれません。国民にとっての緊急事態において、今回のような数年にも及ぶ審議を待っていては裁定の意味がありません。緊急事態に対応できる迅速な審議を可能とするプロセスや判断基準を明確にしておく必要があるでしょう。なお、COVID-19における強制実施権の是非を巡っては国際問題として大きな議論になりました(以下のブログ記事を参照)。
参照:
- 2023.11.11 ブログ記事「TRIPS waiverのCOVID-19診断薬と治療薬への拡大議論の鍵となると期待されていた米国国際貿易委員会(USITC)の調査報告書が発表される」
- 2022.12.17 ブログ記事「WTO TRIPS理事会 COVID-19診断薬・治療薬への「TRIPS waiver」拡大議論 決議延期を勧告」
- 2022.06.19 ブログ記事「WTO閣僚会議 COVID-19ワクチン対象にTRIPS waiver採択 製薬団体は「科学者への冒涜」、「逆行」、「有害な先例」と痛烈に批判」
- 2021.11.14 ブログ記事「TRIPS協定及び公衆衛生に関する宣言(ドーハ宣言)から20年」
(2)裁定までの迅速性の無さという課題は、「公共の利益に特に必要であるとき」要件について具体的基準が無いことや審議内容が不透明であるという課題にも繋がってきます。裁定請求が認められるための要件が明確でなければ、裁定請求人にとって過度の主張負担を強いることになりますし、審議内容や裁定に至った理由の透明性が一定程度担保されなければ、当事者にとって納得感の得られない制度及び予測可能性を著しく欠いた制度となってしまうだけでなく、政府の介入を国民が監視するすべのない制度となってしまい、結果、危険な政治運用を許すことになりかねません。
(3)次に、大学等において政府資金を受けた研究成果から生じた発明に対しては、広義の公共の利益の観点から、強制実施権の設定を容易にすべきという議論があるかもしれません。
例えば、2006年5月23日、内閣府が設置した総合科学技術会議において「大学等における政府資金を原資とする研究開発から生じた知的財産権についての研究ライセンスに関する指針」が決定されました。本指針においては、大学等の研究における知的財産権の使用の円滑化を図るため、政府資金を原資として得られた大学等の知的財産権について、他の大学等が使用する場合の基本的な考え方が示されています。
参照:
- 「大学等における政府資金を原資とする研究開発から生じた知的財産権についての研究ライセンスに関する指針」(平成18年5月23日 総合科学技術会議)
- 総合科学技術会議 ライフサイエンス分野における知的財産の保護・活用等に関する検討プロジェクトチーム
しかし、特許法第93条第1項は「公共の利益のため『特に必要であるとき』」と定めていることからも、政府資金提供だけを理由に公共の利益の意味を広く解釈して裁定のハードルを下げることは妥当とは思えません。米国ではバイ・ドール法に基づく介入権(March-in rights/マーチ・イン・ライト)を製品価格交渉に利用しようとするバイデン政権の政策方針案が批判にさらされています(2024.06.23 ブログ記事「バイデン政権による介入権(March-in rights)を行使する薬価引下施策の提案に各界から反発の声」参照)。迅速な判断が求められる一方で、私権を制限することになる政府介入判断の是非には慎重さも求められます。
(4)また、せっかくの研究成果が世の中に広く還元されなくなるような事態(いわゆる特許権の「塩漬け」の問題)やパテントトロールに関連した課題があります。特許権者が自社の利益を優先し、意図的に特許発明(又はその技術的範囲の一部)の実施を控える場合、「公共の利益のため特に必要」とされる実施とのバランスにおいてどのような基準のもと考慮されるべきかも明確化しておく必要があるかもしれません。この点は、不実施の場合の通常実施権の設定の裁定(第83条)における基準と合わせて議論される必要があるでしょう。
例えば、2007年3月1日、総合科学技術会議において「ライフサイエンス分野におけるリサーチツール特許の使用の円滑化に関する指針」が決定されました。本指針においては、ライフサイエンス分野におけるリサーチツール特許について紛争を未然に回避し、使用の円滑化を図るため、大学等や民間企業におけるライセンスの基本的な考え方や、大学における必要な関連規程の整備や体制整備の促進を行うことが示されています。研究の上流にあるいわゆる「リサーチツール特許」は、そのリサーチツールが円滑に使用されないとその下流となる医薬品の研究開発の全体的な発展を阻害することになりかねないため、権利者と利用者のバランスを考慮した合理的な条件で非独占的に広くライセンスされることが望まれます。この考えは、上流から下流に至る全体の産業の発達に寄与することや国民の生命や健康に貢献するという点でも納得できるものです。本裁定請求の対象である「RPE細胞の製造方法」に関する本件特許が、「リサーチツール特許」に該当するかどうかは議論があるかもしれませんが、総合科学技術会議での議論や指針を考えると、本件特許は合理的な条件で非独占的に広くライセンスされるべきとの議論もあったかもしれません。
参照:
- 「ライフサイエンス分野におけるリサーチツール特許の使用の円滑化に関する指針」(平成19年3月1日 総合科学技術会議)
- 「ライフサイエンス分野におけるリサーチツール特許の使用の円滑化に関する指針」(概要版)(平成19年3月1日 総合科学技術会議資料)
- 総合科学技術会議 ライフサイエンス分野における知的財産の保護・活用等に関する検討プロジェクトチーム
(5)さらに、本裁定請求事件における特有の事情でもありました大学や研究機関といったアカデミアにおける研究者の人材流動とその後の研究活動で生じた支障に関する課題も考慮されるべきかもしれません。特に、大学が特許権の所有者となり独占的ライセンスを企業に与えた場合に、その時はwin-winでも時を経て状況も変わればその発明者(アカデミアの研究者)の独立性や交渉力が損なわれている可能性があります。これは「当事者どうしの契約の問題」といってしまえばそうかもしれません。しかし、医療や産業の発展のために何かできることはないのでしょうか。大学や企業との交渉において、個々の研究者が不利な立場に立たされることがないよう、契約担当者の教育や当事者の十分な理解の醸成等を促す適切な仕組みがまだまだ必要なのかもしれません。
(6)最後に、裁定請求の濫立のおそれが挙げられます。ライフサイエンス分野における特許権侵害訴訟において、被告が公共の利益のための通常実施権の設定の裁定を請求すること又は「裁定に付する旨の抗弁※」を主張することは、新たな防御方法として注目されるかもしれません(「「裁定制度」の在り方に関する一考察」(知財管理 Vol.68, No.1, p42(2018)特許第2委員会第5小委員会)参照)。しかし、ライフサイエンス分野における裁定請求が増加し、裁判所がこの「裁定に付する旨の抗弁」を受け入れ、事件をまずは裁定の審議に委ねるという判断を下す可能性があるとすれば、特許権侵害訴訟の審理は遅延してしまうことが懸念されます。今回の裁定請求事件は、公共性の高い事業の実施に取り組んでおられる企業にとっては希望を与えた一方で、潜在的な濫用にも警鐘を鳴らすものであると言えます。
※抗弁(こうべん)とは、民事訴訟において、被告が原告の申立て(請求)を排斥するために、その基礎となる事実と両立しつつその法律効果を排斥する別個の事実(請求原因事実と両立する権利障害、阻止、消滅事由の主張)をいいます。
以上の課題を踏まえると、本裁定請求事件により、強制実施権の在り方についての検討や政府の介入に関する規定の整備の必要性が浮きぼりになったように思われます。
7.和解後の動き
ヘリオス
2024年6月19日、ヘリオスは、アステラス製薬の子会社で他家多能性幹細胞由来の分化細胞を用いた治療法を研究するアステラス インスティチュート フォー リジェネレイティブ メディシン(Astellas Institute for Regenerative Medicine、以下「AIRM」)との間で、ヘリオスが理研及び大阪大学と共有するRPE細胞の製造法に関する特許(国際公開番号WO2015053375A1)ならびに大阪大学と共有する網膜色素上皮(RPE)細胞の純化法に関する特許(国際公開番号WO2015053376A1)を、日本以外の全世界における当該特許の出願国でAIRMに非独占的に許諾するライセンス契約を締結したと発表しました(2024.06.19 ヘリオス press release: アステラス製薬との RPE 細胞製造方法等に関するライセンス契約締結のお知らせ)。
この2件の特許のうちのひとつ(WO2015053375A1)の日本で登録された特許が、本裁定請求の対象となった本件特許(第6518878号)に該当します。
AIRMは、ヒト多能性幹細胞由来PRE細胞であるASP7317について、地図状萎縮を伴う加齢黄斑変性を対象疾患として、現在、第Ⅰb相試験を進めているようです(アステラス製薬 2024年3月期決算補足資料、ClinicalTrials.gov ID NCT03178149参照)。
またAIRMの親会社であるアステラス製薬は、約1年前、眼科領域における基盤ケイパビリティを獲得することを期待して、地図状萎縮を伴う加齢黄斑変性を対象とする新規補体因子C5阻害剤Avacincaptad Pegol硝子体内注射液(IZERVAY™)をはじめとしたプログラム及び眼科領域におけるバリューチェーン全体に渡るケイパビリティを有しているIveric Bio社を約59億ドル(約8000億円)で買収すると発表していました(2023.05.01 アステラス製薬 press release: 米国Iveric Bio社買収に関する契約締結のお知らせ)。その後、IZERVAY™はFDAで承認されています(2023.08.05 アステラス製薬 press release: IZERVAY™(avacincaptad pegol) 地図状萎縮を伴う加齢黄斑変性の治療薬として米国で承認取得)。
上述したAIRMとヘリオスとのライセンス契約の締結は、このような近年のアステラス製薬の海外での眼科領域におけるケイパビリティ獲得の一環と想像できます。
ビジョンケア及びVCCT社
ビジョンケア及びVCCT社のウェブサイトには、現時点で、RPE不全症を対象とした⾃家iPS細胞由来のRPE細胞(MastCT-02)を用いた自由診療の実施や進捗に関して和解後にアップデートされた具体的な情報は見当たりませんが、2024年6月26日、VCCT社は、北米を中心とした事業展開の強化として、米国に子会社(VCCT USA inc.)を設立したと発表しました。
同社が開発しているiPS細胞由来網膜色素上皮(RPE)移植は世界に広めるべき段階になったということで、その準備として米国の子会社を設立したとのことです(2024.06.26 VCCT社 press release: 米国子会社設立のお知らせ)。
同社が開発しているiPS細胞由来RPE移植を海外の患者さんにも届けるべくとうとう世界に進出するようです。

ヘリオスは、裁定請求の対象となった本件特許を含む2件の特許に関して、日本以外の全世界における当該特許の出願国でAIRMに非独占的に許諾するライセンス契約を締結したと発表してるぞ。米国では特許になっているようだし、今度は海外で問題が起きなければいいのだが・・・。VCCT社は回避策があるのかな。

とにかくiPS細胞由来RPE細胞移植による治療が世界の患者さんにも希望の光として早く届くといいですね。ピポ先輩~。
住友ファーマ
ラツーダクリフに直面し厳しい事業環境が続く住友ファーマは、2024年6月26日の第204期定時株主総会において、グループをあげた徹底的なコスト削減と研究活動については選択と集中により将来を担うパイプラインに経営資源を投下するとの方針を示し、現在進行中の他家iPS細胞由来RPE細胞(HLCR011)の網膜色素上皮裂孔を対象とした日本でのフェーズ1/2試験は着実に推進していくと発表しました(jRCT2073230077)。
2023年4月28日の中計経営計画2027説明会において、対象疾患を加齢黄斑変性から網膜色素上皮裂孔に変えたことに関して「その後、適応拡大で大きく伸びるという見通しなのか」との質問に対して、当時代表取締役専務執行役員だった木村徹氏(現・代表取締役社長)は、「HLCR011のほうですけど。今おっしゃったように、最初我々としては、網膜色素上皮裂孔ということで治験を開始したいと考えてございます。これは、これまでこの細胞を使った主流の治験は、加齢黄斑変性といったような変性疾患を対象にしてございました。変性疾患は進行も緩徐でありまして、そういう効果を見るのに非常に時間がかかる上で曖昧なところがあるというところで、この網膜色素上皮裂孔というのは、ある種、急性の症状でございまして、それに対して短期間でクリアにまず効果を出すということを目指してございます。一方で、患者さんの数はそう多くはございませんので、承認後の、ここの表に表れるような売上としては、大きくは計上していないということでございます。」と回答し、対象疾患の変更に伴う治験の遅れを懸念する質問に対しては、「今まで外部には発表しておりませんが、もうこの何年も前から、これでいくということで全ての計画は進んでございますので、外に公表するインディケーションが変わったことによって、我々の治験の計画が遅れるということはございません。」と回答しています。

もし、住友ファーマがiPS細胞由来RPE細胞の開発を「やっぱ、やめます・・・」と発表してたなら、裁定請求事件でかなり揉めた他の当事者からは「え!(怒)」となってたかもね。あっ、さすがにそれは無いか・・・。住友ファーマには網膜色素上皮裂孔の治験をぜひ成功してもらって、加齢黄斑変性への拡大も取り組んでほしいな、患者さんのために。こちらも期待しているぞ!
8.おわりに
特許法の趣旨は発明の保護及び利用を図ることにより、発明を奨励し、産業の発達に寄与することですが、その一方で発明の保護は公共の利益との間でしばしば対立が生じます。
特にライフサイエンスに関連する場合は、公共の利益が国民の生命や健康に直接関わるため、議論が対立し先鋭化します。
本裁定請求事件は、当事者どうしの自発的な解決により、iPS細胞による再生医療の実用化へ向けて前進することとなり、特許法の趣旨に合致した結果となりました。
しかし、本裁定請求事件からは、政府の介入に関する規定の整備が必要であることなどの課題も浮かび上がってきました。
強制的な実施権の安易な設定は、特許権による競争力、すなわち、医療・産業への投資やライセンス関係構築、を弱体化させ、産業の発展を減退させる可能性があります。
そのため、公共の利益、特許権者の実施状況、政策的観点などを総合的に考慮し、強制実施権の設定に慎重な検討が必要です。とは言っても、緊急実施が求められる裁定のためには迅速な審議運営が求められます。
本裁定請求事件を教訓として、浮かび上がってきた上記の様々な課題に対処するために、政府が中心となって議論を進めていくことを期待します。
最後に、この和解により、iPS細胞を利用した再生医療が患者の皆さまに早く提供されることをお祈りいたします。




コメント
2024.08.05 住友ファーマ press release: 他家iPS細胞由来網膜⾊素上⽪細胞のフェーズ1/2試験における最初の被験者への移植のお知らせ
https://www.sumitomo-pharma.co.jp/news/20240805.html
住友ファーマは、ヘリオスと日本国内で共同開発を進めている他家iPS細胞由来網膜色素上皮(RPE)細胞(開発コード:HLCR011)の網膜色素上皮裂孔の患者を対象とするフェーズ1/2試験において、最初の被験者への移植が九州大学病院にて行われたことを発表した。今後、一定期間経過観察の上、安全性の問題が認められなければ、ランダム化フェーズ(Part2)へと移行する予定。
本治験の開始については、2023年6月23日に開示している。
https://www.sumitomo-pharma.co.jp/news/20230623.html
2024.08.05 ヘリオス press release: 他家 iPS 細胞由来網膜色素上皮細胞(HLCR011)を用いた網膜色素上皮裂孔を対象とした治験における被験者組み入れ開始のお知らせ
https://ssl4.eir-parts.net/doc/4593/tdnet/2483239/00.pdf
先週(2月6日)の先進医療会議で取り上げられていた、RPE細胞凝集紐移植。
使用する再生医療等製品に企業名などの記載がなかったので、なぜかな?と思い、調べて当サイトにたどり着きました。
たぶん、この先進医療会議で扱う製品は、MastCT-02なんだな…ということが理解できました。
MastCT-02ですが、昨年12/27に、J-TEC(帝人グループ)がVCCTと資本提携したようです。
https://www.jpte.co.jp/sys/upload/save/3850607606785b7a36ea04.pdf
とても勉強になりました。ありがとうございました。